Clear Sky Science · nl
DC-CD4 bispecifieke tolerogene nanovesikels wekken antigeenspecifieke regulatoire T-cellen op en verbeteren collageen-geïnduceerde artritis bij muizen
Het immuunsysteem leren wanneer het niet moet aanvallen
Auto-immuunziekten ontstaan wanneer het verdedigingsstelsel van het lichaam ten onrechte het eigen weefsel aanvalt, wat leidt tot chronische pijn en schade. In plaats van de immuniteit algemeen uit te schakelen, zoeken wetenschappers naar manieren om deze verdediging opnieuw te trainen zodat ze specifieke onschadelijke doelen negeert terwijl ze echte bedreigingen blijft bestrijden. Deze studie bij muizen beschrijft een klein, geconstrueerd pakket dat precies dat beoogt, en hint naar preciezere behandelingen voor aandoeningen zoals reumatoïde artritis in de toekomst. 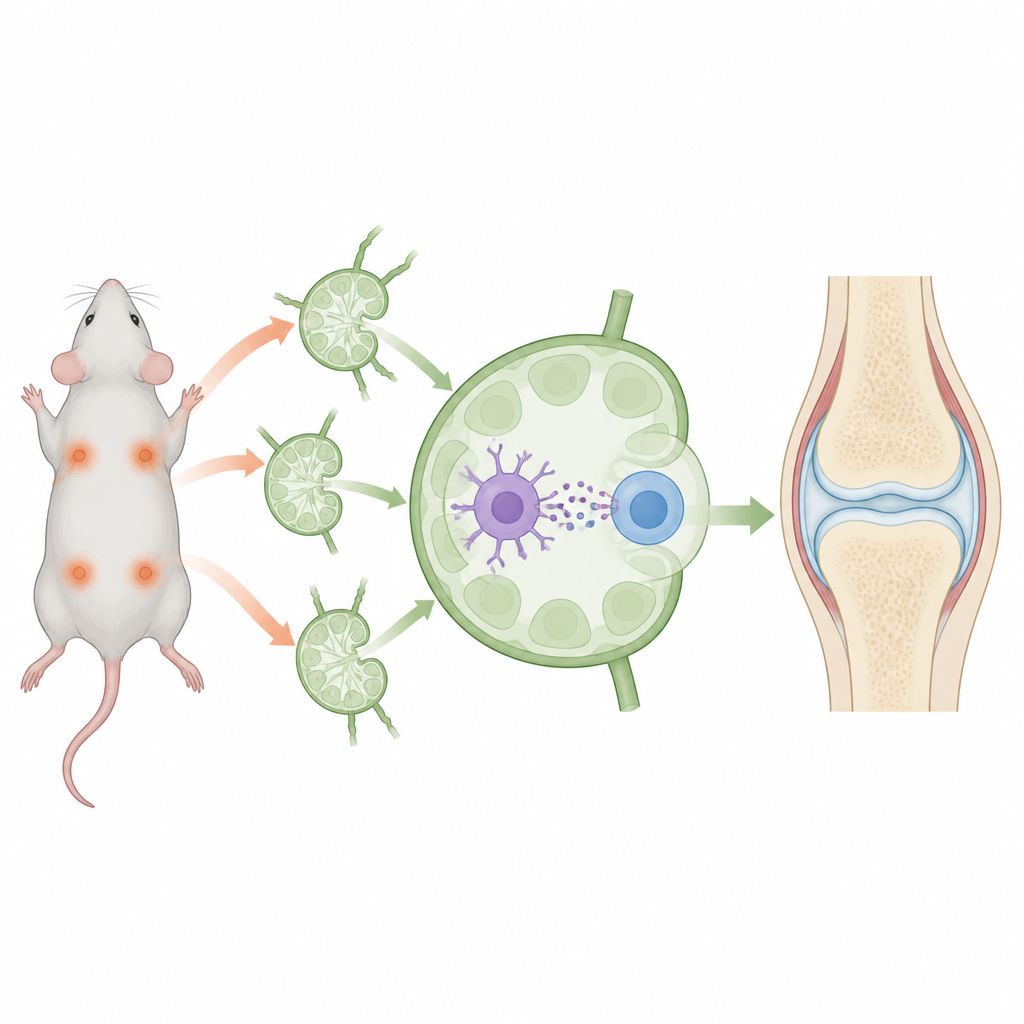
Waarom het dempen van de juiste cellen ertoe doet
Een gezond immuunsysteem kan het verschil zien tussen “zelf” en “indringer,” een evenwicht dat bekendstaat als immuuntolerantie. Speciale witte bloedcellen, regulatoire T-cellen, fungeren als vredestichters en kalmeren schadelijke reacties voordat ze uitgroeien tot ziekte. Artsen hebben geprobeerd deze cellen te versterken door ze buiten het lichaam te laten groeien en terug te infunderen, of door medicijnen te gebruiken die hun groei in het lichaam bevorderen. Beide wegen hebben nadelen, waaronder complexe celverwerking en het risico de immuniteit te zeer te dempen. Het doel is alleen die regulatoire cellen te vergroten die herkenning hebben voor de problematische zelf-moleculen die aan een specifieke ziekte gekoppeld zijn.
Ontwerpen van piepkleine vredespakketten
De onderzoekers bouwden nanoschaal belletjes, of nanovesikels, uit de buitenmembraan van immuuncellen die al kalmerende eigenschappen hebben. Deze vesikels werden geladen met twee sleutelbestanddelen: een kort fragment van collageen, een gewrichtsproteïne die bij artritis doelwit is, en het geneesmiddel rapamycine, dat een tolerantere immuunstatus bevordert. De nanovesikels werden vervolgens "versierd" zodat ze zich aan twee verschillende partners in lymfeklieren konden hechten: dendritische cellen, die antigenen presenteren, en CD4 T-cellen, die ofwel agressieve strijders of regulatoire vredestichters kunnen worden. Door deze twee celtypen fysiek samen te brengen rond hetzelfde collageenfragment en medicijn, waren de vesikels ontworpen om het gesprek richting tolerantie in plaats van aanval te duwen.
Immuunverkeer naar de juiste plaats leiden
Wanneer in de huid van muizen geïnjecteerd, dreven de nanovesikels naar nabijgelegen lymfeklieren, de knooppunten waar immuunbeslissingen worden genomen. Daar hechtten ze sterk aan zowel dendritische cellen als CD4 T-cellen en fungeerden effectief als bruggen tussen hen. Vergeleken met vrij gegeven medicijn en collageen leverden de vesikels veel meer materiaal aan dendritische cellen en versterkten ze sterk hoe goed deze cellen het collageenfragment presenteerden. Tegelijkertijd verschoven zowel dendritische cellen als CD4 T-cellen naar een stiller, meer regulatoir profiel, met minder ontstekingssignalen en meer kalmerende stoffen zoals TGF-beta en IL-10. Deze omgeving bevorderde de groei van collageenspecifieke regulatoire T-cellen die later immuunaanvallen gericht op gewrichten zouden herkennen en beteugelen.
Gewrichten beschermen in een artritismodel
Om te testen of deze immuunheropvoeding van belang was voor ziekte, gebruikte het team een standaard muismodel van collageen-geïnduceerde artritis, dat veel kenmerken van menselijke reumatoïde artritis nabootst. Muizen behandeld met collageen-geladen nanovesikels ontwikkelden veel mildere gewrichtszwellingen, behielden meer normale beweging en verloren minder gewicht dan onbehandelde dieren. Gedetailleerde beeldvorming en weefseldoorsneden toonden minder gewrichtserosie, minder tekenen van actieve ontsteking en verminderde littekenvorming bij behandelde muizen. Belangrijk was dat regulatoire T-cellen toenamen, niet alleen in lymfeklieren en milt maar ook in het gewrichtsvlies zelf, terwijl schadelijke ontstekingsmoleculen daalden. Versies van de nanovesikels die het juiste antigeen misten of die beide celtypen niet effectief konden verbinden, gaven zwakkere bescherming, wat het belang van zowel antigeenkeuze als cel-tot-cel koppeling onderstreept. 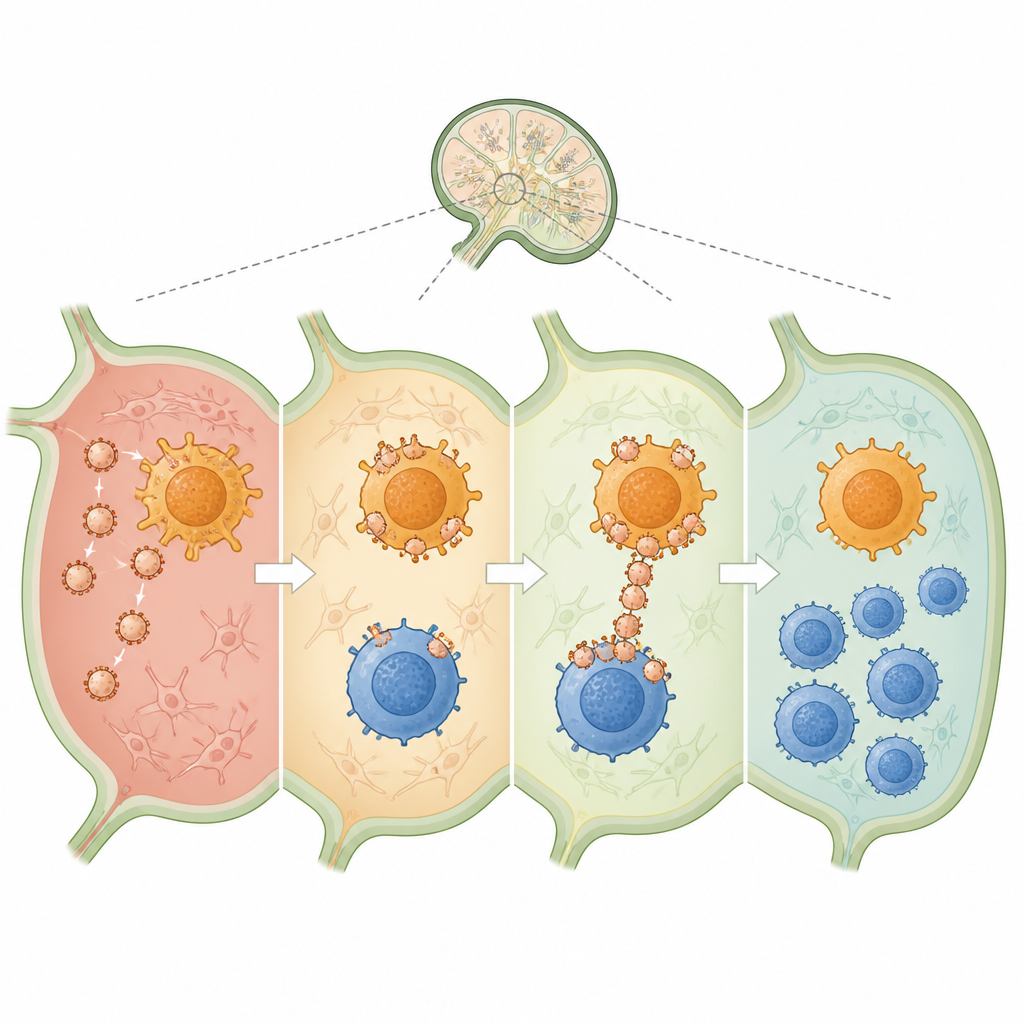
Duurzame rust en wat erna komt
De onderzoekers toonden verder aan dat de regulatoire T-cellen die door deze nanovesikels werden opgewekt bescherming konden overdragen aan andere muizen en konden helpen een latere opvlamming van artritis te weerstaan, wat suggereert dat het immuunsysteem de les "onthoudt." Hoewel het werk nog beperkt is tot muizen en één artritismodel, wijst het op een flexibele platformbenadering waarbij ziektespecifieke zelffragmenten kunnen worden verwisseld om de immuniteit bij verschillende auto-immuuncondities te hertrainen. Voor patiënten is het doel van deze benadering niet het immuunsysteem volledig stil te leggen, maar het te leren alleen terughoudend te zijn op de plekken waar het schade aanricht.
Bronvermelding: Zhao, L., Gao, Z., Yuan, Z. et al. DC-CD4 bispecific tolerogenic nanovesicles induce antigen-specific regulatory T cells and ameliorate collagen-induced arthritis in mice. Nat Commun 17, 4170 (2026). https://doi.org/10.1038/s41467-026-70898-y
Trefwoorden: auto-immuun tolerantie, regulatoire T-cellen, nanovesikels, reumatoïde artritis, immuuntherapie