Clear Sky Science · pl
Dwufunkcyjne tolerogenne nanowezikuly DC‑CD4 indukują swoiste wobec antygenu limfocyty T regulatorowe i łagodzą zapalenie stawów indukowane kolagenem u myszy
Nauka układu odpornościowego, kiedy nie atakować
Choroby autoimmunologiczne pojawiają się, gdy system obronny organizmu błędnie zwraca się przeciw własnym tkankom, prowadząc do przewlekłego bólu i uszkodzeń. Zamiast szeroko wyłączać odporność, naukowcy poszukują sposobów przeuczenia jej tak, aby ignorowała konkretne, nieszkodliwe cele, a jednocześnie dalej zwalczała prawdziwe zagrożenia. To badanie na myszach opisuje maleńkie, zaprojektowane „opakowanie”, które ma właśnie taki cel, sugerując możliwość bardziej precyzyjnych terapii np. w reumatoidalnym zapaleniu stawów w przyszłości. 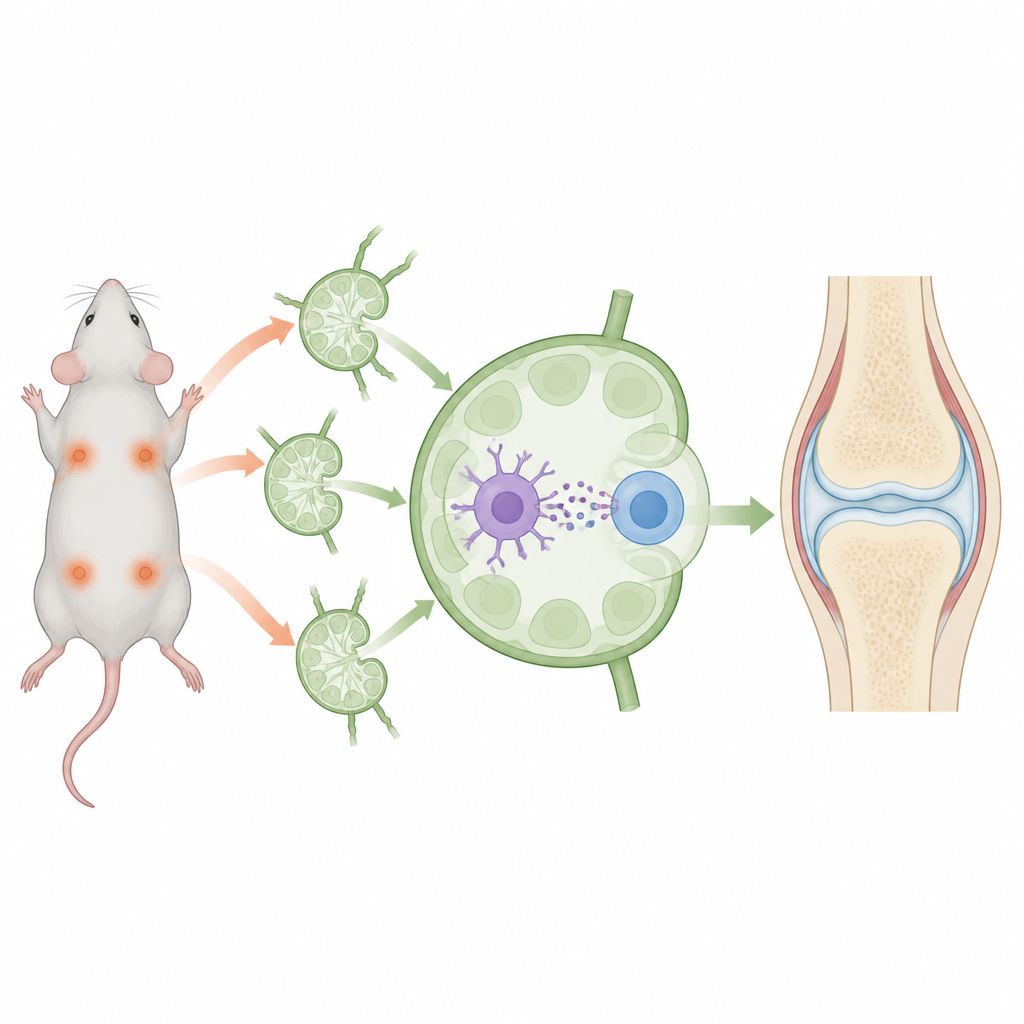
Dlaczego ważne jest wyciszanie właściwych komórek
Zdrowy układ odpornościowy potrafi odróżnić „siebie” od „intruza”, równowaga ta znana jest jako tolerancja immunologiczna. Specjalne białe krwinki zwane limfocytami T regulatorowymi działają jak strażnicy pokoju, tonując szkodliwe reakcje nim przerodzą się w chorobę. Lekarze próbowali zwiększać ich liczbę albo przez hodowlę pozaustrojową i przetoczenie, albo przez leki sprzyjające ich rozwojowi in vivo. Obie drogi mają wady, w tym skomplikowaną obsługę komórek i ryzyko nadmiernego stłumienia odporności. Celem jest zwiększyć jedynie te komórki regulatorowe, które rozpoznają konkretne, problematyczne cząsteczki własne związane z daną chorobą.
Projektowanie małych „paczuszek” strażników pokoju
Naukowcy zbudowali nanometryczne pęcherzyki, czyli nanowezikuly, z błon zewnętrznych komórek odpornościowych, które już mają właściwości uspokajające. Do tych pęcherzyków załadowano dwa kluczowe składniki: krótki fragment kolagenu, białka stawów będącego celem w zapaleniu stawów, oraz lek rapamycynę, który sprzyja stanie bardziej tolerancyjnemu układu odpornościowego. Nanowezikuly zostały następnie „ozdobione”, aby mogły przyczepiać się do dwóch różnych partnerów w węzłach chłonnych: komórek dendrytycznych, które prezentują antygeny, oraz limfocytów CD4, które mogą stać się albo agresywnymi bojownikami, albo regulatorami przywracającymi spokój. Poprzez fizyczne zbliżenie tych dwóch typów komórek wokół tego samego fragmentu kolagenu i leku, wezikuly miały skłaniać komunikację ku tolerancji zamiast ataku.
Kierowanie ruchem immunologicznym we właściwe miejsce
Po wstrzyknięciu do skóry myszy, nanowezikuly spływały do pobliskich węzłów chłonnych, ośrodków, gdzie zapadają decyzje odpornościowe. Tam silnie przyłączały się zarówno do komórek dendrytycznych, jak i do limfocytów CD4, skutecznie działając jako mosty między nimi. W porównaniu z wolnym lekiem i kolagenem, wezikuly dostarczyły znacznie więcej materiału do komórek dendrytycznych i znacznie zwiększyły to, jak dobrze te komórki prezentowały fragment kolagenu. Jednocześnie przesunęły zarówno komórki dendrytyczne, jak i limfocyty CD4 w stronę cichszego, bardziej regulatorowego profilu, z mniejszą liczbą sygnałów zapalnych i większą ilością czynników uspokajających, takich jak TGF‑beta i IL‑10. Takie warunki sprzyjały wzrostowi kolagen‑swoistych limfocytów T regulatorowych, które później rozpoznawały i hamowały ataki układu odpornościowego skierowane na stawy.
Ochrona stawów w modelu zapalenia stawów
Aby sprawdzić, czy ta reedukacja odporności ma znaczenie dla choroby, zespół użył standardowego modelu mysiego zapalenia stawów indukowanego kolagenem, który naśladuje wiele cech ludzkiego reumatoidalnego zapalenia stawów. Myszy leczone nanowezikulami z załadowanym kolagenem rozwijały znacznie łagodniejszy obrzęk stawów, zachowywały bardziej normalną ruchomość i mniej traciły na wadze niż zwierzęta nieleczone. Szczegółowe obrazowanie i preparaty tkankowe wykazały mniejszą erozję stawów, mniej oznak aktywnego zapalenia i zredukowane bliznowacenie u leczonych myszy. Co ważne, limfocyty T regulatorowe zwiększyły się nie tylko w węzłach chłonnych i śledzionie, ale także w samej wyściółce stawu, podczas gdy szkodliwe cząsteczki zapalne spadły. Wersje nanowezikul, którym brakowało odpowiedniego antygenu lub które nie mogły skutecznie łączyć obu typów komórek, dawały słabszą ochronę, podkreślając znaczenie wyboru antygenu i łączenia komórka‑komórka. 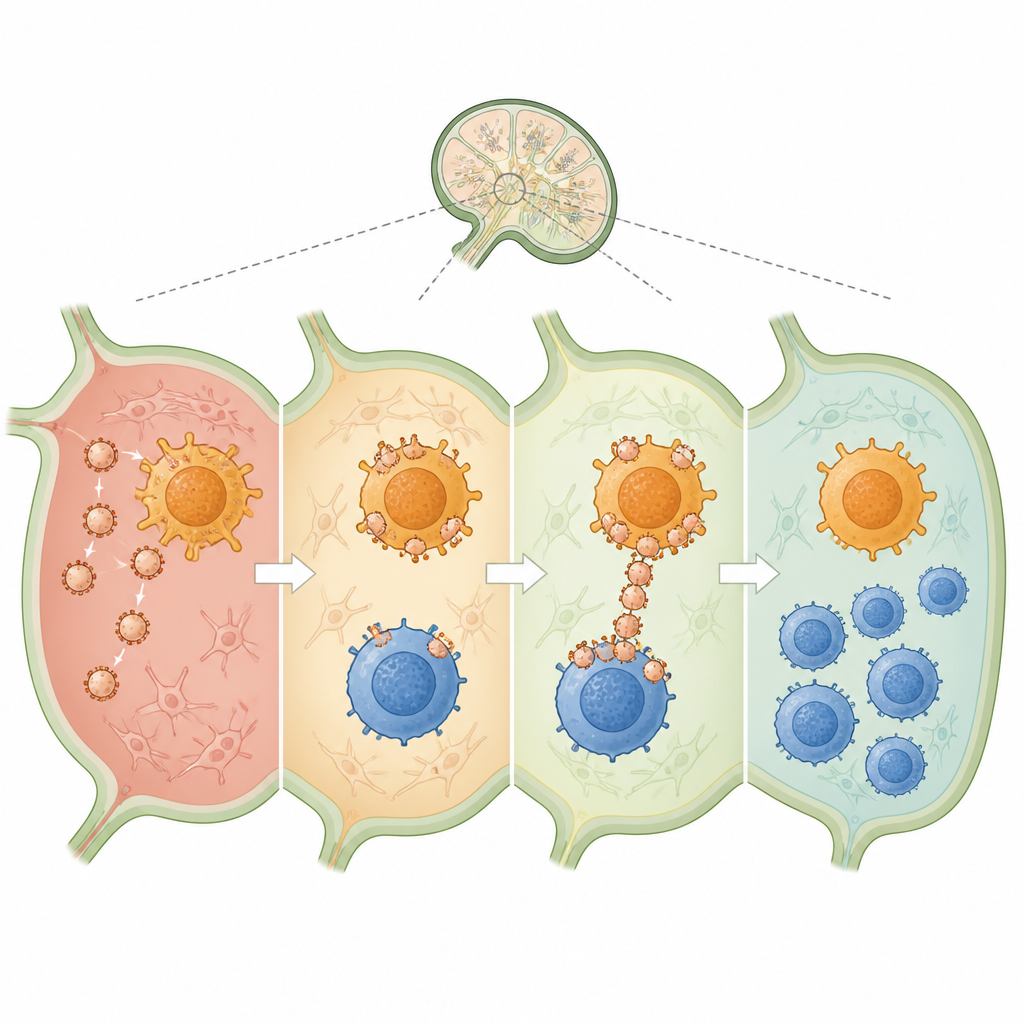
Trwały spokój i co dalej
Naukowcy wykazali ponadto, że limfocyty T regulatorowe wywołane przez te nanowezikuly mogły przenosić ochronę na inne myszy i pomagać przeciwstawić się późniejszemu nawrotowi zapalenia stawów, co sugeruje, że układ odpornościowy „zapamiętuje” otrzymaną lekcję. Choć prace wciąż ograniczają się do myszy i jednego modelu zapalenia stawów, wskazują na elastyczną platformę, w której można by zamieniać fragmenty własne specyficzne dla danej choroby, by reedukować odporność w różnych schorzeniach autoimmunologicznych. Dla pacjentów podejście to ma na celu nie uciszenie całego układu odpornościowego, lecz nauczenie go wycofywania się tylko tam, gdzie wyrządza szkodę.
Cytowanie: Zhao, L., Gao, Z., Yuan, Z. et al. DC-CD4 bispecific tolerogenic nanovesicles induce antigen-specific regulatory T cells and ameliorate collagen-induced arthritis in mice. Nat Commun 17, 4170 (2026). https://doi.org/10.1038/s41467-026-70898-y
Słowa kluczowe: tolerancja autoimmunologiczna, limfocyty T regulatorowe, nanowezikuly, reumatoidalne zapalenie stawów, terapia immunologiczna