Clear Sky Science · zh
哺乳动物线粒体内膜中呼吸超复合体和ATP合酶寡聚体的结构
细胞内的发电厂
每秒钟,体内细胞中有数万亿台微小机器产生维持生命所需的能量。本文以非同寻常的视角细致审视线粒体中一些最重要的这些机器——细胞的所谓“发电厂”。作者利用最前沿的电子显微技术,揭示了这些产能蛋白复合体在天然膜环境中的位置、它们如何组合成更大的装配体,以及它们的形态如何塑造线粒体内部的结构。这些细节重要,因为这些结构的微小缺陷与代谢性疾病和线粒体紊乱有关。
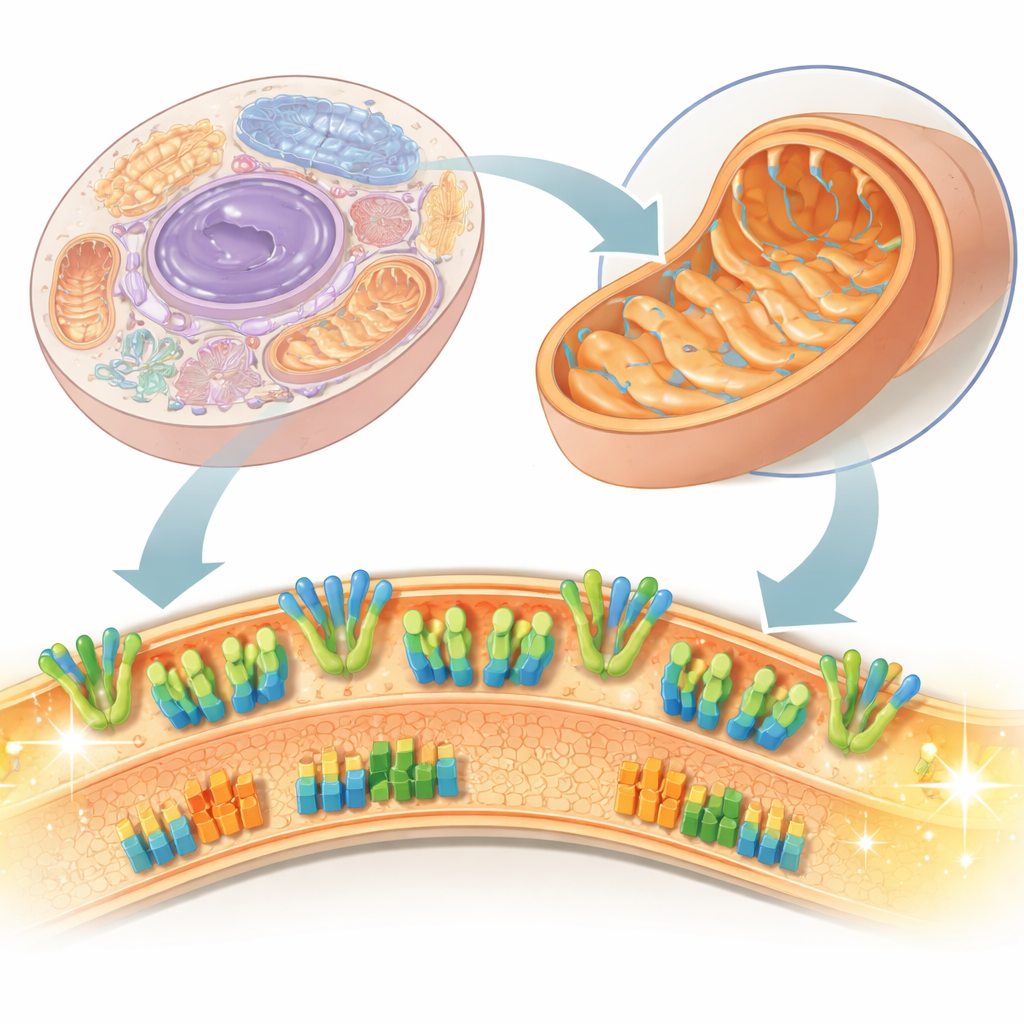
发电厂的内部景观
线粒体有两层膜,真正的能量转换发生在内膜。内膜上存在两类主要蛋白机器:呼吸链,负责转移电子并泵出质子以在膜两侧产生电位;以及ATP合酶,利用该电位合成ATP——细胞的“能量货币”。传统上,科学家常在用去污剂提取蛋白后研究它们,但这可能破坏脆弱的相互作用和脂质。在这项工作中,研究者使用了亚线粒体颗粒——从牛心线粒体剥离的小囊泡——并在冷冻的、接近天然的状态下直接用冷冻电子显微镜对其成像。此方法不仅让他们看到单个蛋白,还能观察这些蛋白在实际膜中如何排列与协同工作。
塑造产生能量的褶脊
一项最引人注目的发现涉及ATP合酶,这种旋转酶负责制造ATP。先前研究表明两个ATP合酶可能配对形成V形,更大的群体可能将内膜弯成称为嵴(cristae)的狭窄褶脊,但尚不清楚更大装配体是真实存在还是提取过程中的人工产物。在这里,作者明确观察到ATP合酶二聚体由一个小的调控蛋白连接,成对嵌入膜中。更重要的是,他们在天然膜中看到了线性四聚体——两个二聚体并列排列。这些四聚体位于高曲率区域,并集体将膜弯成U形剖面,支持ATP合酶装配体主动塑造哺乳动物线粒体嵴尖的观点。
旋转机器的精细结构
研究还对ATP合酶的跨膜部分进行了放大观察,揭示了一些挑战早期解释的细节。一个蛋白亚基环(c8环)在膜中旋转,早期基于去污剂的结构在该环内显示出额外密度,被认为是与另一个亚基(称为e)相互作用的紧密结合脂质。然而在天然膜中,作者发现该环内的内向密度很弱或不存在,这表明先前观察到的可能实际上是去污剂分子而非必需脂质。相反,他们的图谱暗示e亚基的末端可能携带小的化学修饰并直接与环相互作用。这种微妙的重排改变了科学家对于膜电位如何通过机械联动驱动ATP生成的想象。
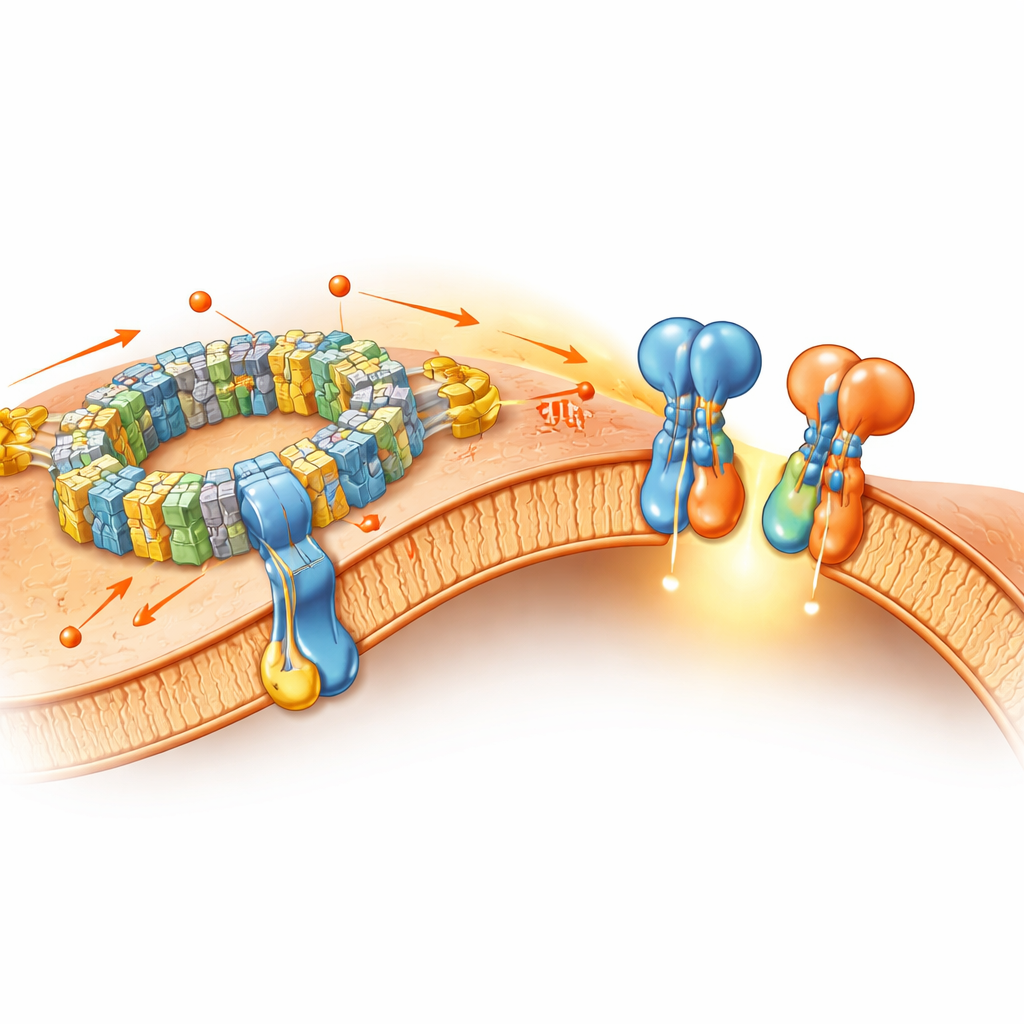
能量机器的协作
除了ATP合酶,论文还探讨了呼吸链复合体——编号为I、III和IV的复合体——如何聚集成“超复合体”。在他们的天然膜样品中,作者不仅发现了先前已知的组合(例如一个复合体I与一个复合体III二聚体及一份或两份复合体IV),还发现了一种包含三个复合体IV附着在核心单元的新形式,甚至发现了一个巨大的“巨复合体”,包含两个复合体I、一个复合体III二聚体和六份复合体IV。这些高阶装配体会略微弯曲膜,并很可能优化电子和质子的传递,从而提高能量转换效率。与此同时,单个复合体在细微尺度上的结构大体保留了传统纯化样品中看到的特征,表明许多核心结构在去污剂处理下仍能保留。
对健康与疾病的意义
通过保留这些蛋白机器的自然环境,这项工作提供了线粒体“硬件”在活细胞中组织方式的更真实快照。作者表明ATP合酶四聚体是真实存在于哺乳动物线粒体中的结构,并帮助塑造聚集ATP生成的尖锐褶脊。他们还展示了比先前认识更丰富的呼吸超复合体和巨复合体种类。由于这些复合体的突变和组装方式的改变与代谢紊乱、线粒体疾病乃至细胞死亡的早期步骤有关,这张结构图为未来研究奠定了坚实基础。简言之,本文解释了细胞中最微小的涡轮与“电线”的布局与协作如何保持我们的能量供应顺畅——以及微小的接线错误如何可能促成人类疾病。
引用: Nakano, A., Masuya, T., Akisada, S. et al. Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane. Nat Commun 17, 4075 (2026). https://doi.org/10.1038/s41467-026-70578-x
关键词: 线粒体, ATP合酶, 呼吸超复合体, 冷冻电子显微镜, 线粒体疾病