Clear Sky Science · ru
Структуры респираторных суперкомплексов и олигомеров АТФ‑синтазы во внутренней митохондриальной мембране млекопитающих
Электростанции внутри наших клеток
Каждую секунду триллионы крошечных машин внутри ваших клеток вырабатывают энергию, которая поддерживает жизнь. В этой работе даётся необычайно близкий взгляд на одни из наиболее важных таких машин в митохондриях — так называемых «электростанций» клетки. С помощью передовой электронной микроскопии авторы показывают, как протеиновые комплексы, производящие энергию, располагаются в своей природной мембранной среде, как они объединяются в более крупные структуры и как их формы помогают формировать внутреннюю архитектуру митохондрий. Эти детали важны, потому что тонкие дефекты в этих структурах связаны с нарушениями обмена веществ и митохондриальными заболеваниями.
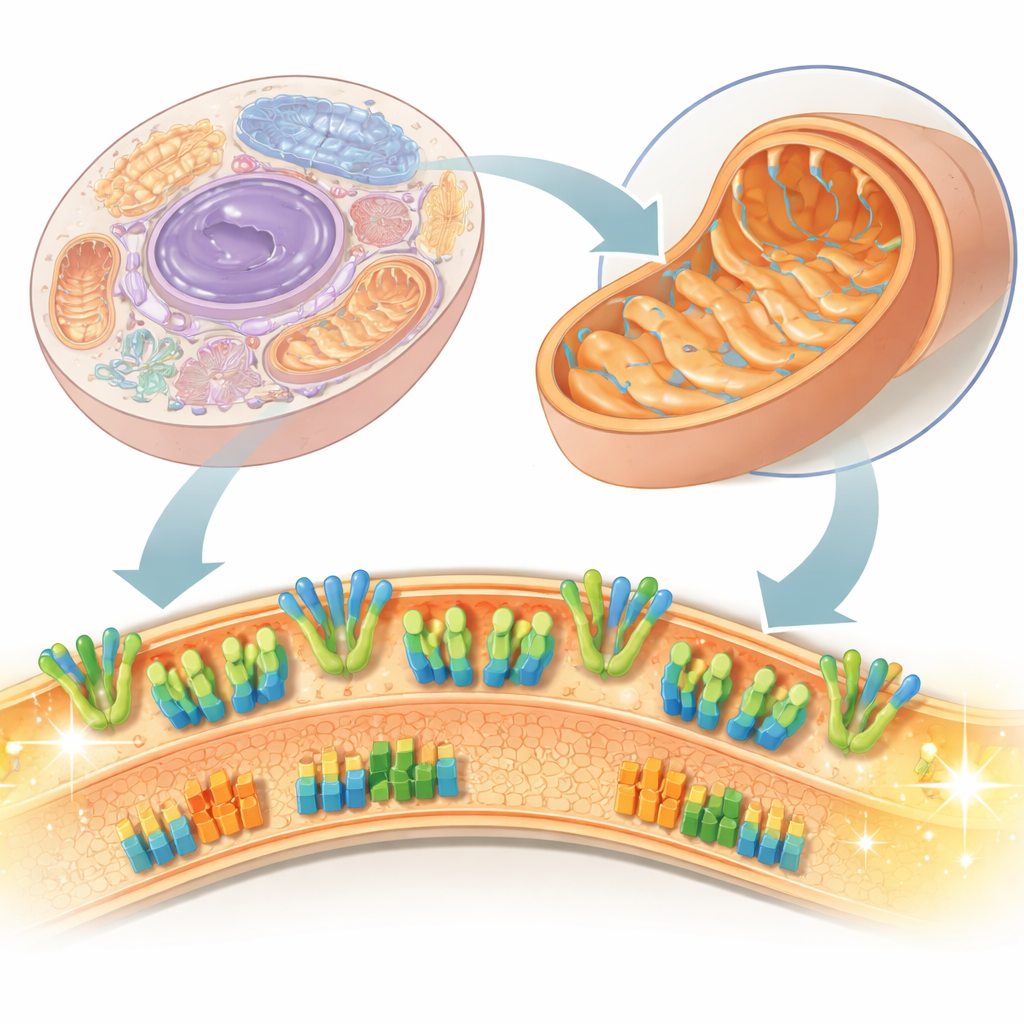
Внутренний ландшафт «электростанции»
У митохондрий две мембраны, и внутренняя — это место, где происходит основное производство энергии. В ней расположены два крупных набора протеиновых машин: респираторная цепь, которая перемещает электроны и перекачивает протоны, создавая потенциал через мембрану, и АТФ‑синтаза, использующая этот потенциал для синтеза АТФ — «энергетической валюты» клетки. Традиционно эти белки изучали после их извлечения с помощью детергентов, что могло нарушать слабые взаимодействия и липиды. В этой работе исследователи используют субмитохондриальные частицы — небольшие везикулы, полученные из митохондрий коровьего сердца — и изображают их непосредственно в замороженном, близком к нативному состоянии с помощью крио‑электронной микроскопии. Такой подход позволяет видеть не только отдельные белки, но и то, как они организованы и взаимодействуют в реальной мембране.
Формирование гребней, где создаётся энергия
Одно из наиболее впечатляющих наблюдений касается АТФ‑синтазы, ротора‑фермента, который синтезирует АТФ. Ранние исследования предполагали, что две единицы АТФ‑синтазы могут образовывать V‑образную пару, а большие группы способны изгибать внутреннюю мембрану в плотные гребни — кристы. Однако оставалось неясным, являются ли такие крупные сборки естественными или артефактами подготовки образца. В этой работе авторы однозначно видят димеры АТФ‑синтазы, соединённые небольшим регуляторным белком, встроенные в мембрану. Ещё важнее то, что они наблюдают линейные тетрамеры — две димерные пары, расположенные рядом — прямо в нативной мембране. Эти тетрамеры сидят в участках с резким изгибом и совместно изгибают мембрану в U‑образный профиль, поддерживая идею о том, что ансамбли АТФ‑синтазы активно формируют кончики крист митохондрий млекопитающих.
Тонкие детали ротора
Исследование также в деталях рассматривает мембрано‑проникающую часть АТФ‑синтазы, обнаруживая особенности, которые ставят под вопрос предыдущие интерпретации. Кольцо белковых субъединиц (c8‑кольцо) вращается в мембране, и ранние структуры, полученные с детергентами, показывали дополнительную плотность внутри этого кольца, которую считали плотно связанные липиды, взаимодействующие с другой субъединией (обозначаемой как e). В нативной мембране, однако, авторы находят, что эта внутренняя плотность очень слабая или отсутствует, что указывает на то, что ранее наблюдавшиеся объекты могли быть молекулами детергентов, а не важными липидами. Вместо этого их карты намекают, что конец e‑субъединицы, возможно несущий небольшую химическую модификацию, взаимодействует непосредственно с кольцом. Эта тонкая перестройка меняет представление о механической связи, благодаря которой мембранный потенциал приводит к синтезу АТФ.
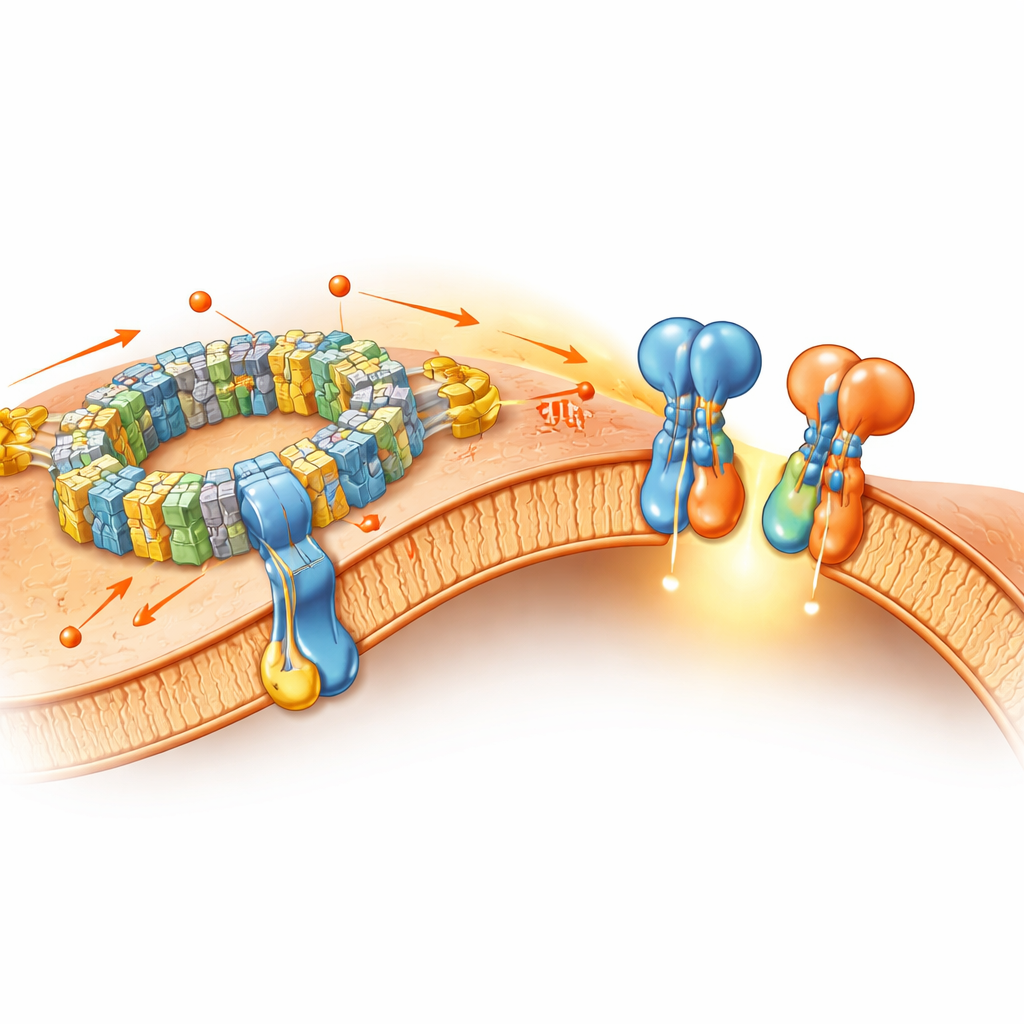
Энергетические машины объединяются
Помимо АТФ‑синтазы, статья исследует, как комплексы респираторной цепи — обозначаемые как I, III и IV — образуют кластеры или «суперкомплексы». В их нативных мембранных образцах авторы находят не только ранее известные сочетания (например, один комплекс I с димером комплекса III и одной‑двумя копиями комплекса IV), но и новую форму с тремя копиями комплекса IV, присоединёнными к ядру, а также гигантский «мегакомплекс», содержащий два комплекса I, димер комплекса III и шесть копий комплекса IV. Эти высокоорганизованные сборки слегка изгибают мембрану и, вероятно, оптимизируют пути переноса электронов и протонов, повышая эффективность преобразования энергии. При этом отдельные комплексы в основном сохраняют те же тонкоструктурные черты, что и в традиционно очищенных образцах, что указывает на то, что многие их основные свойства выживают при подготовке с детергентами.
Значение для здоровья и болезней
Сохраняя природный контекст этих протеиновых машин, работа даёт более точную картину того, как «аппаратное обеспечение» митохондрий организовано в живых клетках. Авторы показывают, что тетрамеры АТФ‑синтазы действительно присутствуют в митохондриях млекопитающих и способствуют формированию острых гребней, где сосредоточено производство АТФ. Они также раскрывают более богатое разнообразие респираторных суперкомплексов и мегакомплексов, чем считалось ранее. Поскольку мутации в этих комплексах и изменения в их сборке связаны с нарушениями метаболизма, митохондриальными болезнями и даже ранними этапами запрограммированной клеточной гибели, эта структурная карта даёт прочную основу для дальнейших исследований. Проще говоря, работа объясняет, как планировка и сотрудничество крошечных турбин и проводящих цепочек клетки помогают поддерживать стабильное снабжение энергией — и как тонкие нарушения «проводки» могут способствовать развитию заболеваний человека.
Цитирование: Nakano, A., Masuya, T., Akisada, S. et al. Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane. Nat Commun 17, 4075 (2026). https://doi.org/10.1038/s41467-026-70578-x
Ключевые слова: митохондрии, АТФ‑синтаза, респираторные суперкомплексы, криоэлектронная микроскопия, митохондриальные заболевания