Clear Sky Science · de
Strukturen respiratorischer Superkomplexe und Oligomere der ATP‑Synthase in der inneren Membran von Säugetiermitochondrien
Kraftwerke in unseren Zellen
Sekündlich erzeugen Billionen winziger Maschinen in Ihren Zellen die Energie, die Sie am Leben hält. Dieses Paper wirft einen ungewöhnlich genauen Blick auf einige der wichtigsten dieser Maschinen in den Mitochondrien, den sogenannten „Kraftwerken“ der Zelle. Mithilfe moderner Elektronenmikroskopie zeigen die Autorinnen und Autoren, wie energieliefernde Proteinkomplexe in ihrer nativen Membranumgebung sitzen, wie sie sich zu größeren Verbänden zusammenfinden und wie ihre Formen die innere Architektur der Mitochondrien mitprägen. Diese Details sind wichtig, weil feine Defekte in diesen Strukturen mit Stoffwechselerkrankungen und mitochondrialen Störungen verknüpft sind.
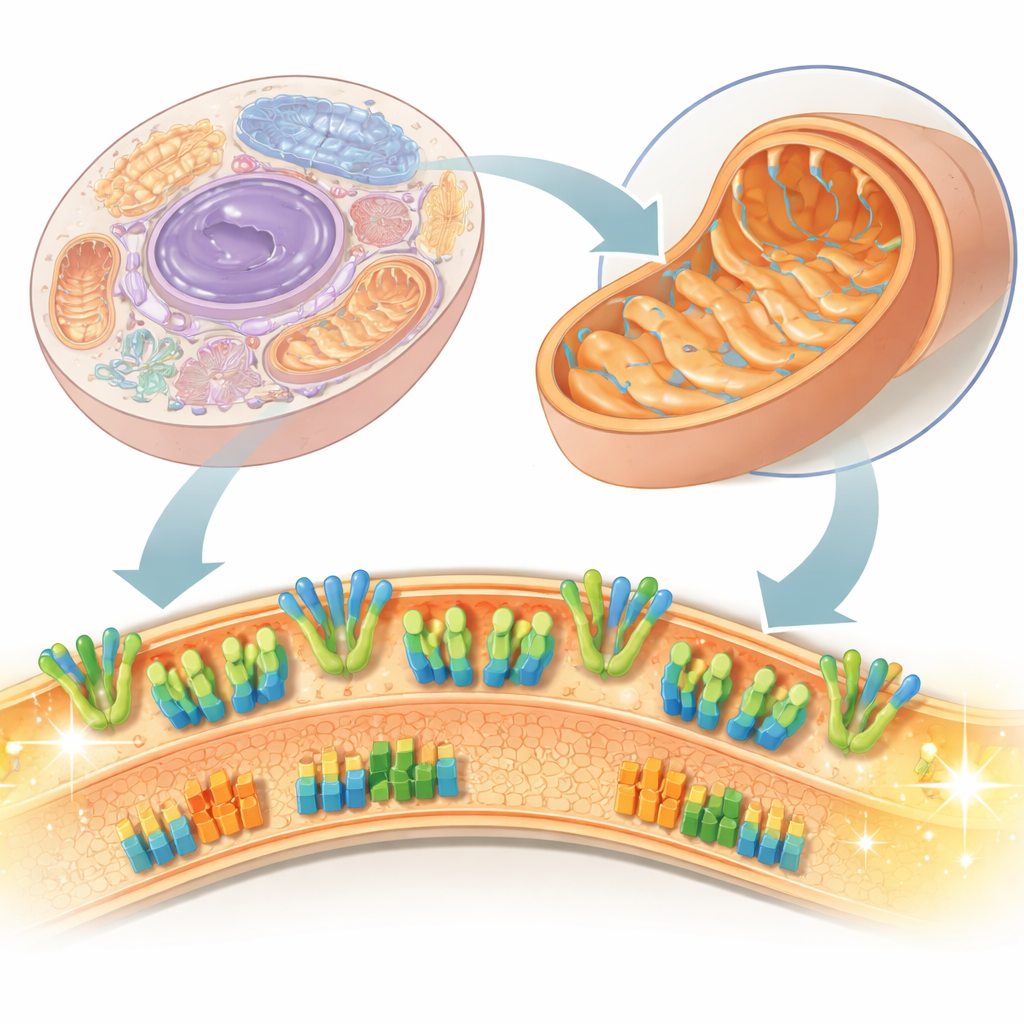
Die innere Landschaft eines Kraftwerks
Mitochondrien besitzen zwei Membranen; die innere ist der Ort, an dem die eigentliche Energiegewinnung stattfindet. Dort sitzen zwei große Gruppen von Proteinmaschinen: die Atmungskette, die Elektronen transportiert und Protonen pumpt, um eine Spannung über die Membran aufzubauen, und die ATP‑Synthase, die diese Spannung nutzt, um ATP herzustellen, die „Energieeinheit“ der Zelle. Üblicherweise wurden diese Proteine nach Extraktion mit Detergenzien untersucht, was empfindliche Wechselwirkungen und Lipide stören kann. In dieser Arbeit verwenden die Forschenden sub‑mitochondriale Partikel – kleine Vesikel, die aus Rinderherz‑Mitochondrien gewonnen wurden – und untersuchen sie direkt in einem eingefrorenen, naturnahen Zustand mittels Kryo‑Elektronenmikroskopie. Dieser Ansatz erlaubt es, nicht nur einzelne Proteine, sondern auch ihre Anordnung und Kooperation in der tatsächlichen Membran zu sehen.
Die Rillen, in denen Energie entsteht, formen
Eines der auffälligsten Ergebnisse betrifft die ATP‑Synthase, das rotierende Enzym, das ATP herstellt. Frühere Studien legten nahe, dass sich zwei ATP‑Synthase‑Einheiten zu einer V‑Form paaren können und dass größere Gruppen die innere Membran zu dicht gebogenen Rillen (Cristae) formen könnten; unklar war jedoch, ob größere Assemblierungen natürlich sind oder Artefakte der Extraktion. Hier sehen die Autorinnen und Autoren deutlich ATP‑Synthase‑Dimere, die durch ein kleines regulatorisches Protein verbunden sind und in der Membran eingebettet liegen. Noch wichtiger: Sie beobachten lineare Tetramere – zwei Dimere nebeneinander angeordnet – direkt in der nativen Membran. Diese Tetramere sitzen an stark gekrümmten Bereichen und biegen die Membran kollektiv zu einem U‑förmigen Profil, was die Idee stützt, dass ATP‑Synthase‑Verbände aktiv die Spitzen der Cristae in Säugetiermitochondrien formen.
Feine Details der rotierenden Maschine
Die Studie zoomt außerdem in den membranüberspannenden Anteil der ATP‑Synthase und zeigt Details, die frühere Interpretationen in Frage stellen. Ein Ring von Proteinsubunits (der c8‑Ring) rotiert in der Membran; frühere detergenbasierte Strukturen zeigten zusätzliche Dichte innerhalb dieses Rings, die als fest gebundene Lipide interpretiert wurde, die mit einer anderen Untereinheit (genannt e) interagieren. In der nativen Membran finden die Autorinnen und Autoren jedoch, dass diese innere Dichte sehr schwach oder gar nicht vorhanden ist, was darauf hindeutet, dass das zuvor sichtbare Material möglicherweise Detergensubstanzen und nicht essentielle Lipide waren. Stattdessen deuten ihre Karten darauf hin, dass das Ende der e‑Untereinheit, möglicherweise mit einer kleinen chemischen Modifikation, direkt mit dem Ring interagiert. Diese subtile Umordnung verändert die Vorstellung davon, wie die mechanische Verbindung aussieht, die es der Membranspannung ermöglicht, die ATP‑Produktion anzutreiben.
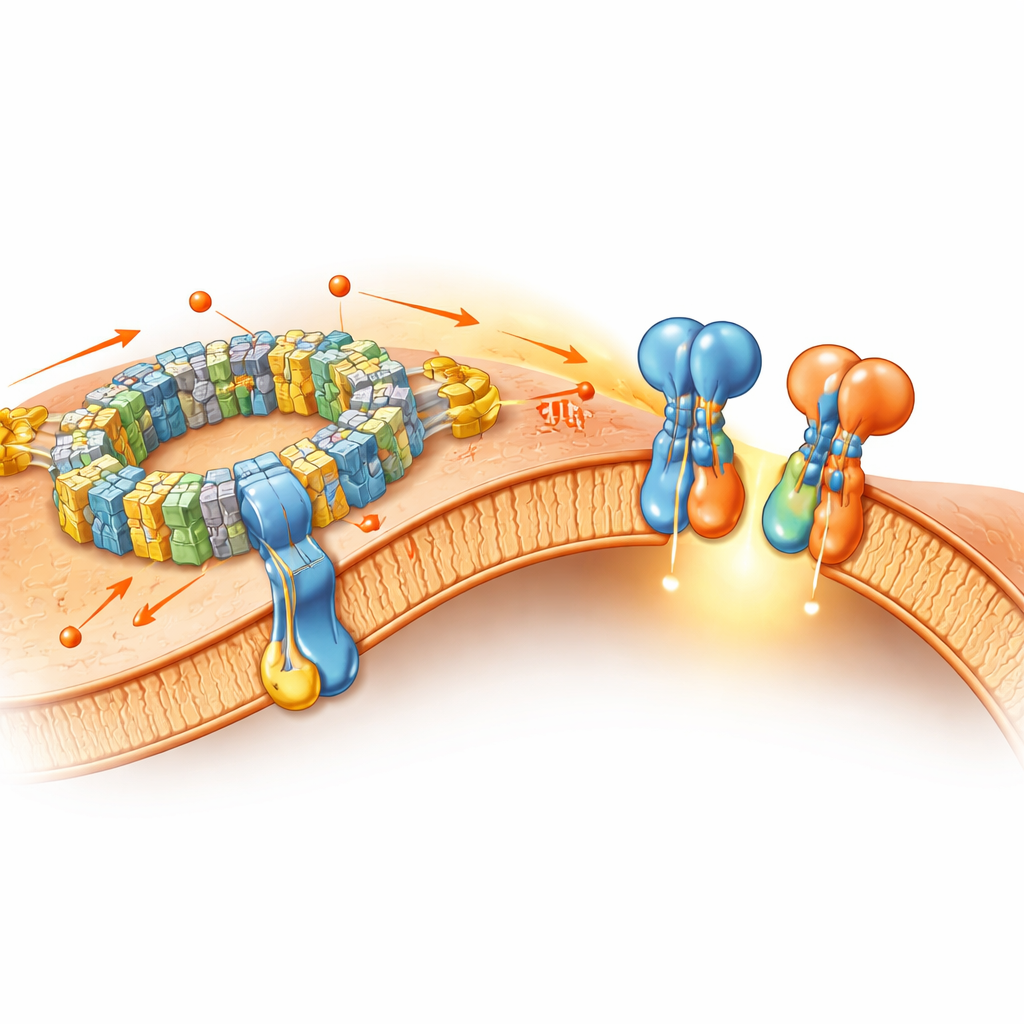
Energie‑Maschinen schließen sich zusammen
Über die ATP‑Synthase hinaus untersucht das Paper, wie sich die Komplexe der Atmungskette – nummeriert I, III und IV – zu „Superkomplexen“ zusammenschließen. In ihren nativen Membranproben finden die Forschenden nicht nur die zuvor bekannten Kombinationen (etwa ein Komplex I mit einem Dimer von Komplex III und einer oder zwei Kopien von Komplex IV), sondern auch eine neue Form mit drei Kopien von Komplex IV, die an die Kerneinheit gebunden sind, und sogar einen riesigen „Megakomplex“, das zwei Komplex‑I‑Einheiten, ein Dimer von Komplex III und sechs Kopien von Komplex IV enthält. Diese höhergeordneten Assemblierungen krümmen die Membran leicht und optimieren vermutlich den Fluss von Elektronen und Protonen, wodurch die Energieumwandlung effizienter wird. Zugleich behalten die einzelnen Komplexe im Wesentlichen dieselben Feinstrukturen wie in traditionellen, gereinigten Proben bei, was darauf hindeutet, dass viele ihrer Kernmerkmale die detergenbasierte Aufbereitung überdauern.
Folgen für Gesundheit und Krankheit
Indem sie die natürliche Umgebung dieser Proteinkomplexe bewahren, liefert diese Arbeit eine treuere Momentaufnahme davon, wie die mitochondriale „Hardware“ in lebenden Zellen organisiert ist. Die Autorinnen und Autoren zeigen, dass ATP‑Synthase‑Tetramere echte Merkmale von Säugetiermitochondrien sind und dass sie helfen, die scharfen Rillen zu formen, in denen ATP‑Produktion konzentriert stattfindet. Sie zeigen außerdem eine vielfältigere Palette respiratorischer Superkomplexe und Megakomplexe als zuvor erkannt. Da Mutationen in diesen Komplexen und Veränderungen in ihrer Assemblierung mit Stoffwechselstörungen, mitochondrialen Erkrankungen und sogar frühen Schritten des Zelltods verbunden sind, bietet diese strukturelle Karte eine solide Grundlage für künftige Studien. Vereinfacht gesagt erklärt das Paper, wie das Layout und das Zusammenspiel der kleinsten Turbinen und Leitungen der Zelle unsere Energieversorgung am Laufen halten – und wie feine Fehlverdrahtung zur menschlichen Krankheit beitragen kann.
Zitation: Nakano, A., Masuya, T., Akisada, S. et al. Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane. Nat Commun 17, 4075 (2026). https://doi.org/10.1038/s41467-026-70578-x
Schlüsselwörter: Mitochondrien, ATP‑Synthase, respiratorische Superkomplexe, Cryo‑Elektronenmikroskopie, mitochondriale Erkrankungen