Clear Sky Science · pl
Struktury nadkompleksów oddechowych i oligomerów syntazy ATP w wewnętrznej błonie mitochondriów ssaków
Elektrownie wewnątrz naszych komórek
Co sekundę biliony maleńkich maszyn w twoich komórkach wytwarzają energię, która utrzymuje cię przy życiu. W tym artykule autorzy przyglądają się wyjątkowo z bliska niektórym z najważniejszych z tych maszyn w mitochondriach, zwanych „elektrowniami” komórki. Przy użyciu zaawansowanej mikroskopii elektronowej ukazują, jak białkowe komplexy produkujące energię osadzone są w naturalnym środowisku błonowym, jak łączą się w większe zespoły oraz jak ich kształty wpływają na wewnętrzną architekturę mitochondriów. Te szczegóły mają znaczenie, ponieważ subtelne usterki w tych strukturach wiążą się z zaburzeniami metabolicznymi i chorobami mitochondrialnymi.
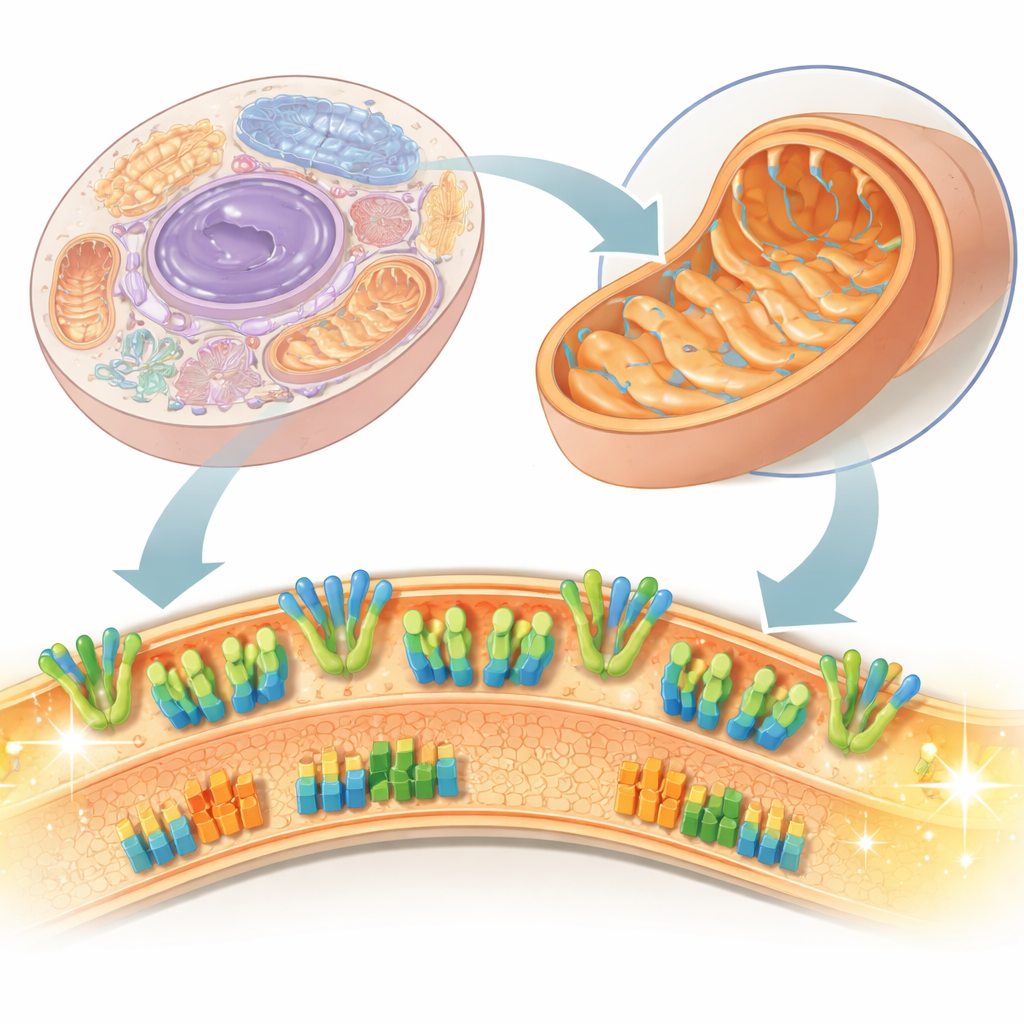
Wewnętrzny krajobraz elektrowni
Mitochondria mają dwie błony, a to właśnie wewnętrzna błona jest miejscem, gdzie odbywa się rzeczywista produkcja energii. Mieszczą się na niej dwa główne zestawy maszyn białkowych: łańcuch oddechowy, który przemieszcza elektrony i pompuje protony, tworząc różnicę potencjałów przez błonę, oraz syntaza ATP, która wykorzystuje tę różnicę potencjałów do wytwarzania ATP — „waluty energetycznej” komórki. Tradycyjnie naukowcy badali te białka po ich ekstrakcji detergentami, co grozi zaburzeniem delikatnych oddziaływań i lipidów. W tej pracy badacze używają podmitochondrialnych pęcherzyków — małych pęcherzy odczepionych od mitochondriów bydlecego serca — i obrazują je bezpośrednio w zamrożonym, natywnie przypominającym stanie za pomocą krioelektronowej mikroskopii. To podejście pozwala zobaczyć nie tylko pojedyncze białka, lecz także to, jak są one rozmieszczone i współdziałają w rzeczywistej błonie.
Formowanie grzbietów, które wytwarzają energię
Jedno z najbardziej uderzających odkryć dotyczy syntazy ATP, obrotowej enzymu wytwarzającego ATP. Wcześniejsze badania sugerowały, że dwie jednostki syntazy ATP mogą parować, tworząc kształt litery V, oraz że większe grupy mogą wyginać wewnętrzną błonę w ciasne grzbiety zwane krystami, lecz nie było jasne, czy większe zespoły są naturalne, czy też artefaktami procesu ekstrakcji. Tutaj autorzy wyraźnie obserwują dymery syntazy ATP połączone małym białkiem regulatorowym, tworzące pary osadzone w błonie. Co ważniejsze, widzą linowe tetramery — dwa dymery ustawione obok siebie — bezpośrednio w natywnej błonie. Te tetramery leżą w miejscach o silnym zakrzywieniu i wspólnie zaginają błonę w profil przypominający literę U, co wspiera hipotezę, że zespoły syntazy ATP aktywnie kształtują wierzchołki kryst w mitochondriach ssaków.
Szczegóły obrotowej maszyny
Badanie przygląda się również części transbłonowej syntazy ATP, odkrywając detale, które kwestionują wcześniejsze interpretacje. Pierścień podjednostek białkowych (pierścień c8) obraca się w obrębie błony, a wcześniejsze struktury otrzymane po użyciu detergentów pokazywały dodatkową gęstość wewnątrz tego pierścienia, uznawaną za ściśle związane lipidy oddziałujące z inną podjednostką (nazwaną e). W natywnej błonie autorzy stwierdzają jednak, że ta wewnętrzna gęstość jest bardzo słaba lub nieobecna, co sugeruje, że to, co wcześniej widziano, mogły być cząsteczki detergentu, a nie niezbędne lipidy. Zamiast tego ich mapy sugerują, że koniec podjednostki e, być może z małą modyfikacją chemiczną, oddziałuje bezpośrednio z pierścieniem. Ta subtelna zmiana przestawia wyobrażenie naukowców o mechanicznej więzi pozwalającej, by napięcie błony napędzało produkcję ATP.
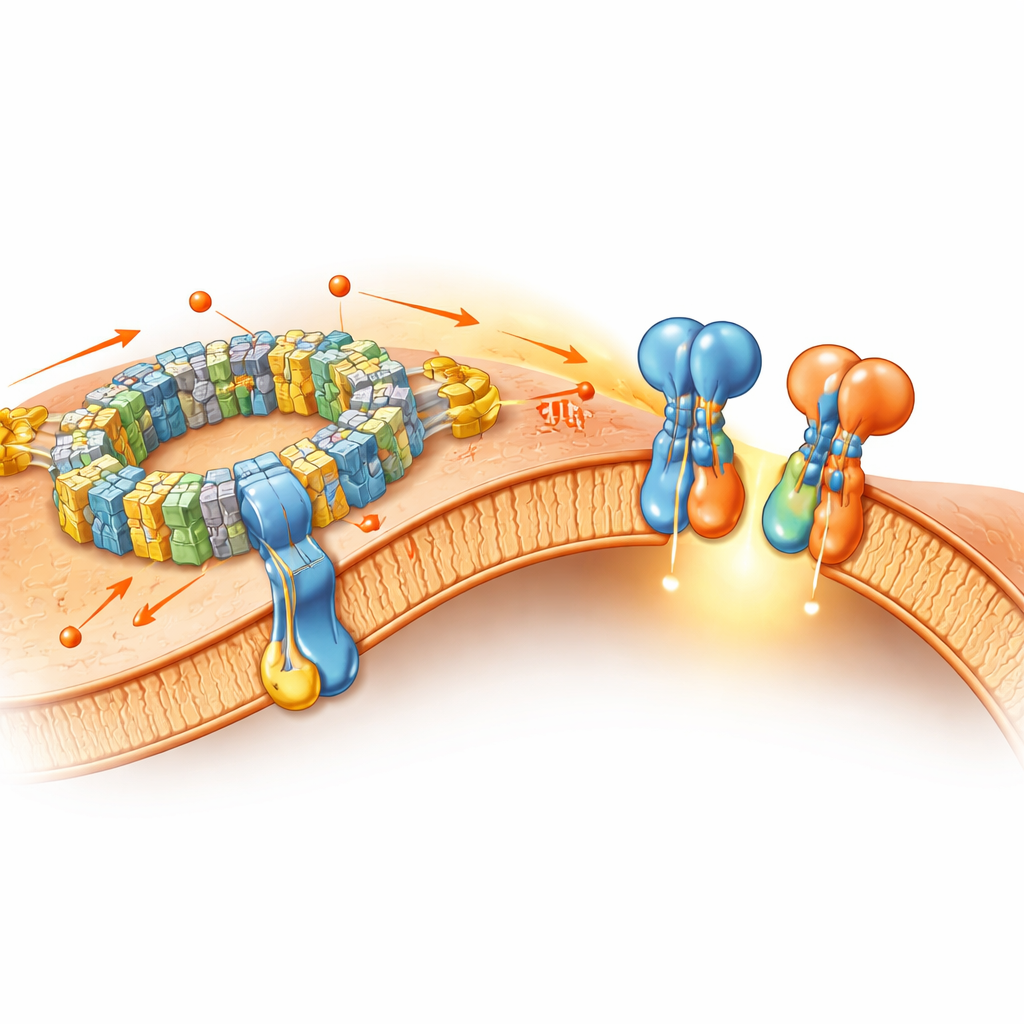
Maszyny energetyczne łączą siły
Poza syntazą ATP artykuł bada, jak komplexy łańcucha oddechowego — oznaczone jako I, III i IV — skupiają się w „nadkompleksy”. W próbkach natywnej błony autorzy znajdują nie tylko wcześniej znane kombinacje (takie jak jeden kompleks I z dimerem kompleksu III i jedną lub dwiema kopii kompleksu IV), lecz także nową formę zawierającą trzy kopie kompleksu IV przyłączone do jednostki rdzeniowej, a nawet olbrzymi „megakompleks” obejmujący dwa kompleksy I, dimer kompleksu III i sześć kopii kompleksu IV. Te wyższe porządkowo zespoły nieznacznie zakrzywiają błonę i prawdopodobnie optymalizują przepływ elektronów i protonów, zwiększając efektywność konwersji energii. Jednocześnie poszczególne kompleksy w dużej mierze zachowują te same drobne struktury obserwowane w tradycyjnych oczyszczonych próbkach, co wskazuje, że wiele ich podstawowych cech przetrwa przygotowanie z użyciem detergentów.
Implikacje dla zdrowia i chorób
Zachowując naturalne otoczenie tych maszyn białkowych, praca ta dostarcza wierniejszego obrazu tego, jak „sprzęt” mitochondrialny jest zorganizowany w żywych komórkach. Autorzy pokazują, że tetramery syntazy ATP są rzeczywistymi elementami mitochondriów ssaków i że pomagają formować ostre grzebienie, gdzie skoncentrowana jest produkcja ATP. Ujawniają również bogatszą gamę nadkompleksów oddechowych i megakompleksów, niż dotąd sądzono. Ponieważ mutacje w tych kompleksach i zmiany w ich składaniu wiążą się z zaburzeniami metabolicznymi, chorobami mitochondrialnymi, a także wczesnymi etapami śmierci komórkowej, ta mapa strukturalna stanowi solidną podstawę do przyszłych badań. Mówiąc prosto: artykuł wyjaśnia, jak rozmieszczenie i współpraca najdrobniejszych turbin i przewodów komórki pomagają utrzymać płynność dostaw energii — i jak subtelne błędy połączeń mogą przyczyniać się do chorób człowieka.
Cytowanie: Nakano, A., Masuya, T., Akisada, S. et al. Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane. Nat Commun 17, 4075 (2026). https://doi.org/10.1038/s41467-026-70578-x
Słowa kluczowe: mitochondria, syntaza ATP, nadkompleksy oddechowe, mikroskopia krioelektronowa, choroby mitochondrialne