Clear Sky Science · fr
Structures des supercomplexes de la respiration et des oligomères d’ATP synthase dans la membrane interne mitochondriale des mammifères
Centrales électriques à l’intérieur de nos cellules
Chaque seconde, des milliards de petites machines dans vos cellules produisent l’énergie qui vous maintient en vie. Cet article examine de très près certaines des plus importantes de ces machines situées dans les mitochondries, les « centrales » de la cellule. Grâce à une microscopie électronique de pointe, les auteurs révèlent comment les complexes protéiques producteurs d’énergie se disposent dans leur environnement membranaire naturel, comment ils s’associent en assemblages plus grands, et comment leurs formes contribuent à modeler l’architecture interne même des mitochondries. Ces détails sont importants car des anomalies subtiles de ces structures sont liées à des troubles métaboliques et à des maladies mitochondriales.
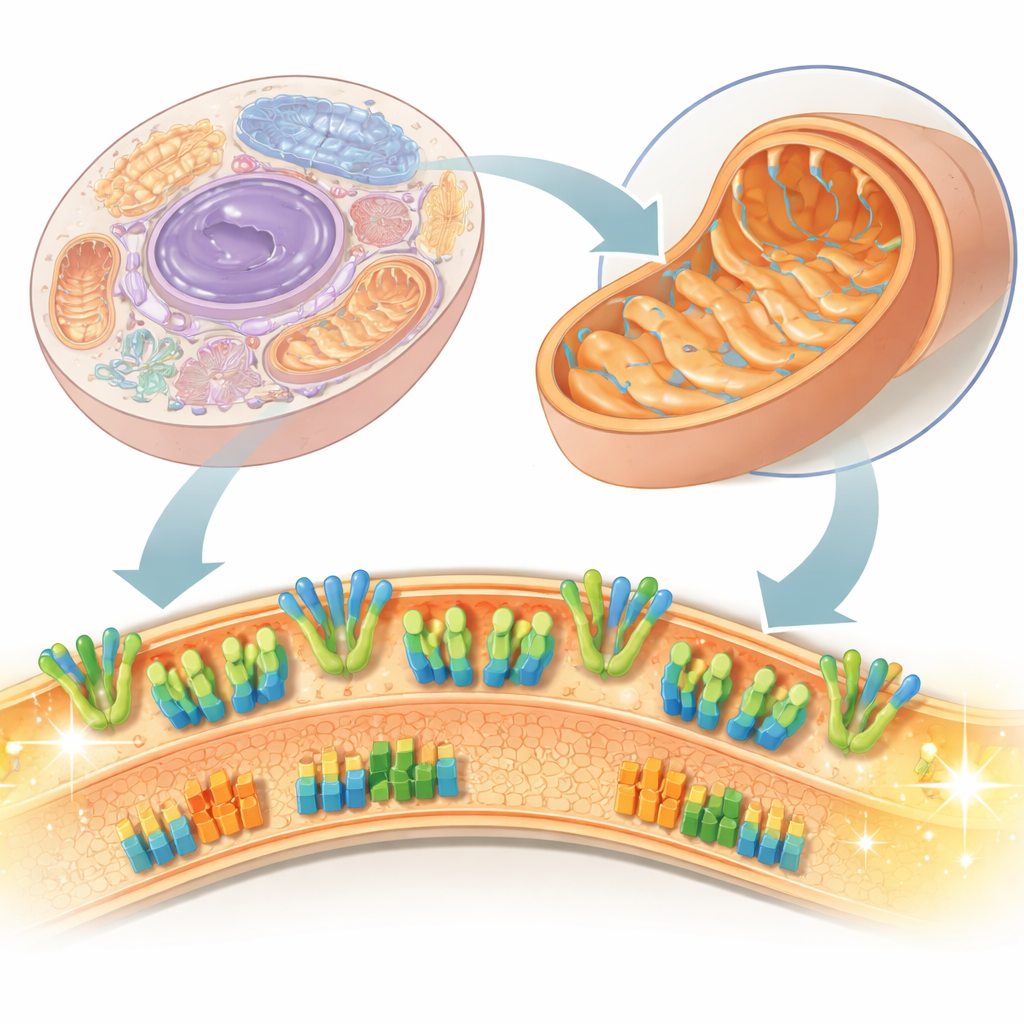
Le paysage intérieur d’une centrale
Les mitochondries possèdent deux membranes, et c’est la membrane interne qui concentre l’essentiel de l’activité énergétique. Elle héberge deux grands ensembles de machines protéiques : la chaîne respiratoire, qui transporte des électrons et pompe des protons pour créer une différence de potentiel à travers la membrane, et l’ATP synthase, qui utilise ce potentiel pour fabriquer l’ATP, la « monnaie énergétique » de la cellule. Traditionnellement, les scientifiques ont étudié ces protéines après les avoir extraites avec des détergents, ce qui risque de perturber des liaisons fragiles et des lipides. Dans ce travail, les chercheurs utilisent des particules sous‑mitochondriales — de petites vésicules prélevées sur des mitochondries de cœur bovin — et les imagent directement dans un état vitrifié et proche du natif par cryo‑microscopie électronique. Cette approche leur permet de voir non seulement des protéines isolées, mais aussi comment ces protéines sont agencées et coopèrent dans la membrane réelle.
Façonner les crêtes productrices d’énergie
Une des découvertes les plus marquantes concerne l’ATP synthase, l’enzyme rotative qui fabrique l’ATP. Des études antérieures suggéraient que deux unités d’ATP synthase peuvent s’apparier pour former un V, et que des groupes plus importants pourraient plier la membrane interne en des crêtes serrées appelées cristae, mais il n’était pas clair si ces assemblages supérieurs étaient naturels ou des artefacts de l’extraction. Ici, les auteurs observent clairement des dimères d’ATP synthase joints par une petite protéine régulatrice, formant des paires intégrées dans la membrane. Plus important encore, ils voient des tétramères linéaires — deux dimères disposés côte à côte — directement dans la membrane native. Ces tétramères se trouvent dans des régions fortement courbées et courbent collectivement la membrane en un profil en U, soutenant l’idée que les assemblages d’ATP synthase sculptent activement les pointes des cristae chez les mammifères.
Détails fins de la machine rotative
L’étude examine aussi de près la portion transmembranaire de l’ATP synthase, dévoilant des détails qui remettent en question des interprétations antérieures. Un anneau de sous‑unités protéiques (l’anneau c8) tourne dans la membrane, et des structures obtenues précédemment après extraction montraient une densité supplémentaire à l’intérieur de cet anneau, attribuée à des lipides fortement liés interagissant avec une autre sous‑unité (appelée e). Dans la membrane native, cependant, les auteurs constatent que cette densité interne est très faible ou absente, ce qui suggère que ce qui avait été vu auparavant pouvait être des molécules de détergent et non des lipides essentiels. À la place, leurs cartes laissent entendre que l’extrémité de la sous‑unité e, éventuellement porteuse d’une petite modification chimique, interagit directement avec l’anneau. Ce réarrangement subtil modifie la manière dont les scientifiques conçoivent la liaison mécanique qui permet au potentiel membranaire de piloter la production d’ATP.
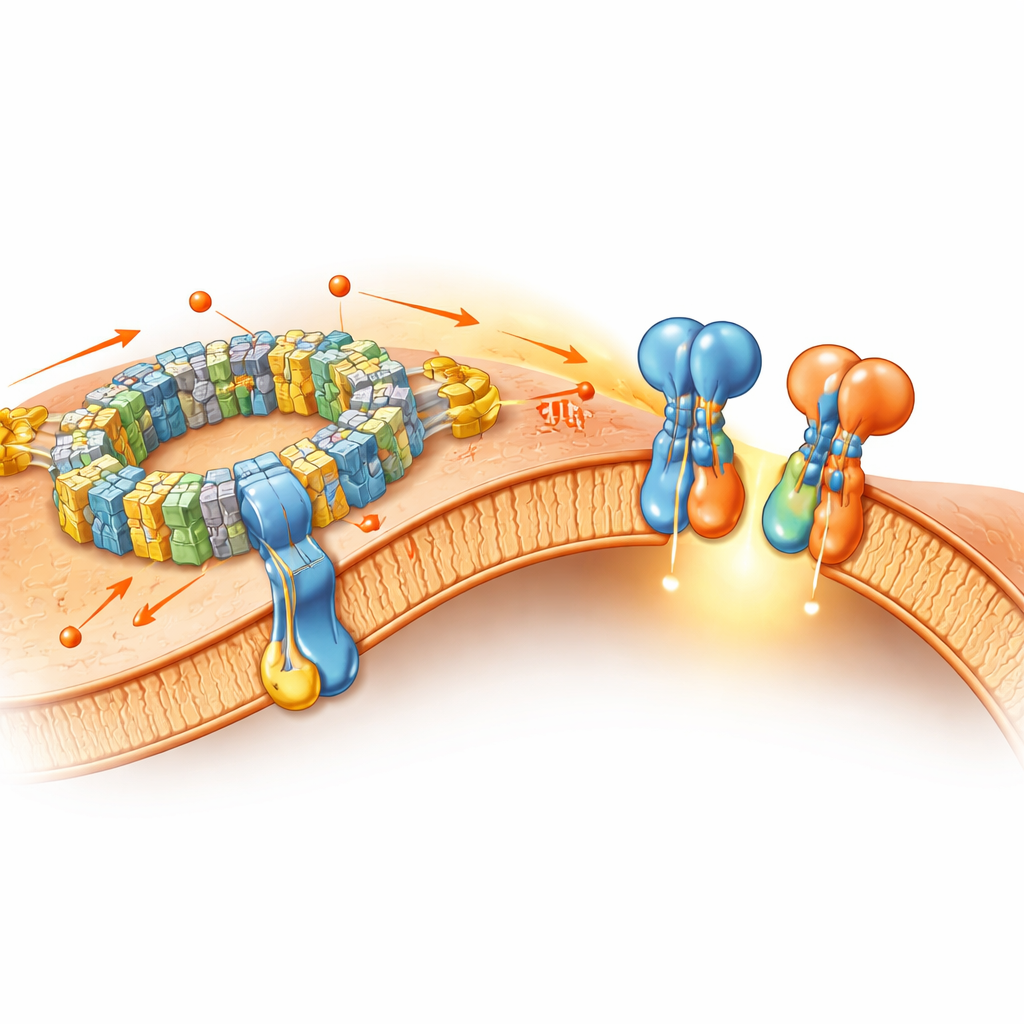
Les machines énergétiques s’associent
Au‑delà de l’ATP synthase, l’article explore comment les complexes de la chaîne respiratoire — numérotés I, III et IV — se regroupent en « supercomplexes ». Dans leurs échantillons de membrane native, les auteurs trouvent non seulement les combinaisons déjà connues (comme un complexe I avec un dimère du complexe III et une ou deux copies du complexe IV), mais aussi une forme nouvelle contenant trois copies du complexe IV attachées à l’unité centrale, et même un « mégacomplexe » géant qui regroupe deux complexes I, un dimère du complexe III et six copies du complexe IV. Ces assemblages d’ordre supérieur courbent légèrement la membrane et optimisent vraisemblablement le flux d’électrons et de protons, rendant la conversion d’énergie plus efficace. Parallèlement, les complexes individuels conservent en grande partie les mêmes structures fines observées dans les échantillons purifiés traditionnels, ce qui indique que nombre de leurs caractéristiques de base survivent à la préparation avec détergent.
Implications pour la santé et la maladie
En préservant le contexte naturel de ces machines protéiques, ce travail fournit un instantané plus fidèle de l’organisation du « matériel » mitochondrial dans les cellules vivantes. Les auteurs montrent que les tétramères d’ATP synthase sont des éléments authentiques des mitochondries de mammifères et qu’ils contribuent à façonner les crêtes aiguës où la production d’ATP est concentrée. Ils révèlent aussi une plus grande diversité de supercomplexes respiratoires et de mégacomplexes que précédemment reconnue. Parce que des mutations dans ces complexes et des altérations de leur assemblage sont liées à des troubles métaboliques, à des maladies mitochondriales et même aux premiers stades de la mort cellulaire, cette cartographie structurale offre une base solide pour des études futures. En termes simples, l’article explique comment l’agencement et la coopération des plus petites turbines et circuits cellulaires aident à maintenir notre approvisionnement énergétique — et comment un mauvais assemblage subtil pourrait contribuer à des maladies humaines.
Citation: Nakano, A., Masuya, T., Akisada, S. et al. Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane. Nat Commun 17, 4075 (2026). https://doi.org/10.1038/s41467-026-70578-x
Mots-clés: mitochondries, ATP synthase, supercomplexes respiratoires, cryomicroscopie électronique, maladies mitochondriales