Clear Sky Science · zh
支链α-酮酸通过重新激活LDHA-乳酸轴,在糖尿病状态下损害胰腺β细胞的葡萄糖刺激性胰岛素分泌
这一发现为何与日常健康相关
2型糖尿病通常被描述为机体对胰岛素不敏感的问题,但这项研究表明,产生胰岛素的细胞本身也可能被我们饮食的某些代谢物毒害。研究人员揭示了常见氨基酸的特定分解产物如何悄然破坏胰岛素释放,这有助于解释为何部分糖尿病患者难以控制血糖,并指向保护胰腺的新途径。
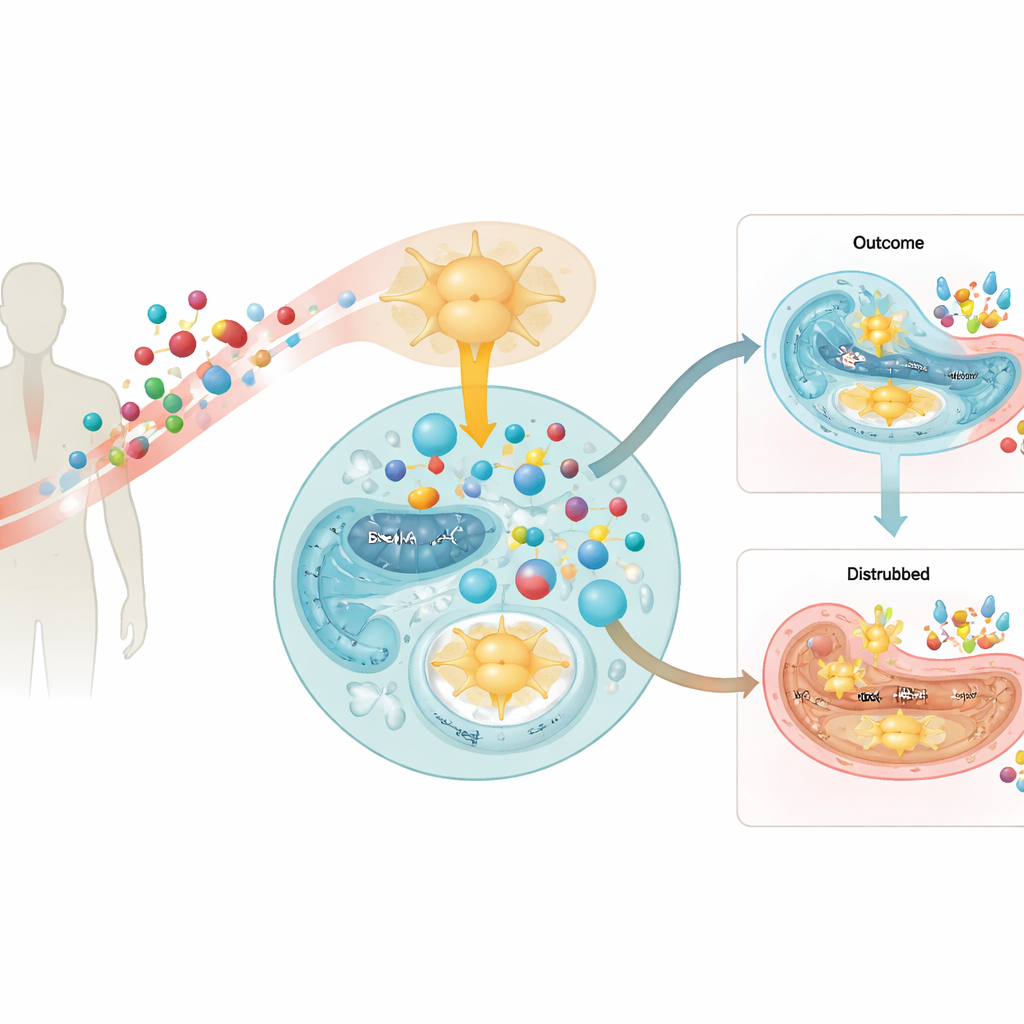
有“暗面”的膳食构建模块
这项工作聚焦于支链氨基酸——存在于高蛋白食物和流行运动补剂中的营养物质。体内分解这些氨基酸会产生称为支链α-酮酸的化合物。在健康情况下,这些酮酸会在线粒体中进一步被氧化,以助力能量生成。然而在患有糖尿病的人和小鼠中,作者发现用于清除这些酮酸的代谢装置在胰腺的胰岛β细胞内减弱。因此,这些酮酸在β细胞所在的胰岛内积累。
来自患者和动物模型的线索
通过分析糖尿病患者与社区志愿者的血样,团队发现循环中这些酮酸水平较高与β细胞功能较差相关,即使在调整了胰岛素抵抗等因素后,这一关联仍然存在。在糖尿病小鼠和人类供体胰岛中,通常负责清除酮酸的关键酶呈现水平降低或被化学修饰而关闭,且β细胞内含有更多的酮酸。当健康小鼠饮水中添加这些分子时,它们逐渐变得难以应对糖负荷——并非因为肌肉或肝脏对胰岛素不敏感,而是因为β细胞在血糖升高时不再释放足够的胰岛素。
β细胞内能量通路如何被改写
在正常情况下,进入β细胞的葡萄糖被分解为丙酮酸,随后被输送入线粒体并进入三羧酸循环以生成ATP,这一能量信号触发快速的胰岛素释放。使用同位素标记的葡萄糖和高精度代谢测量,研究人员发现过量的酮酸会将丙酮酸从该能量循环中分流。丙酮酸不再进入线粒体,而是更多地被转化为乳酸——在β细胞中属于一个“死胡同”产物。此转变降低了ATP生成并削弱了血糖升高时的关键首发胰岛素高潮,同时对细胞生存和一般葡萄糖摄取等其他方面影响较小。
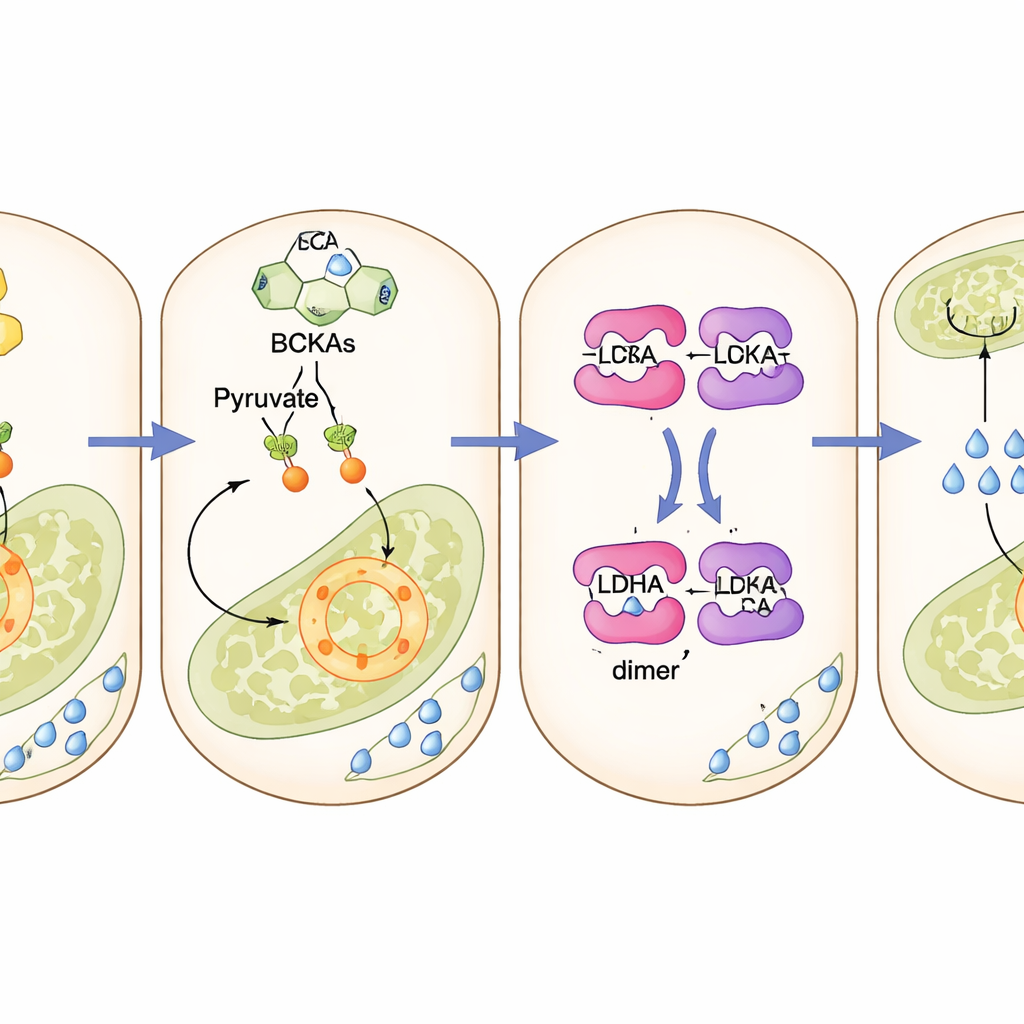
被重新激活的休眠酶
这一分流的核心是一种名为乳酸脱氢酶A(LDHA)的酶,该酶在β细胞中通常保持沉默,以便将葡萄糖导向能量生成而非乳酸产生。研究显示,积累的酮酸可以物理结合该酶,像微小的桥梁一样将其亚基拉拢成更具活性的构象。一旦被激活,酶就会将丙酮酸拉向乳酸生成,使线粒体燃料匮乏。在β细胞中通过基因手段阻断该酶或使用小分子抑制剂,能够保护细胞和小鼠免受酮酸的有害影响并恢复正常的胰岛素分泌。促使酮酸回到其正常分解途径的药物也具有类似的挽救效果。
这对糖尿病治疗意味着什么
对非专业读者而言,关键信息是:在糖尿病中,问题不仅在于机体对胰岛素的反应,还与胰岛素产生细胞如何处理某些饮食代谢物有关。当支链氨基酸的分解受扰动时,其酮酸代谢物会积累、激活本来沉默的酶,并将糖的流向从能量生成改写,削弱胰腺对葡萄糖的反应能力。这提示监测血中这些酮酸可能有助于发现β细胞功能衰竭,并且通过谨慎调整支链氨基酸摄入或设计旨在恢复其正常代谢的药物,可能为在2型糖尿病中保护或恢复胰岛素分泌开辟新途径。
引用: Lin, H., Ho, M.Y.M., Wang, B. et al. Branched-chain α-keto acids impair glucose-stimulated insulin secretion in pancreatic β-cells under diabetes by reactivating the LDHA-lactate axis. Nat Commun 17, 3346 (2026). https://doi.org/10.1038/s41467-026-70004-2
关键词: 2型糖尿病, 胰岛素分泌, 支链氨基酸, 胰腺β细胞, 乳酸代谢