Clear Sky Science · de
Verzweigtkettige α-Ketosäuren beeinträchtigen die glukosegetriebene Insulinsekretion in pankreatischen β‑Zellen bei Diabetes durch Reaktivierung der LDHA‑Laktat‑Achse
Warum diese Entdeckung für die alltägliche Gesundheit wichtig ist
Typ‑2‑Diabetes wird oft als Problem der verminderten Insulinempfindlichkeit beschrieben, doch diese Studie zeigt, dass auch die Zellen, die Insulin produzieren, durch bestimmte Stoffwechselprodukte unserer Ernährung geschädigt werden können. Die Forschenden legen dar, wie spezifische Abbauprodukte häufiger Aminosäuren still und heimlich die Insulinfreisetzung sabotieren können. Das hilft zu erklären, warum einige Menschen mit Diabetes Schwierigkeiten haben, ihren Blutzucker zu kontrollieren, und weist auf neue Wege hin, die Bauchspeicheldrüse zu schützen.
Bausteine der Nahrung mit einer verborgenen Schattenseite
Die Arbeit konzentriert sich auf verzweigtkettige Aminosäuren, Nährstoffe, die in proteinreichen Lebensmitteln und populären Sportergänzungen vorkommen. Beim Abbau dieser Aminosäuren entstehen Verbindungen, die als verzweigtkettige alpha‑Ketosäuren bezeichnet werden. Unter gesunden Bedingungen werden diese Ketosäuren in den Mitochondrien, den Kraftwerken der Zelle, weiter verbrannt und tragen so zur Energiegewinnung bei. Bei Menschen und Mäusen mit Diabetes jedoch stellten die Autorinnen und Autoren fest, dass die Maschinerie, die diese Ketosäuren entsorgt, in den insulinproduzierenden Zellen der Bauchspeicheldrüse verlangsamt ist. Infolgedessen reichern sich die Ketosäuren in den Inseln an, in denen die Beta‑Zellen leben.
Hinweise aus Patienten und Tiermodellen
Durch die Analyse von Blutproben von Menschen mit Diabetes und von Gemeindefreiwilligen zeigte das Team, dass höhere zirkulierende Spiegel dieser Ketosäuren mit einer schlechteren Beta‑Zell‑Funktion verbunden waren, selbst nach Berücksichtigung der Insulinresistenz. In diabetischen Mäusen und in humanen Spender‑Islets waren Schlüsselenzyme, die die Ketosäuren normalerweise entfernen, in geringeren Mengen vorhanden oder durch chemische Markierungen abgeschaltet, und die Beta‑Zellen selbst enthielten mehr dieser Ketosäuren. Wenn gesunden Mäusen über Trinkwasser diese Moleküle verabreicht wurden, verschlechterte sich ihre Fähigkeit, eine Zuckerlösung zu verarbeiten — nicht weil Muskeln oder Leber Insulin ignorierten, sondern weil die Beta‑Zellen bei steigendem Glukosespiegel nicht mehr ausreichend Insulin freisetzten.
Wie die Energiepipeline in Beta‑Zellen umgebaut wird
Unter normalen Umständen wird Glukose, die in eine Beta‑Zelle eintritt, zu Pyruvat abgebaut, das dann in die Mitochondrien geschleust und in den Tricarbonsäurezyklus eingespeist wird, um ATP zu erzeugen — das Energiesignal, das die rasche Insulinfreisetzung auslöst. Mit isotopenmarkierter Glukose und hochpräzisen Stoffwechselmessungen fanden die Forschenden heraus, dass überschüssige Ketosäuren Pyruvat von diesem Energiezyklus weglenken. Statt in die Mitochondrien zu gelangen, wird mehr Pyruvat in Laktat umgewandelt, ein für Beta‑Zellen „Sackgassenprodukt“. Diese Verschiebung senkte die ATP‑Produktion und dämpfte den wichtigen ersten Insulinschub, der normalerweise auf einen Blutzuckeranstieg folgt, während andere Aspekte der Zellgesundheit, wie Überleben und allgemeine Glukoseaufnahme, weitgehend erhalten blieben.
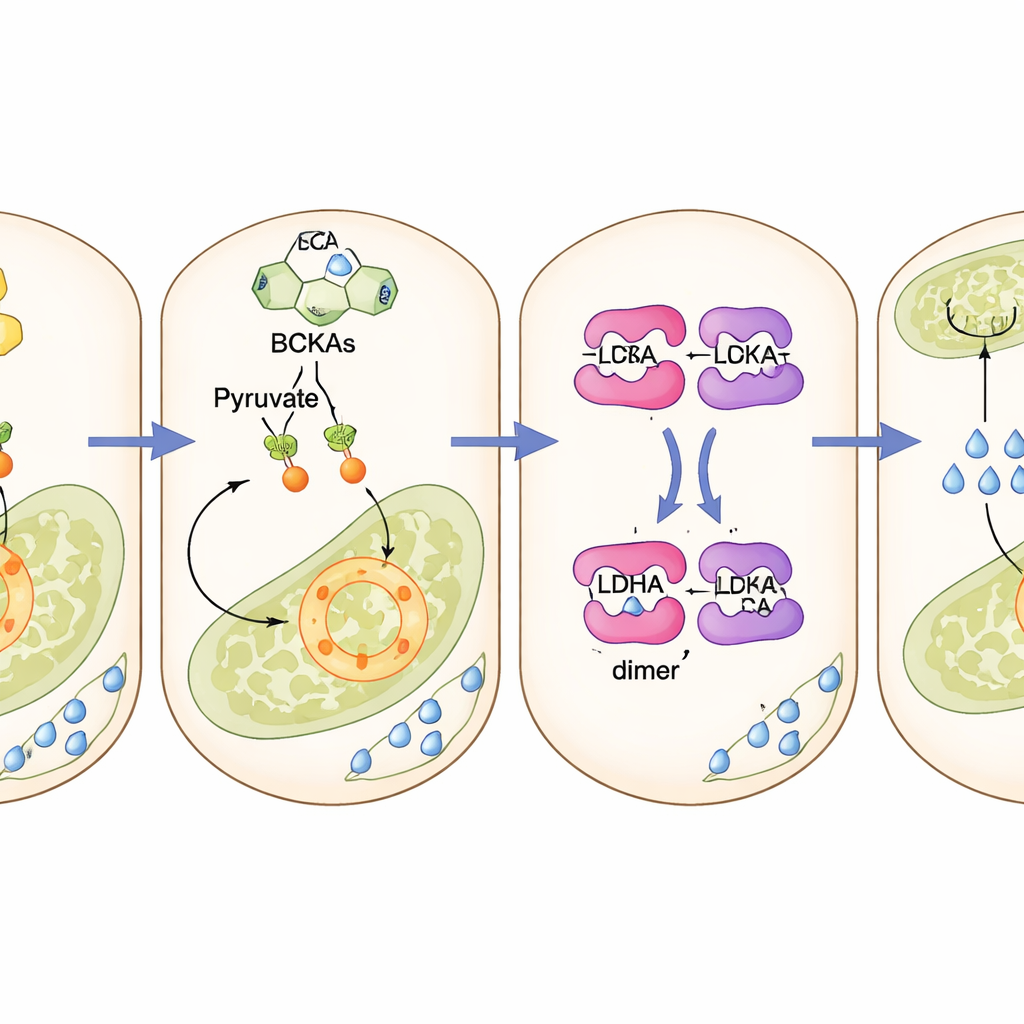
Ein ruhendes Enzym wird wieder aktiviert
Im Zentrum dieser Umlenkung steht ein Enzym namens Laktatdehydrogenase A, das in Beta‑Zellen normalerweise stillgesetzt ist, damit Glukose in die Energieproduktion und nicht in Laktat geleitet wird. Die Studie zeigt, dass sich die akkumulierten Ketosäuren physikalisch an dieses Enzym binden und wie winzige Brücken wirken, die seine Untereinheiten zu einer aktiveren Form zusammenziehen. Einmal aktiviert, zieht das Enzym Pyruvat in Richtung Laktat und beraubt so die Mitochondrien des Brennstoffs. Die genetische Blockade des Enzyms in Beta‑Zellen oder der Einsatz eines niedermolekularen Inhibitors schützte Zellen und Mäuse vor den schädlichen Effekten der Ketosäuren und stellte die normale Insulinfreisetzung wieder her. Medikamente, die die Ketosäuren wieder in ihren üblichen Abbauweg lenken, zeigten einen ähnlichen Rettungseffekt.
Was das für die Behandlung von Diabetes bedeutet
Für Nicht‑Spezialisten lautet die zentrale Botschaft: Bei Diabetes geht es nicht nur darum, wie der Körper auf Insulin reagiert, sondern auch darum, wie die Insulin produzierenden Zellen mit bestimmten ernährungsbedingten Nebenprodukten umgehen. Wenn der Abbau verzweigtkettiger Aminosäuren gestört ist, reichern sich deren Keto‑Säure‑Nachkommen an, schalten ein normalerweise stummes Enzym an und leiten Zucker weg von der Energieproduktion — wodurch die Fähigkeit der Bauchspeicheldrüse, auf Glukose zu reagieren, geschwächt wird. Das legt nahe, dass die Überwachung dieser Ketosäuren im Blut helfen könnte, versagende Beta‑Zellen zu identifizieren, und dass eine gezielte Anpassung der Aufnahme verzweigtkettiger Aminosäuren oder die Entwicklung von Medikamenten zur Wiederherstellung ihres ordnungsgemäßen Abbaus neue Wege eröffnen könnte, die Insulinsekretion bei Typ‑2‑Diabetes zu erhalten oder wiederherzustellen.
Zitation: Lin, H., Ho, M.Y.M., Wang, B. et al. Branched-chain α-keto acids impair glucose-stimulated insulin secretion in pancreatic β-cells under diabetes by reactivating the LDHA-lactate axis. Nat Commun 17, 3346 (2026). https://doi.org/10.1038/s41467-026-70004-2
Schlüsselwörter: Typ‑2‑Diabetes, Insulinsekretion, verzweigtkettige Aminosäuren, Pankreas‑Beta‑Zellen, Laktatstoffwechsel