Clear Sky Science · pl
Kwas alfa-ketonowy o rozgałęzionym łańcuchu upośledza wydzielanie insuliny stymulowane glukozą w komórkach β trzustki w cukrzycy przez reaktywację osi LDHA–mleczan
Dlaczego to odkrycie ma znaczenie dla codziennego zdrowia
Cukrzycę typu 2 często opisuje się jako problem oporności tkanek na insulinę, ale to badanie pokazuje, że same komórki produkujące insulinę mogą zostać „zatrute” przez pewne produkty uboczne naszej diety. Naukowcy odkrywają, jak konkretne metabolity powszechnych aminokwasów mogą po cichu sabotować uwalnianie insuliny, co pomaga wyjaśnić, dlaczego niektórzy chorzy mają trudności z utrzymaniem poziomu cukru we krwi, i wskazuje nowe drogi ochrony trzustki.
Składniki diety z ukrytą mroczną stroną
Praca koncentruje się na aminokwasach o rozgałęzionych łańcuchach, obecnych w pokarmach bogatych w białko i popularnych suplementach sportowych. Gdy organizm rozkłada te aminokwasy, powstają związki zwane rozgałęzionymi alfa-ketonami. W warunkach prawidłowych te keto-kwasy są dalej utleniane w mitochondriach, „elektrowniach” komórki, wspierając wytwarzanie energii. U osób i myszy z cukrzycą badacze stwierdzili jednak, że mechanizmy usuwania tych keto-kwasów są spowolnione w komórkach produkujących insulinę w trzustce. W efekcie keto-kwasy gromadzą się w wyspach trzustkowych, gdzie żyją komórki beta.
Wskazówki od pacjentów i modeli zwierzęcych
Analizując próbki krwi od osób z cukrzycą oraz od ochotników z populacji, zespół wykazał, że wyższe krążące stężenia tych keto-kwasów wiązały się z gorszą funkcją komórek beta, nawet po uwzględnieniu oporności na insulinę. U chorych myszy i w wyspach pobranych od ludzkich dawców kluczowe enzymy normalnie oczyszczające keto-kwasy występowały w niższych ilościach lub były wyłączone przez chemiczne znaczniki, a same komórki beta zawierały więcej tych keto-kwasów. Gdy zdrowym myszom podawano wodę do picia wzbogaconą tymi związkami, stopniowo traciły one zdolność do właściwego radzenia sobie z obciążeniem cukrem — nie dlatego, że mięśnie czy wątroba ignorowały insulinę, lecz dlatego, że komórki beta przestały wydzielać jej wystarczająco dużo po wzroście glukozy.
Jak przebudowywany jest szlak energetyczny w komórkach beta
W normalnych warunkach glukoza wchodząca do komórki beta jest rozkładana do pirogronianu, który następnie trafia do mitochondriów i zasila cykl kwasów trikarboksylowych w celu produkcji ATP — sygnału energetycznego wywołującego szybkie wydzielanie insuliny. Korzystając z izotopowo znakowanej glukozy i precyzyjnych pomiarów metabolicznych, badacze odkryli, że nadmiar keto-kwasów odciąga pirogronian od tego cyklu energetycznego. Zamiast trafiać do mitochondriów, większa jego część jest przekształcana w mleczan, produkt „ślepego zaułka” w komórkach beta. Ten przesunięty tor obniżał produkcję ATP i tłumił kluczowy pierwszy wyrzut insuliny, który normalnie następuje po wzroście poziomu glukozy, pozostawiając inne aspekty zdrowia komórki, takie jak przeżycie czy ogólne pobieranie glukozy, w dużej mierze nienaruszone.
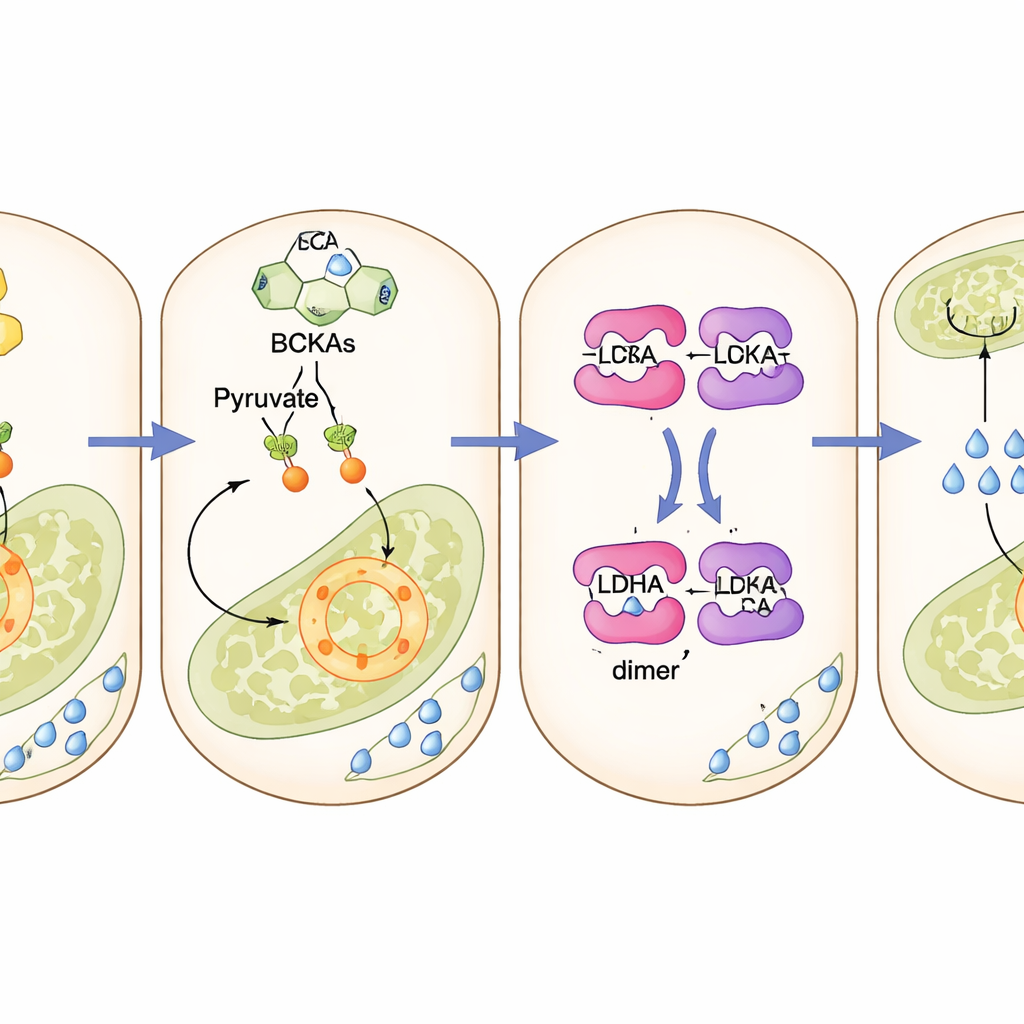
Uśpiony enzym znów aktywowany
W centrum tego przekierowania znajduje się enzym zwany dehydrogenazą mleczanową A (LDHA), który w komórkach beta zwykle jest utrzymywany w stanie uśpienia, aby glukoza była skierowana na produkcję energii zamiast w stronę mleczanu. Badanie pokazuje, że zgromadzone keto-kwasy wiążą się fizycznie z tym enzymem i działają jak małe mostki, które łączą jego podjednostki w bardziej aktywną formę. Gdy enzym zostaje aktywowany, ściąga pirogronian w kierunku produkcji mleczanu, pozbawiając mitochondria paliwa. Genetyczne zablokowanie enzymu w komórkach beta lub zastosowanie inhibitora małocząsteczkowego chroniło komórki i myszy przed szkodliwym działaniem keto-kwasów i przywracało prawidłowe wydzielanie insuliny. Leki kierujące keto-kwasy z powrotem na ich normalną ścieżkę rozpadu miały podobny efekt ratunkowy.
Co to oznacza dla leczenia cukrzycy
Dla odbiorcy niespecjalistycznego kluczowy przekaz jest taki, że w cukrzycy problem nie dotyczy wyłącznie reakcji tkanek na insulinę, lecz także sposobu, w jaki komórki produkujące insulinę radzą sobie z pewnymi produktami ubocznymi diety. Gdy rozkład aminokwasów o rozgałęzionych łańcuchach zostaje zaburzony, powstające keto-kwasy gromadzą się, włączają zwykle uśpiony enzym i przekierowują cukier z dala od produkcji energii, osłabiając zdolność trzustki do reagowania na glukozę. To sugeruje, że monitorowanie tych keto-kwasów we krwi mogłoby pomóc wykryć pogarszającą się funkcję komórek beta, a ostrożna modyfikacja spożycia aminokwasów rozgałęzionych lub opracowanie leków przywracających ich prawidłowy rozkład może otworzyć nowe drogi do zachowania lub odzyskania wydzielania insuliny w cukrzycy typu 2.
Cytowanie: Lin, H., Ho, M.Y.M., Wang, B. et al. Branched-chain α-keto acids impair glucose-stimulated insulin secretion in pancreatic β-cells under diabetes by reactivating the LDHA-lactate axis. Nat Commun 17, 3346 (2026). https://doi.org/10.1038/s41467-026-70004-2
Słowa kluczowe: cukrzyca typu 2, wydzielanie insuliny, aminokwasy o rozgałęzionych łańcuchach, komórki beta trzustki, metabolizm mleczanu