Clear Sky Science · fr
Les α-cétoacides à chaîne ramifiée altèrent la sécrétion d’insuline stimulée par le glucose dans les cellules β pancréatiques en situation de diabète en réactivant l’axe LDHA‑lactate
Pourquoi cette découverte compte pour la santé quotidienne
Le diabète de type 2 est souvent décrit comme un problème d’insensibilité de l’organisme à l’insuline, mais cette étude montre que les cellules qui produisent l’insuline peuvent elles‑mêmes être empoisonnées par certains sous‑produits de notre alimentation. Les chercheurs dévoilent comment des produits de dégradation spécifiques d’acides aminés courants peuvent, de manière insidieuse, saboter la libération d’insuline, ce qui aide à expliquer pourquoi certaines personnes atteintes de diabète peinent à garder leur glycémie sous contrôle et oriente vers de nouvelles pistes pour protéger le pancréas.
Des éléments de l’alimentation avec un côté sombre caché
Les travaux se concentrent sur les acides aminés à chaîne ramifiée, des nutriments présents dans les aliments riches en protéines et dans des compléments populaires pour sportifs. Lorsque l’organisme dégrade ces acides aminés, il produit des composés appelés α‑cétoacides à chaîne ramifiée. Dans des conditions saines, ces cétoacides sont ensuite oxydés dans les mitochondries, les centrales énergétiques de la cellule, pour contribuer à la production d’énergie. Chez les personnes et les souris diabétiques, toutefois, les auteurs ont constaté que la machinerie qui élimine ces cétoacides est ralentie dans les cellules productrices d’insuline du pancréas. En conséquence, les cétoacides s’accumulent au sein des îlots où résident les cellules β.
Indices venant de patients et de modèles animaux
En analysant des échantillons sanguins de personnes diabétiques et de volontaires communautaires, l’équipe a montré que des niveaux circulants plus élevés de ces cétoacides étaient associés à une fonction des cellules β plus faible, même après avoir tenu compte de la résistance à l’insuline. Chez des souris diabétiques et dans des îlots humains de donneurs, des enzymes clés qui normalement dégradent ces cétoacides étaient présentes à des niveaux réduits ou inactivées par des marques chimiques, et les cellules β elles‑mêmes contenaient davantage de ces cétoacides. Lorsque des souris saines ont reçu de l’eau de boisson enrichie en ces molécules, elles sont progressivement devenues moins capables de gérer une charge de sucre, non pas parce que leurs muscles ou leur foie ignoraient l’insuline, mais parce que leurs cellules β ont cessé de libérer suffisamment d’insuline lorsque la glycémie augmentait.
Comment la filière énergétique des cellules β est réorientée
Dans des circonstances normales, le glucose entrant dans une cellule β est dégradé en pyruvate, qui est alors envoyé dans les mitochondries et alimenté dans le cycle de l’acide tricarboxylique pour produire de l’ATP, le signal énergétique qui déclenche la libération rapide d’insuline. En utilisant du glucose marqué par isotopes et des mesures métaboliques de haute précision, les chercheurs ont découvert que l’excès de cétoacides détourne le pyruvate de ce cycle énergétique. Au lieu de pénétrer dans les mitochondries, une plus grande partie est convertie en lactate, un produit final sans issue dans les cellules β. Ce basculement réduit la production d’ATP et atténue l’explosion initiale cruciale d’insuline qui suit normalement une élévation de la glycémie, tout en laissant d’autres aspects de la santé cellulaire, comme la survie et l’absorption générale du glucose, globalement intacts.
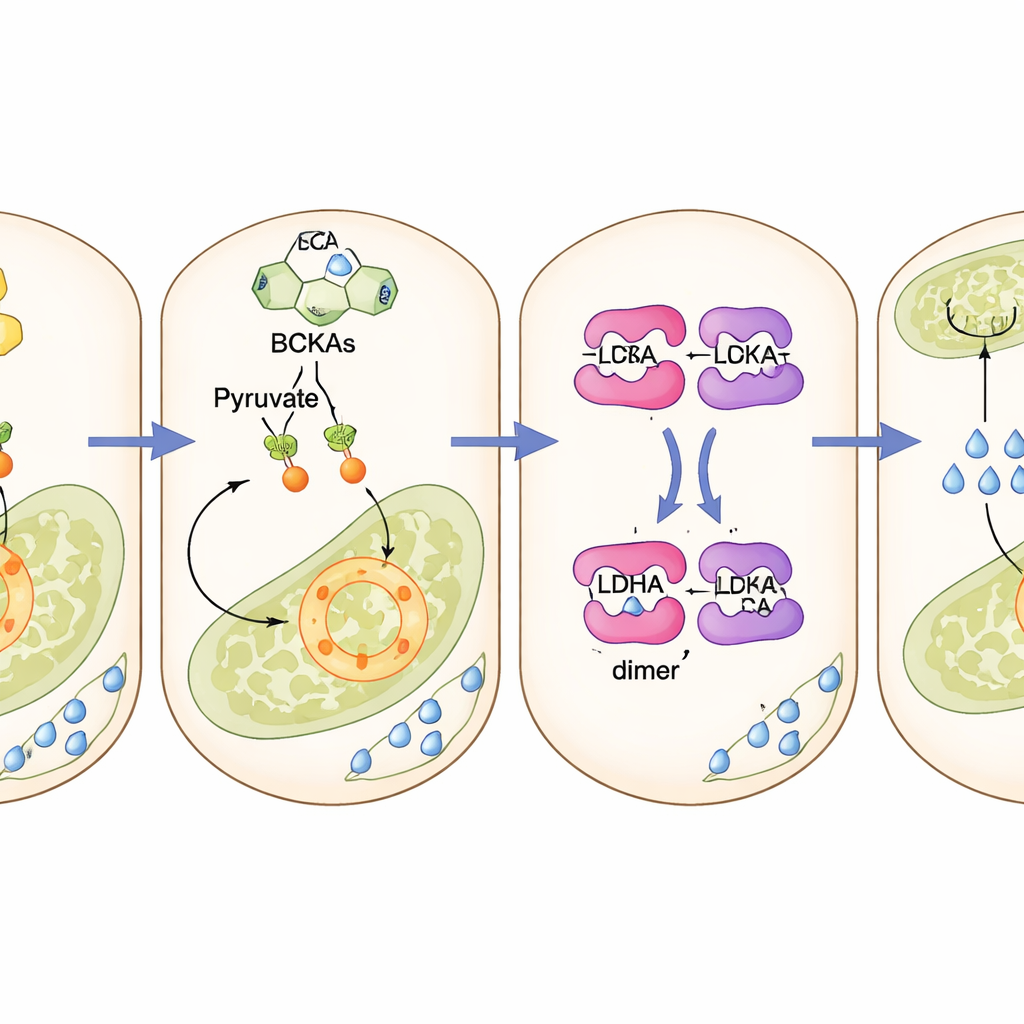
Une enzyme dormante réactivée
Au cœur de cette réorientation se trouve une enzyme appelée lactate déshydrogénase A (LDHA), qui est normalement maintenue silencieuse dans les cellules β afin que le glucose soit orienté vers la production d’énergie plutôt que vers le lactate. L’étude montre que les cétoacides accumulés se lient physiquement à cette enzyme et agissent comme de petits ponts qui rapprochent ses sous‑unités pour la rendre plus active. Une fois activée, l’enzyme attire le pyruvate vers la formation de lactate, privant ainsi les mitochondries de carburant. Bloquer l’enzyme de manière génétique dans les cellules β, ou utiliser un inhibiteur de petite molécule, a protégé les cellules et les souris des effets néfastes des cétoacides et a restauré la sécrétion normale d’insuline. Des médicaments qui réorientent les cétoacides vers leur voie de dégradation habituelle ont eu un effet protecteur similaire.
Ce que cela signifie pour le traitement du diabète
Pour un non‑spécialiste, le message clé est que dans le diabète, le problème ne tient pas seulement à la manière dont l’organisme répond à l’insuline, mais aussi à la façon dont les cellules productrices d’insuline gèrent certains sous‑produits alimentaires. Lorsque la dégradation des acides aminés à chaîne ramifiée est perturbée, leurs descendants céto‑acides s’accumulent, activent une enzyme normalement silencieuse et réorientent le glucose loin de la production d’énergie, affaiblissant la capacité du pancréas à répondre au glucose. Cela suggère que la surveillance de ces cétoacides dans le sang pourrait aider à détecter des cellules β défaillantes, et que l’ajustement maîtrisé de l’apport en acides aminés à chaîne ramifiée ou la mise au point de médicaments visant à restaurer leur élimination correcte pourrait ouvrir de nouvelles voies pour préserver ou récupérer la sécrétion d’insuline dans le diabète de type 2.
Citation: Lin, H., Ho, M.Y.M., Wang, B. et al. Branched-chain α-keto acids impair glucose-stimulated insulin secretion in pancreatic β-cells under diabetes by reactivating the LDHA-lactate axis. Nat Commun 17, 3346 (2026). https://doi.org/10.1038/s41467-026-70004-2
Mots-clés: diabète de type 2, sécrétion d’insuline, acides aminés à chaîne ramifiée, cellules bêta pancréatiques, métabolisme du lactate