Clear Sky Science · es
Los ácidos α-ceto ramificados perjudican la secreción de insulina estimulada por glucosa en las células β pancreáticas en la diabetes al reactivar el eje LDHA-lactato
Por qué este hallazgo importa para la salud cotidiana
La diabetes tipo 2 se describe a menudo como un problema de insensibilidad del cuerpo a la insulina, pero este estudio muestra que las propias células que fabrican insulina también pueden ser envenenadas por ciertos subproductos de nuestra dieta. Los investigadores desvelan cómo productos de degradación específicos de aminoácidos comunes pueden sabotear silenciosamente la liberación de insulina, lo que ayuda a explicar por qué algunas personas con diabetes tienen dificultades para mantener el azúcar en sangre bajo control y apunta a nuevas vías para proteger el páncreas.
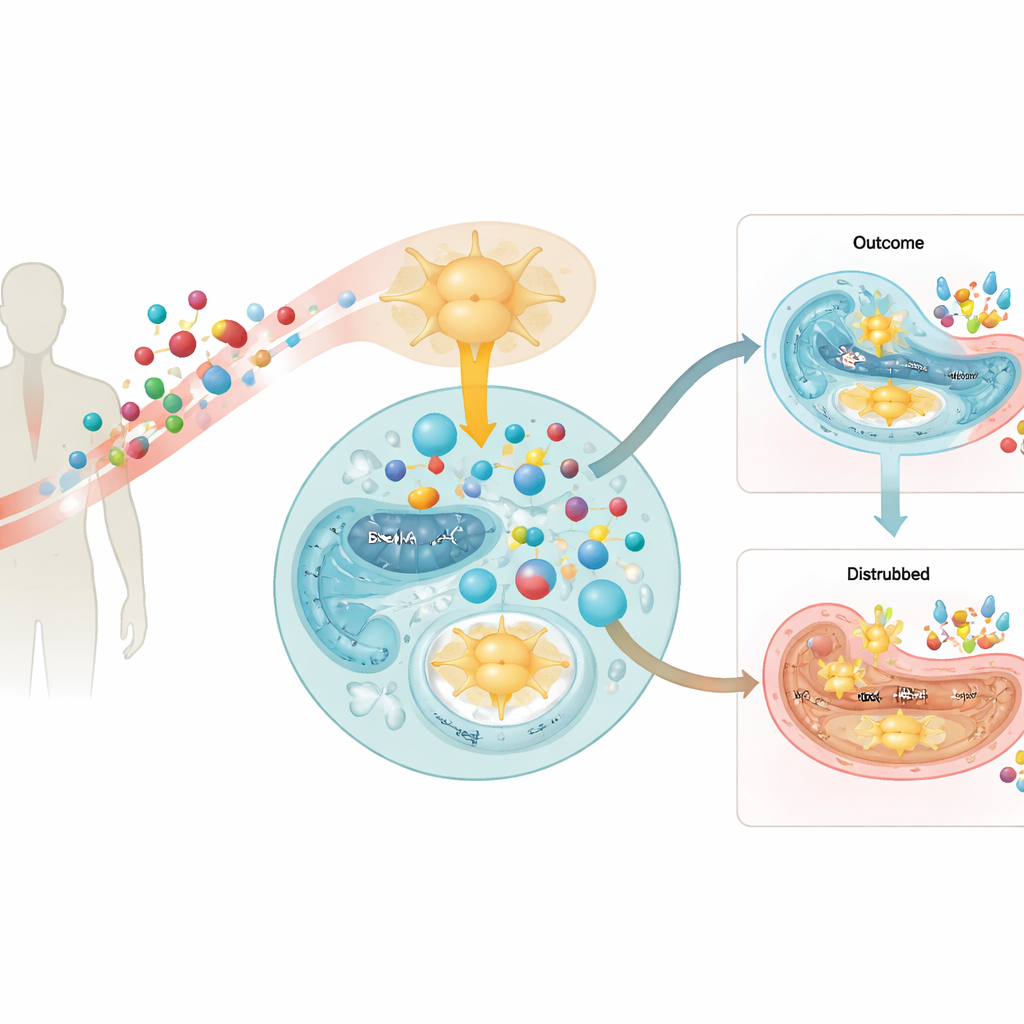
Bloques de construcción dietéticos con un lado oscuro oculto
El trabajo se centra en los aminoácidos de cadena ramificada, nutrientes presentes en alimentos ricos en proteínas y en suplementos deportivos populares. Cuando el cuerpo descompone estos aminoácidos, produce compuestos denominados ácidos α-ceto ramificados. En condiciones saludables, estos cetoácidos se oxidan más en las mitocondrias, las centrales energéticas de la célula, para ayudar a generar energía. Sin embargo, en personas y ratones con diabetes, los autores encontraron que la maquinaria que elimina estos cetoácidos está ralentizada en las células productoras de insulina del páncreas. Como resultado, los cetoácidos se acumulan dentro de los islotes donde residen las células beta.
Pistas de pacientes humanos y modelos animales
Analizando muestras de sangre de personas con diabetes y de voluntarios de la comunidad, el equipo mostró que niveles circulantes más altos de estos cetoácidos se asociaban con una peor función de las células beta, incluso tras ajustar por la resistencia a la insulina. En ratones diabéticos y en islotes humanos donados, enzimas clave que normalmente eliminan los cetoácidos estaban presentes en niveles más bajos o inactivadas por marcas químicas, y las propias células beta contenían más de estos compuestos. Cuando a ratones sanos se les dio agua de bebida enriquecida con estas moléculas, gradualmente se volvieron menos capaces de manejar una carga de azúcar, no porque sus músculos o hígado ignoraran la insulina, sino porque sus células beta dejaron de liberar suficiente insulina cuando aumentaba la glucosa.
Cómo se reconduce la vía energética en las células beta
En circunstancias normales, la glucosa que entra en una célula beta se descompone hasta piruvato, que luego es transportado a las mitocondrias y alimenta el ciclo del ácido tricarboxílico para producir ATP, la señal energética que desencadena la liberación rápida de insulina. Usando glucosa marcada con isótopos y mediciones metabólicas de alta precisión, los investigadores encontraron que el exceso de cetoácidos desvía el piruvato de este ciclo energético. En lugar de entrar en las mitocondrias, más piruvato se convierte en lactato, un producto final sin salida en las células beta. Este cambio redujo la producción de ATP y atenuó el pulso inicial crucial de insulina que normalmente sigue a un aumento de la glucosa en sangre, mientras que dejó otros aspectos de la salud celular, como la supervivencia y la captación general de glucosa, en gran medida intactos.
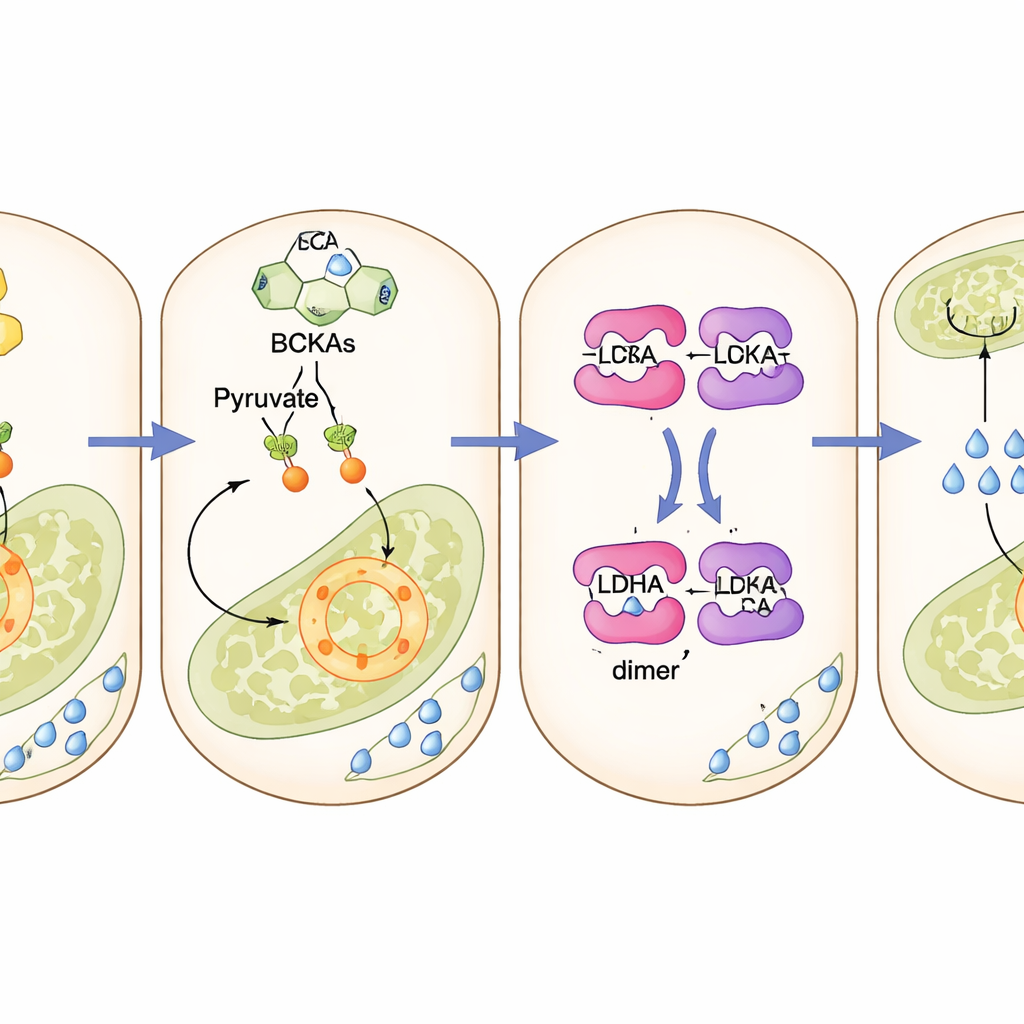
Una enzima dormida que se reactiva
En el corazón de esta desviación está una enzima llamada lactato deshidrogenasa A, que normalmente se mantiene silenciosa en las células beta para que la glucosa se canalice hacia la producción de energía en lugar de hacia el lactato. El estudio muestra que los cetoácidos acumulados se unen físicamente a esta enzima y actúan como pequeños puentes que juntan sus subunidades en una forma más activa. Una vez activada, la enzima dirige el piruvato hacia el lactato, privando a las mitocondrias de combustible. Bloquear la enzima genéticamente en las células beta, o usar un inhibidor de pequeña molécula, protegió a las células y a los ratones de los efectos nocivos de los cetoácidos y restauró la liberación normal de insulina. Fármacos que redirigen los cetoácidos hacia su ruta habitual de degradación tuvieron un efecto rescatador similar.
Qué significa esto para el tratamiento de la diabetes
Para un público no especialista, el mensaje clave es que en la diabetes el problema no es solo cómo responde el cuerpo a la insulina, sino también cómo las células productoras de insulina manejan ciertos subproductos dietéticos. Cuando se altera la degradación de los aminoácidos de cadena ramificada, sus descendientes cetoácidos se acumulan, activan una enzima normalmente silenciosa y desvían la glucosa de la producción de energía, debilitando la capacidad del páncreas para responder a la glucosa. Esto sugiere que monitorizar estos cetoácidos en sangre podría ayudar a detectar células beta en deterioro, y que ajustar con cuidado la ingesta de aminoácidos de cadena ramificada o diseñar medicamentos para restaurar su eliminación adecuada puede abrir nuevas vías para preservar o recuperar la secreción de insulina en la diabetes tipo 2.
Cita: Lin, H., Ho, M.Y.M., Wang, B. et al. Branched-chain α-keto acids impair glucose-stimulated insulin secretion in pancreatic β-cells under diabetes by reactivating the LDHA-lactate axis. Nat Commun 17, 3346 (2026). https://doi.org/10.1038/s41467-026-70004-2
Palabras clave: diabetes tipo 2, secreción de insulina, aminoácidos de cadena ramificada, células beta pancreáticas, metabolismo de la lactato