Clear Sky Science · zh
β1,4-半乳糖基转移酶 III 通过激活整合素–FAK 轴驱动视网膜母细胞瘤侵袭
这项儿童眼部癌症研究为何重要
视网膜母细胞瘤是一种罕见的儿童眼部癌症,多发于非常幼小的孩子。尽管现代治疗能治愈许多病例,但当肿瘤细胞突破眼球并扩散时,仍可能危及生命。本研究揭示了一种肿瘤细胞表面的单一加糖酶如何促使它们更快生长、更牢固地附着于周围环境并侵入邻近组织——以及一种天然化合物如何可能阻断这一过程。理解这一分子连锁反应,可能带来更安全且保眼的治疗方案,惠及高危儿童。
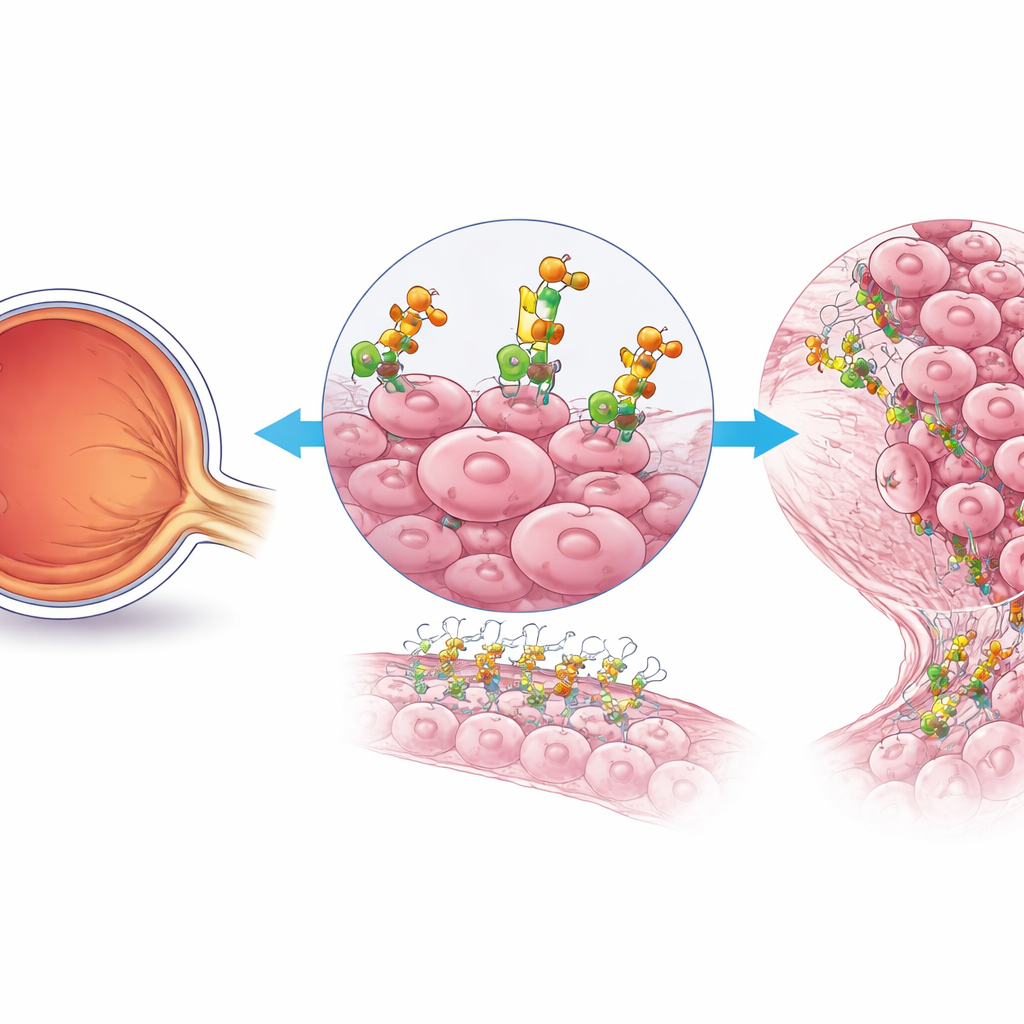
肿瘤生长的隐秘帮手
研究人员聚焦于那些尤为侵袭性强且分裂迅速的视网膜母细胞瘤细胞。通过对患者样本进行单细胞基因分析,他们发现这些细胞在其表面的一条特定糖链合成通路上活动增强。有一类酶尤为突出:B4GALT3,它将糖链附加到蛋白质和脂质上。与正常视网膜相比,视网膜母细胞瘤组织——尤其是在进展期、向外扩散的肿瘤中——表现出显著升高的 B4GALT3 水平。在人类样本和小鼠模型中,B4GALT3 在富含高度增殖肿瘤细胞的区域集中分布,提示其在癌症最危险部分中发挥核心作用。
肿瘤细胞如何抓附并突破屏障
癌细胞必须附着并重塑周围的支持性网状基质才能生长和扩散。研究中,团队发现 B4GALT3 通过给肿瘤细胞表面的一种关键“抓钩”蛋白 β1-整合素 加上糖链,从而对其进行修饰。这种化学修饰增强了该受体与细胞外基质重要成分纤连蛋白的结合能力。当科学家在视网膜母细胞瘤细胞系中降低 B4GALT3 表达时,细胞分裂变慢,对纤连蛋白的粘附减少,且内部信号蛋白 FAK 及其下游生存通路的活性减弱。相反,提高 B4GALT3 则带来相反效应:细胞生长更快,粘附更牢固,增长与存活相关的信号回路被激活。
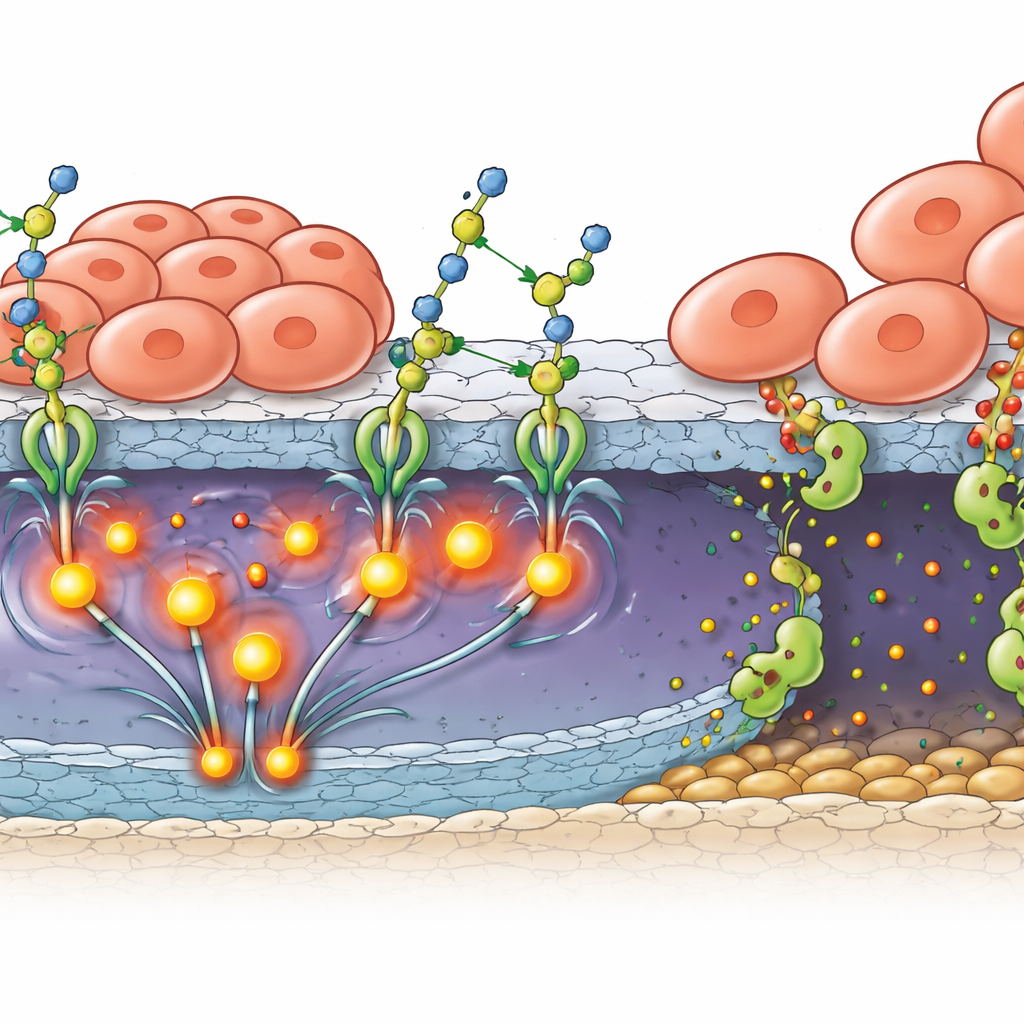
从更强的抓附到主动侵袭
仅有附着并不能解释肿瘤如何刺穿保护眼球后部的天然屏障。研究团队表明,B4GALT3 还促使 MMP2(一种可分解基底膜结构蛋白的蛋白酶)的产生与激活。在患者样本和小鼠肿瘤中,B4GALT3 与 MMP2 在靠近视网膜外缘的肿瘤细胞中共同存在。在体外模型中,当视网膜母细胞瘤细胞铺在视网膜色素上皮细胞之上——后者有助形成外血视网膜屏障——过表达 B4GALT3 的肿瘤细胞使屏障层的紧密连接蛋白丢失、结构变得不连续。阻断 FAK 或 MMP2 均可在很大程度上恢复屏障完整性,将 B4GALT3 的加糖活性与完整的侵袭程序联系起来:抓附更强、信号更强、局部组织消化能力更高。
动物模型验证及一种天然化合物的抑制作用
在注射视网膜母细胞瘤细胞的小鼠中,过表达 B4GALT3 的肿瘤长得更大,导致眼球突出,表面糖基异常增多,分裂中的癌细胞增多而凋亡细胞减少。降低 B4GALT3 的肿瘤则呈现相反特征,体积更小且侵袭性较低。为将此发现转化为潜在疗法,研究者通过计算模拟筛选 B4GALT3 结构的天然化合物库,鉴定出 myricoside(一种来自植物的分子)能紧密嵌入该酶的活性位点。在细胞实验中,myricoside 降低了视网膜母细胞瘤细胞的存活率,减弱其对纤连蛋白的粘附,降低了 β1-整合素 上的糖基装饰,并抑制了 FAK 生存通路,模拟了 B4GALT3 基因缺失的效应。
这对未来治疗意味着什么
将 myricoside 直接注入带瘤小鼠眼内后,肿瘤缩小、侵袭特征减少、B4GALT3 和 MMP2 信号减弱、屏障蛋白恢复且癌细胞凋亡增加——而正常视网膜层未见明显损伤。总体而言,这项工作勾勒出一幅清晰图景:B4GALT3 位于一条链的上游,赋予视网膜母细胞瘤细胞更强的抓附、信号传导与穿透眼部防御的能力。对非专业读者而言,结论是:一种原被视为背景作用的加糖酶,实际上是让这种儿童癌症更具侵袭性的关键开关。以 myricoside 之类的药物靶向 B4GALT3,或可阻止肿瘤突破眼球,从而提高儿童保留视力与生命的机会。
引用: Tang, J., Li, J., Wang, M. et al. β1,4-galactosyltransferase III drives retinoblastoma invasion via activation of integrin-FAK axis. Cell Death Dis 17, 336 (2026). https://doi.org/10.1038/s41419-026-08620-5
关键词: 视网膜母细胞瘤, 癌症侵袭, 糖基化, 整合素信号传导, 靶向治疗