Clear Sky Science · de
β1,4-Galactosyltransferase III treibt die Invasion von Retinoblastomen durch Aktivierung der Integrin-FAK-Achse voran
Warum diese Studie zu diesem kindlichen Augenkrebs wichtig ist
Das Retinoblastom ist ein seltener Augenkrebs, der sehr junge Kinder betrifft. Obwohl viele Fälle mit modernen Therapien inzwischen heilbar sind, kann die Krankheit tödlich werden, wenn Tumorzellen aus dem Auge austreten und sich ausbreiten. Diese Studie zeigt, wie ein einzelnes, zuckeranhängendes Enzym auf Tumorzellen ihnen hilft, schneller zu wachsen, ihre Umgebung stärker zu greifen und in benachbartes Gewebe einzudringen — und wie eine natürliche Verbindung diesen Prozess blockieren könnte. Das Verständnis dieser molekularen Kettenreaktion könnte zu schonenderen, das Auge erhaltenden Behandlungen für Kinder mit hohem Risiko führen.
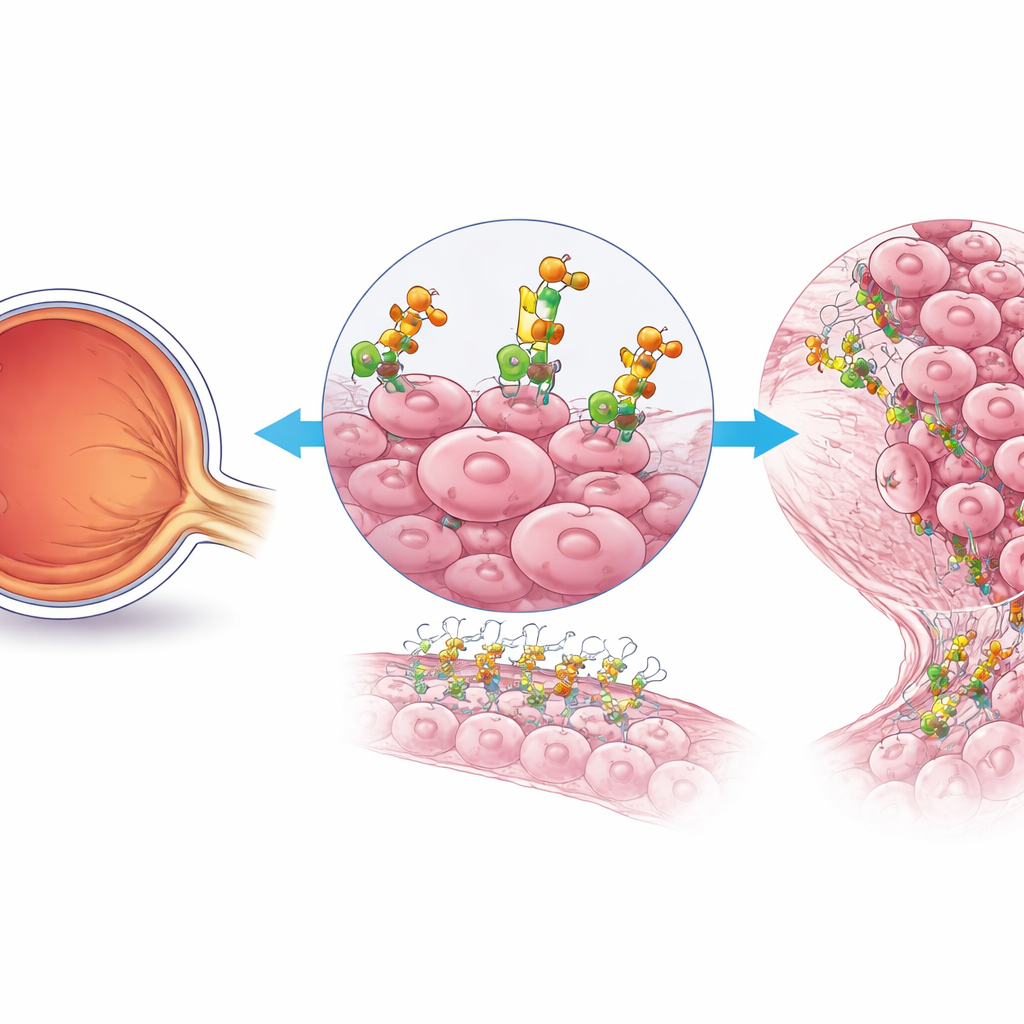
Ein versteckter Helfer des Tumorwachstums
Die Forschenden konzentrierten sich auf Retinoblastomzellen, die besonders aggressiv und schnell teilungsaktiv sind. Mithilfe einzelzellgenetischer Analysen von Patientenproben fanden sie, dass diese Zellen die Aktivität eines bestimmten auf der Zelloberfläche ablaufenden Zuckeraufbauwegs hochfahren. Ein Enzym stach hervor: B4GALT3, das Proteine und Lipide mit Zuckerketten versieht. Im Vergleich zur normalen Netzhaut zeigte das Retinoblastomgewebe — besonders in fortgeschrittenen, nach außen streuenden Tumoren — deutlich erhöhte B4GALT3-Spiegel. In menschlichen Proben und Mausmodellen konzentrierte sich B4GALT3 in Regionen mit hoher Zellproliferation, was darauf hindeutet, dass es eine zentrale Rolle im gefährlichsten Anteil des Tumors spielt.
Wie Tumorzellen greifen und Barrieren durchbrechen
Krebszellen müssen sich an das sie stützende Geflecht heften und es umgestalten, um zu wachsen und sich auszubreiten. In dieser Studie entdeckte das Team, dass B4GALT3 ein wichtiges "Greifhaken"-Protein auf der Tumorzelloberfläche, das β1-Integrin, durch Anhängen von Zuckerketten modifiziert. Diese chemische Veränderung verstärkt die Fähigkeit des Rezeptors, an Fibronectin zu binden, einen Hauptbestandteil des stützenden Gewebes im Auge. Wenn die Wissenschaftler B4GALT3 in Retinoblastomzelllinien reduzierten, teilten sich die Zellen langsamer, hafteten schlechter an Fibronectin und zeigten geringere Aktivität eines intrazellulären Signalmoleküls namens FAK sowie seines nachgeschalteten Überlebenswegs. Eine Erhöhung von B4GALT3 bewirkte das Gegenteil: Die Zellen wuchsen schneller, hafteten fester und schalteten diese Wachstums- und Überlebensschaltung ein.
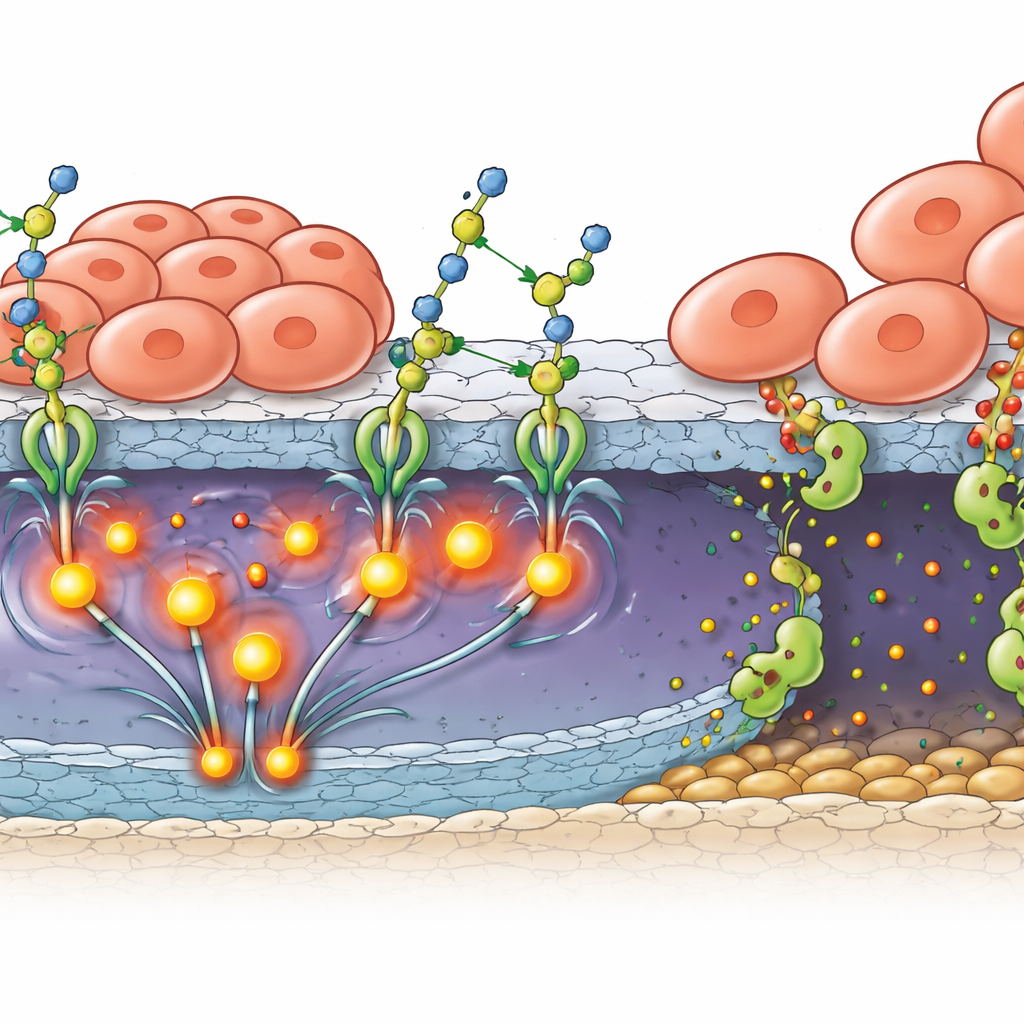
Vom stärkeren Halt zur aktiven Invasion
Allein die Anheftung erklärt nicht, wie Tumoren die natürlichen Barrieren durchstoßen, die den hinteren Teil des Auges schützen. Das Team zeigte, dass B4GALT3 auch die Produktion und Aktivierung von MMP2 fördert, einem Protein, das Strukturproteine in Basalmembranen abbaut. In Patientenproben und Maustumoren wurden B4GALT3 und MMP2 gemeinsam in Tumorzellen nahe der äußeren Grenze der Netzhaut nachgewiesen. In Labormodellen, bei denen Retinoblastomzellen über retinalen Pigmentepithelzellen geschichtet wurden — den Zellen, die zur äußeren blut-retina-Schranke beitragen — führten Tumorzellen mit erhöhtem B4GALT3 dazu, dass die Barrierenzellen ihre dichtenden Proteine verloren und die Schicht diskontinuierlich wurde. Die Hemmung von FAK oder MMP2 konnte einen Großteil dieser Barrierefunktion wiederherstellen und verband damit die zuckeranhängende Aktivität von B4GALT3 mit einem vollständigen Invasionsprogramm: stärkerer Halt, stärkere Signalgebung und intensivere lokale Gewebeauflösung.
Beleg in Tiermodellen und ein natürlicher Hemmstoff
Bei Mäusen, denen Retinoblastomzellen injiziert wurden, wuchsen Tumoren, die zur Überproduktion von B4GALT3 programmiert waren, größer, verursachten eine Vorwölbung des Auges, zeigten mehr abnorme Oberflächenzucker und enthielten mehr teilende sowie weniger sterbende Krebszellen. Tumoren mit reduziertem B4GALT3 zeigten das Gegenteil: Sie blieben kleiner und weniger invasiv. Um diese Erkenntnis in eine mögliche Therapie zu überführen, durchsuchten die Forschenden eine Bibliothek natürlicher Verbindungen mithilfe von Computermodellen der B4GALT3-Struktur. Sie identifizierten Myricosid, ein pflanzliches Molekül, das gut in die aktive Tasche des Enzyms passt. In Zelltests verringerten Myricosid die Lebensfähigkeit von Retinoblastomzellen, reduzierte ihre Haftung an Fibronectin, senkte die Zuckeranlagerung am β1-Integrin und dämpfte den FAK-Überlebensweg — Effekte, die einem genetischen Verlust von B4GALT3 ähneln.
Was das für künftige Behandlungen bedeuten könnte
Wurde Myricosid direkt in die Augen von tumortragenden Mäusen verabreicht, schrumpften die Tumoren, invasive Merkmale nahmen ab, B4GALT3- und MMP2-Signale wurden reduziert, Barriereproteine wiederhergestellt und der Zelltod der Krebszellen stieg — ohne offensichtliche Schäden an normalen Netzhautschichten. Insgesamt ergibt sich ein klares Bild: B4GALT3 steht nahe dem Anfang einer Kette, die es Retinoblastomzellen erlaubt, sich festzuhalten, Signale zu aktivieren und sich durch die Abwehr des Auges zu fressen. Für Nichtfachleute ist die Botschaft, dass ein einst als Nebendarsteller betrachtetes zuckeranhängendes Enzym tatsächlich ein schaltendes Element ist, das diesen kindlichen Krebs invasiver macht. Die gezielte Hemmung von B4GALT3 mit Wirkstoffen wie Myricosid könnte verhindern, dass Tumoren aus dem Auge ausbrechen, und so die Chancen erhöhen, dass Kinder sowohl ihr Sehvermögen als auch ihr Leben behalten.
Zitation: Tang, J., Li, J., Wang, M. et al. β1,4-galactosyltransferase III drives retinoblastoma invasion via activation of integrin-FAK axis. Cell Death Dis 17, 336 (2026). https://doi.org/10.1038/s41419-026-08620-5
Schlüsselwörter: Retinoblastom, Krebsinvasion, Glykosylierung, Integrin-Signalgebung, zielgerichtete Therapie