Clear Sky Science · pl
β1,4-galaktozylotransferaza III napędza inwazję siatkówczaka poprzez aktywację osi integryna-FAK
Dlaczego to badanie dotyczące dziecięcego raka oka ma znaczenie
Siatkówczak to rzadki rak oka występujący u bardzo małych dzieci; choć współczesne terapie leczą wiele przypadków, choroba nadal może być śmiertelna, gdy komórki nowotworowe wydostaną się z oka i rozprzestrzenią. W badaniu tym wykazano, jak pojedynczy enzym doklejający cukry na powierzchni komórek nowotworowych pomaga im szybciej rosnąć, mocniej przyczepiać się do otoczenia i naciekać pobliskie tkanki — oraz jak związek naturalnego pochodzenia może zablokować ten proces. Zrozumienie tego molekularnego łańcucha reakcji może doprowadzić do bezpieczniejszych, zachowujących oko terapii dla dzieci o najwyższym ryzyku.
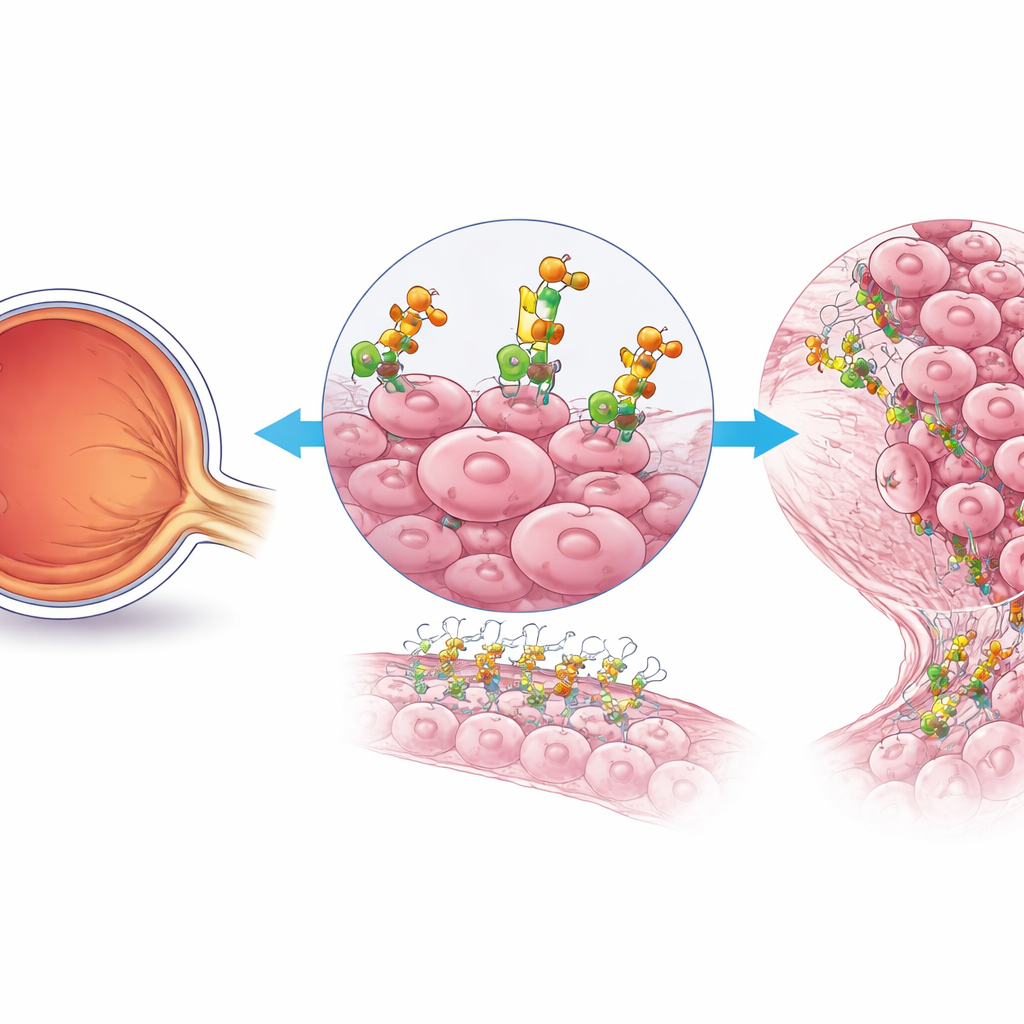
Ukryty współpracownik wzrostu guza
Naukowcy skupili się na komórkach siatkówczaka, które są szczególnie agresywne i szybko się dzielą. Dzięki analizie jednoukładowej materiału genetycznego z próbek pacjentów stwierdzili, że te komórki nasilają aktywność konkretnej ścieżki budowania łańcuchów cukrowych na swojej powierzchni. Wyróżniał się jeden enzym: B4GALT3, który ozdabia białka i lipidy łańcuchami sacharydowymi. W porównaniu ze zdrową siatkówką tkanka siatkówczaka — zwłaszcza w zaawansowanych guzach rozprzestrzeniających się na zewnątrz — wykazywała znacznie wyższy poziom B4GALT3. Zarówno w próbkach ludzkich, jak i modelach mysich, B4GALT3 koncentrowała się w obszarach wypełnionych silnie proliferującymi komórkami nowotworowymi, co sugeruje jej centralną rolę w najniebezpieczniejszej części guza.
Jak komórki nowotworowe chwytają i przebijają bariery
Komórki nowotworowe muszą przyczepiać się do i przebudowywać podporową sieć otaczającą je, by rosnąć i rozprzestrzeniać się. W badaniu zespół odkrył, że B4GALT3 modyfikuje kluczowe „hakowate” białko na powierzchni komórki nowotworowej, β1-integrynę, poprzez doklejanie do niej łańcuchów cukrowych. Ta chemiczna „dekoracja” wzmacnia zdolność receptora do wiązania fibryonektyny, głównego składnika tkanki podporowej oka. Gdy naukowcy zmniejszyli poziom B4GALT3 w liniach komórkowych siatkówczaka, komórki dzieliły się wolniej, słabiej przyczepiały do fibryonektyny i wykazywały osłabioną aktywność wewnątrzkomórkowego białka sygnałowego FAK oraz jego dalszej ścieżki przetrwania. Zwiększenie poziomu B4GALT3 wywołało efekt odwrotny: komórki rosły szybciej, przyczepiały się mocniej i aktywowały ten szlak wzrostu i przeżycia.
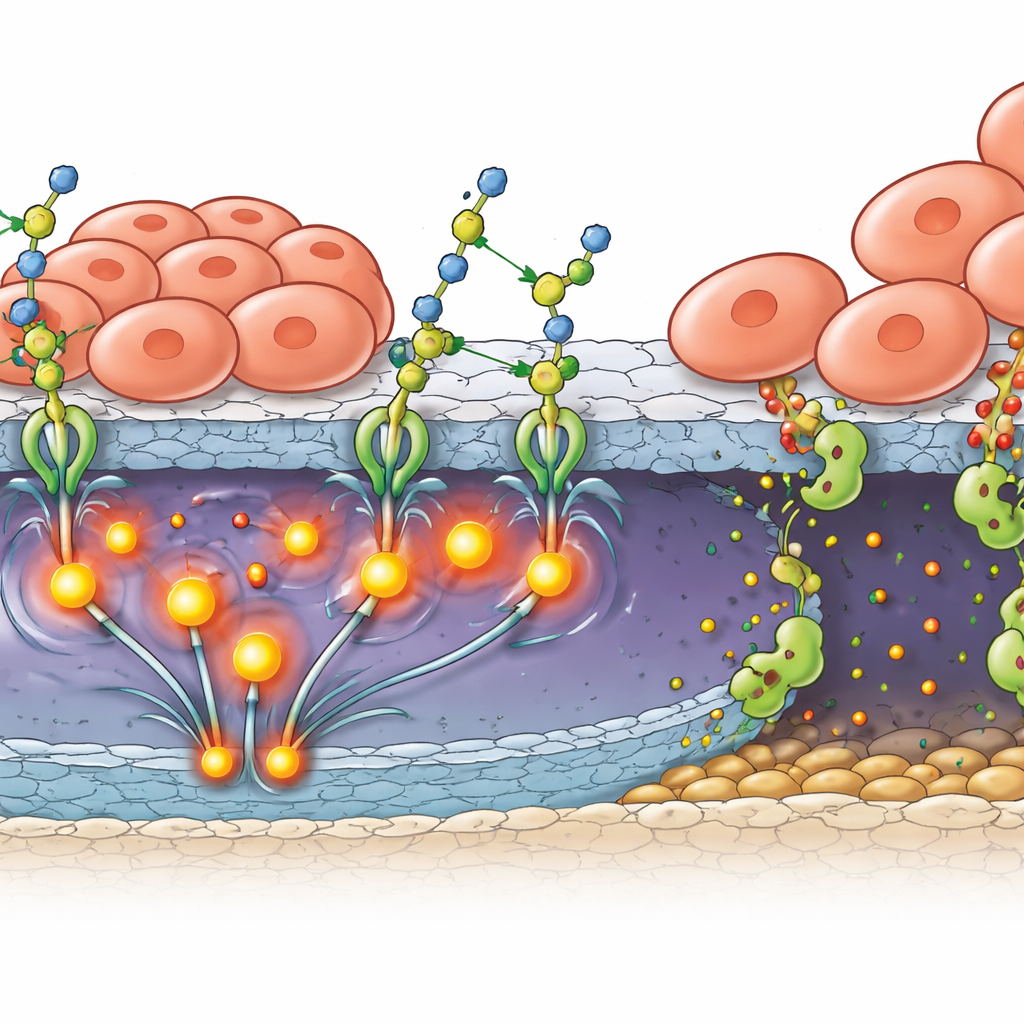
Od silniejszego chwytu do aktywnej inwazji
Samo przytwierdzenie się nie wyjaśnia, jak guzy przebijają naturalne bariery chroniące tylną część oka. Zespół wykazał, że B4GALT3 napędza także produkcję i aktywację MMP2 — białka rozkładającego strukturalne składniki błon podstawnych. W próbkach pacjentów i guzach mysich B4GALT3 i MMP2 występowały razem w komórkach nowotworowych w pobliżu zewnętrznej granicy siatkówki. W hodowlach laboratoryjnych, w których komórki siatkówczaka układano nad komórkami nabłonka barwnikowego siatkówki — komórkami pomagającymi tworzyć zewnętrzną barierę krew–siatkówka — komórki nowotworowe z nadmiarem B4GALT3 spowodowały utratę białek uszczelniających warstwę bariery i jej nieciągłość. Zablokowanie FAK lub MMP2 mogło przywrócić dużą część integralności tej bariery, łącząc aktywność doklejania cukrów przez B4GALT3 z pełnym programem inwazji: mocniejszy chwyt, silniejsza sygnalizacja i intensywniejsze miejscowe trawienie tkanek.
Dowód w modelach zwierzęcych i naturalny inhibitor
U myszy wstrzykniętych komórkami siatkówczaka guzy genetycznie zmodyfikowane do nadprodukcji B4GALT3 były większe, powodowały uwypuklenie oka, wykazywały więcej nieprawidłowych powierzchniowych cukrów oraz zawierały więcej dzielących się i mniej umierających komórek nowotworowych. Guzy z obniżonym B4GALT3 zachowywały się odwrotnie — pozostawały mniejsze i mniej inwazyjne. Aby przekuć to odkrycie w potencjalną terapię, badacze przeszukali bibliotekę związków naturalnych, używając modeli komputerowych struktury B4GALT3. Zidentyfikowali myrykozyd, związek roślinny dobrze dopasowany do aktywnego miejsca enzymu. W testach komórkowych myrykozyd zmniejszał żywotność komórek siatkówczaka, osłabiał ich przyczepność do fibryonektyny, obniżał ozdabianie β1-integryny łańcuchami cukrowymi i tłumił szlak przetrwania FAK, naśladując genetyczną utratę B4GALT3.
Co to może znaczyć dla przyszłych terapii
Podawany bezpośrednio do oczu myszy z guzami myrykozyd zmniejszał rozmiar guzów, ograniczał cechy inwazyjne, obniżał sygnały B4GALT3 i MMP2, przywracał białka bariery i zwiększał śmierć komórek nowotworowych — bez oczywistych szkód dla normalnych warstw siatkówki. Całość prac układa się w jasny obraz: B4GALT3 znajduje się blisko szczytu łańcucha, który pozwala komórkom siatkówczaka chwytać, sygnalizować i przedzierać się przez obronę oka. Dla odbiorców niebędących specjalistami wniosek jest taki, że enzym doklejający cukry, kiedyś uważany za drugoplanowego aktora, jest w rzeczywistości kluczowym przełącznikiem zwiększającym inwazyjność tego dziecięcego nowotworu. Celowanie w B4GALT3 za pomocą leków takich jak myrykozyd mogłoby pomóc powstrzymać guzy przed wydostawaniem się z oka, zwiększając szansę, że dzieci zachowają wzrok i życie.
Cytowanie: Tang, J., Li, J., Wang, M. et al. β1,4-galactosyltransferase III drives retinoblastoma invasion via activation of integrin-FAK axis. Cell Death Dis 17, 336 (2026). https://doi.org/10.1038/s41419-026-08620-5
Słowa kluczowe: siatkówczak, inwazja nowotworu, glikozylacja, sygnalizacja integryn, terapia celowana