Clear Sky Science · fr
La β1,4-galactosyltransférase III favorise l’invasion du rétinoblastome via l’activation de l’axe intégrine-FAK
Pourquoi cette étude sur le cancer oculaire pédiatrique est importante
Le rétinoblastome est un cancer rare de l’œil qui touche de très jeunes enfants. Bien que de nombreux cas puissent aujourd’hui être guéris grâce aux traitements modernes, la maladie peut rester mortelle lorsque des cellules tumorales s’échappent de l’œil et se propagent. Cette étude révèle comment une seule enzyme qui ajoute des sucres à la surface des cellules tumorales leur permet de croître plus rapidement, d’adhérer plus fortement à leur environnement et d’envahir les tissus voisins — et comment un composé d’origine naturelle pourrait bloquer ce processus. Comprendre cette chaîne moléculaire pourrait conduire à des traitements plus sûrs, préservant l’œil, pour les enfants les plus à risque.
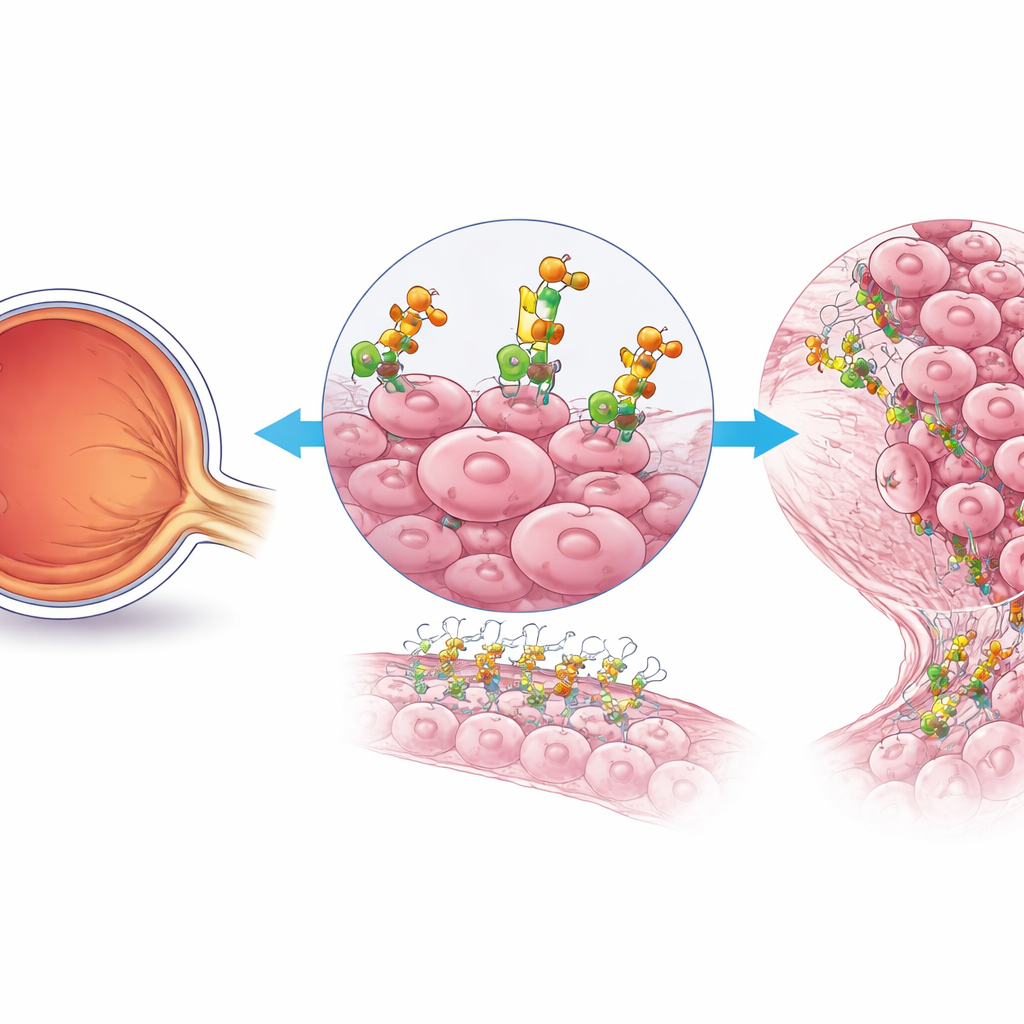
Un auxiliaire caché de la croissance tumorale
Les chercheurs se sont concentrés sur des cellules de rétinoblastome particulièrement agressives et à division rapide. Grâce à une analyse génétique cellule par cellule d’échantillons de patients, ils ont constaté que ces cellules augmentent l’activité d’une voie spécifique de construction de sucres à leur surface. Une enzyme s’est distinguée : B4GALT3, qui orne des protéines et des lipides de chaînes de molécules sucrées. Par rapport à la rétine normale, les tissus de rétinoblastome — en particulier dans les tumeurs avancées et en extension vers l’extérieur — présentaient des niveaux beaucoup plus élevés de B4GALT3. Chez l’humain comme chez la souris, B4GALT3 se concentrait dans des zones riches en cellules tumorales hautement prolifératives, ce qui suggère qu’elle joue un rôle central dans la partie la plus dangereuse du cancer.
Comment les cellules tumorales s’accrochent et traversent les barrières
Pour croître et se disséminer, les cellules cancéreuses doivent s’accrocher au maillage de soutien qui les entoure et le remodeler. Dans cette étude, l’équipe a découvert que B4GALT3 modifie une protéine-clé de « crochet » à la surface des cellules tumorales appelée β1-intégrine en y ajoutant des chaînes de sucres. Cette modification chimique renforce la capacité du récepteur à se lier à la fibronectine, un composant majeur du tissu de soutien de l’œil. Lorsque les scientifiques ont réduit l’expression de B4GALT3 dans des lignées de rétinoblastome, les cellules se divisaient plus lentement, adhéraient moins bien à la fibronectine et présentaient une activité moindre d’une protéine de signalisation interne appelée FAK ainsi que de sa voie de survie en aval. À l’inverse, surexprimer B4GALT3 favorisait la croissance cellulaire, une adhérence plus forte et l’activation de ce circuit de croissance et de survie.
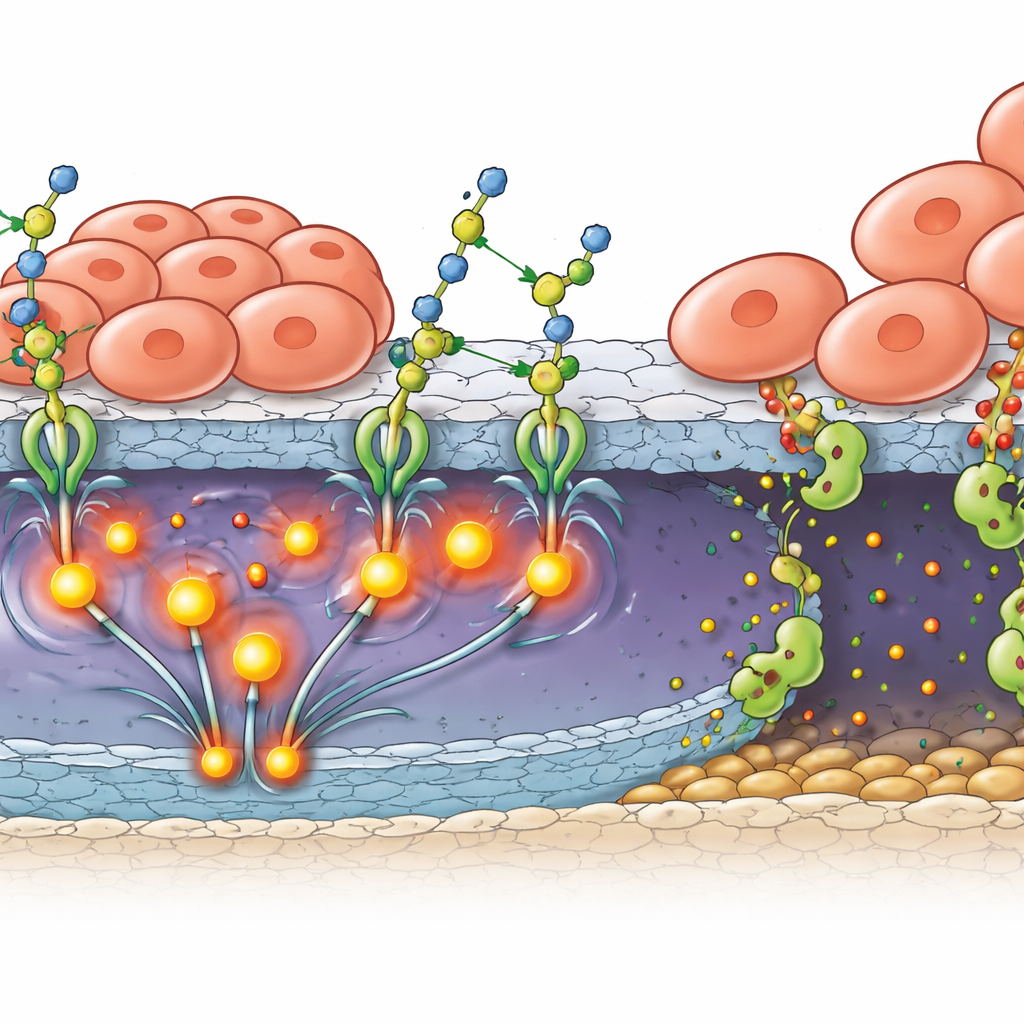
De l’adhérence renforcée à une invasion active
L’adhérence seule n’explique pas comment les tumeurs percent les barrières naturelles qui protègent l’arrière de l’œil. L’équipe a montré que B4GALT3 stimule aussi la production et l’activation de MMP2, une protéine qui digère les protéines structurelles des membranes basales. Dans des échantillons de patients et des tumeurs de souris, B4GALT3 et MMP2 étaient retrouvées ensemble dans les cellules tumorales proches de la bordure externe de la rétine. Dans des modèles in vitro où des cellules de rétinoblastome étaient disposées au‑dessus de cellules épithéliales pigmentaires rétiniennes — les cellules qui contribuent à former la barrière sang–rétine externe — les cellules tumorales sur‑exprimant B4GALT3 provoquaient la perte des protéines d’étanchéité de la couche barrière et sa discontinuité. Le blocage de FAK ou de MMP2 permettait de restaurer en grande partie l’intégrité de cette barrière, reliant l’activité glycosylante de B4GALT3 à un programme d’invasion complet : adhérence renforcée, signalisation accrue et digestion locale plus intense des tissus.
Preuves dans des modèles animaux et un inhibiteur d’origine naturelle
Chez des souris injectées avec des cellules de rétinoblastome, les tumeurs génétiquement modifiées pour surexprimer B4GALT3 étaient plus volumineuses, causaient une protrusion oculaire, présentaient davantage de sucres de surface anormaux et contenaient plus de cellules en division et moins de cellules en mort. Les tumeurs avec une expression réduite de B4GALT3 présentaient l’effet inverse : elles restaient plus petites et moins invasives. Pour transformer cette découverte en une piste thérapeutique, les chercheurs ont exploré une bibliothèque de composés naturels en s’appuyant sur des modèles informatiques de la structure de B4GALT3. Ils ont identifié la myricoside, une molécule végétale qui s’insère bien dans la poche active de l’enzyme. In vitro, la myricoside diminuait la viabilité des cellules de rétinoblastome, réduisait leur adhérence à la fibronectine, abaissait la glycosylation de la β1-intégrine et atténuait la voie de survie FAK, imitant la perte génétique de B4GALT3.
Ce que cela pourrait signifier pour les traitements futurs
Quand elle a été administrée directement dans les yeux de souris porteuses de tumeurs, la myricoside a réduit la taille des tumeurs, diminué les caractéristiques d’invasion, abaissé les signaux de B4GALT3 et de MMP2, restauré les protéines de la barrière et augmenté la mort des cellules cancéreuses — sans dommage évident des couches rétiniennes normales. Dans l’ensemble, ce travail brosse un tableau net : B4GALT3 se situe près du sommet d’une chaîne qui permet aux cellules de rétinoblastome de s’accrocher, de signaler et de percer les défenses de l’œil. Pour le grand public, la conclusion est qu’une enzyme d’ajout de sucres, naguère considérée comme un acteur secondaire, constitue en réalité un commutateur majeur rendant ce cancer infantile plus invasif. Cibler B4GALT3 avec des molécules comme la myricoside pourrait empêcher les tumeurs de s’échapper de l’œil, améliorant ainsi les chances pour les enfants de conserver leur vision et leur vie.
Citation: Tang, J., Li, J., Wang, M. et al. β1,4-galactosyltransferase III drives retinoblastoma invasion via activation of integrin-FAK axis. Cell Death Dis 17, 336 (2026). https://doi.org/10.1038/s41419-026-08620-5
Mots-clés: rétinoblastome, invasion cancéreuse, glycosylation, signalisation des intégrines, thérapie ciblée