Clear Sky Science · nl
β1,4-galactosyltransferase III drijft retinoblastoominvasie via activatie van de integrine-FAK-as
Waarom deze studie over kinderoogkanker ertoe doet
Retinoblastoom is een zeldzame oogkanker die vooral zeer jonge kinderen treft. Hoewel veel gevallen tegenwoordig met moderne behandelingen te genezen zijn, kan de ziekte levensbedreigend worden wanneer tumorcellen uit het oog uitbreken en zich verspreiden. Deze studie onthult hoe een enkel suikerbindend enzym op tumorcellen hen helpt sneller te groeien, zich steviger aan hun omgeving vast te hechten en omliggend weefsel binnen te dringen — en hoe een natuurlijke verbinding dit proces mogelijk kan blokkeren. Inzicht in deze moleculaire ketenreactie kan leiden tot veiliger, oogbehoudende behandelingen voor kinderen met het hoogste risico.
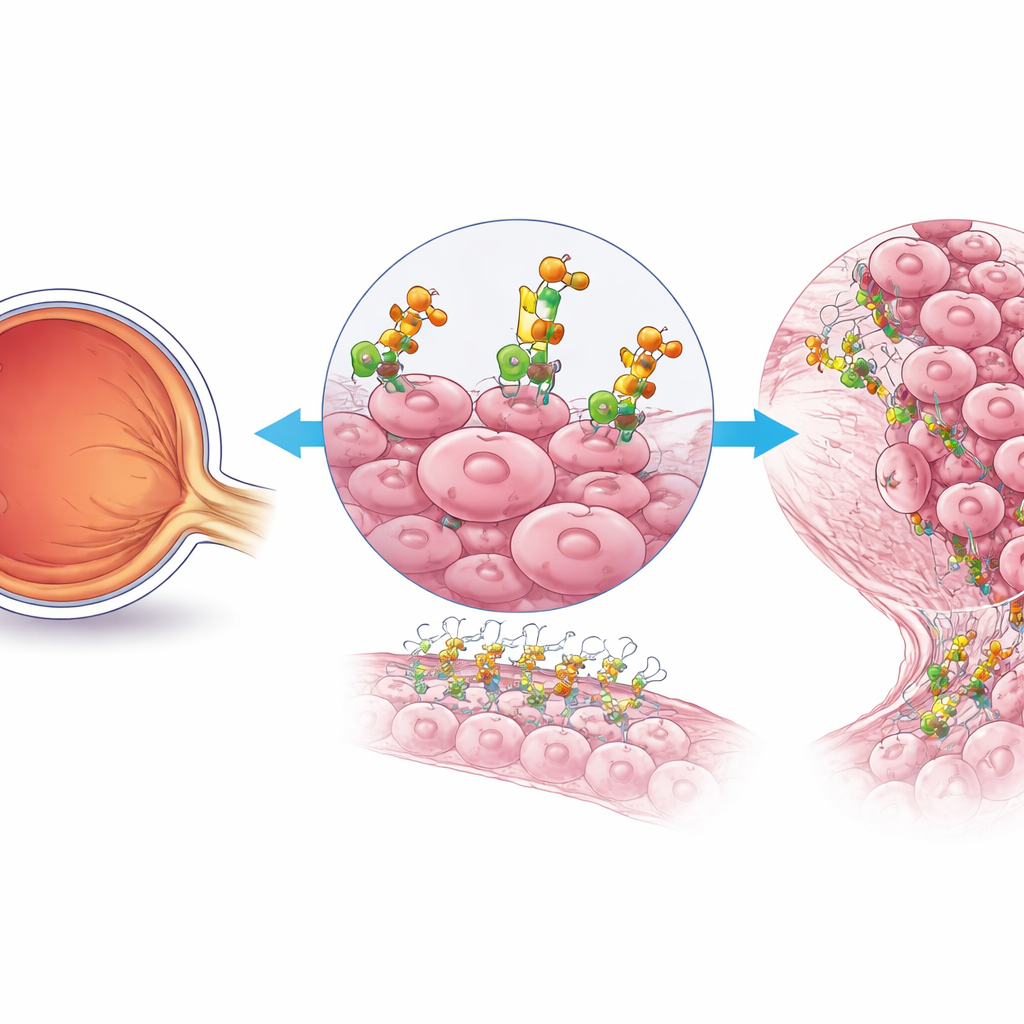
Een verborgen helper van tumorgroei
De onderzoekers richtten zich op retinoblastoomcellen die bijzonder agressief en snel delend zijn. Met behulp van enkelcellig genetisch onderzoek van patiëntmonsters ontdekten ze dat deze cellen de activiteit opvoeren in een specifiek suikeropbouwend pad aan hun oppervlakte. Één enzym sprong eruit: B4GALT3, dat eiwitten en vetten voorziet van ketens van suikermoleculen. In vergelijking met normaal netvlies vertoonde retinoblastoomweefsel — vooral in gevorderde, naar buiten uitbreidende tumoren — veel hogere B4GALT3-niveaus. Zowel in menselijke monsters als in muismodellen was B4GALT3 geconcentreerd in regio’s vol met sterk prolifererende tumorcellen, wat suggereert dat het een centrale rol speelt in het gevaarlijkste deel van de kanker.
Hoe tumorcellen zich vasthechten en barrières doorbreken
Kankercellen moeten zich vasthechten aan en het ondersteunende netwerk rond hen omvormen om te groeien en zich te verspreiden. In deze studie ontdekten de onderzoekers dat B4GALT3 een sleutelproteïne op het celoppervlak — β1-integrine, een soort ‘haak’ — wijzigt door er suikerketens aan toe te voegen. Deze chemische versiering versterkt het vermogen van de receptor om te binden aan fibronectine, een belangrijk bestanddeel van het steunweefsel in het oog. Wanneer de wetenschappers B4GALT3 in retinoblastoomcelijnen verminderden, deelden de cellen langzamer, hechtten ze minder goed aan fibronectine en vertoonden ze zwakkere activiteit in een intern signaalproteïne genaamd FAK en het downstream overlevingspad. Verhogen van B4GALT3 had het omgekeerde effect: cellen groeiden sneller, kleefden steviger en schakelden deze groei- en overlevingscircuit in.
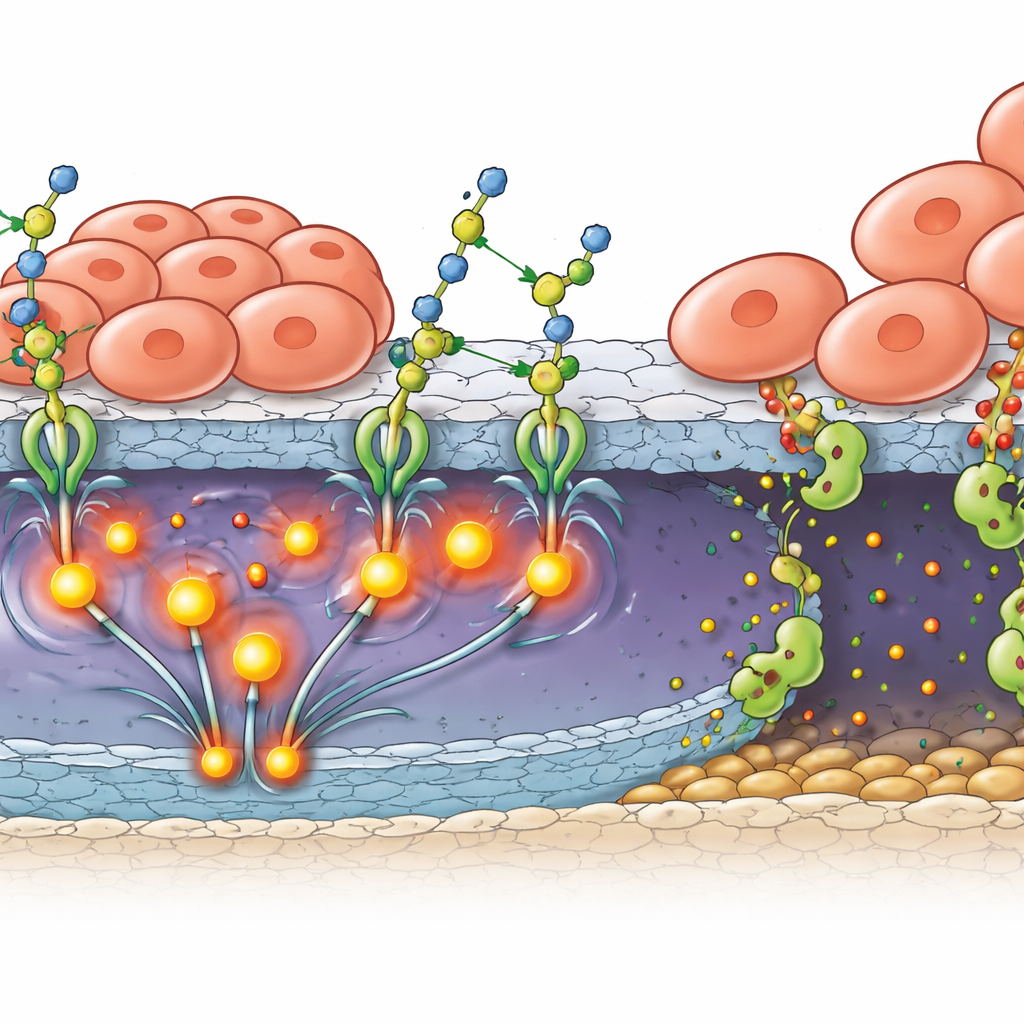
Van sterkere grip naar actieve invasie
Alleen aanhechting verklaart niet hoe tumoren de natuurlijke barrières doorboren die de achterkant van het oog beschermen. Het team toonde aan dat B4GALT3 ook de productie en activatie van MMP2 stimuleert, een eiwit dat structurele eiwitten in basale membranen afbreekt. In patiëntmonsters en muizentumoren werden B4GALT3 en MMP2 samen aangetroffen in tumorcellen nabij de buitengrens van het netvlies. In in-vitromodellen waarbij retinoblastoomcellen boven op retinale pigmentepitheelcellen lagen — de cellen die helpen bij het vormen van de buitenste bloed–netvliesbarrière — veroorzaakten tumoren met extra B4GALT3 dat de barrièrelaag haar sluitende eiwitten verloor en discontinu werd. Het blokkeren van FAK of MMP2 kon een groot deel van deze barrière-integriteit herstellen, waarmee de suikertoevoegende activiteit van B4GALT3 wordt verbonden met een volledig invasieprogramma: sterkere grip, sterkere signalering en krachtigere lokale weefselafbraak.
Bewijs in diermodellen en een natuurlijke remmer
Bij muizen die geïnjecteerd waren met retinoblastoomcellen, groeiden tumoren die waren genetisch gemodificeerd om B4GALT3 te overproduceren groter, veroorzaakten ze uitpuiling van het oog, vertoonden ze meer abnormale oppervlakte-sugars en bevatten ze meer delende en minder stervende kankercellen. Tumoren met verminderde B4GALT3 deden het tegenovergestelde: ze bleven kleiner en minder invasief. Om dit inzicht naar een potentiële therapie te vertalen, doorzochten de onderzoekers een bibliotheek van natuurlijke verbindingen met behulp van computermodellen van de B4GALT3-structuur. Ze identificeerden myricoside, een plantafgeleid molecuul dat precies in het actieve pocket van het enzym paste. In celtesten maakte myricoside retinoblastoomcellen minder levensvatbaar, verminderde het hun hechting aan fibronectine, verlaagde het de suikerversiering van β1-integrine en dempte het het FAK-overlevingspad, waarmee het genetisch verlies van B4GALT3 werd nagebootst.
Wat dit kan betekenen voor toekomstige behandelingen
Wanneer myricoside direct in de ogen van tumorbevattende muizen werd toegediend, krompen tumoren, verminderden invasieve kenmerken, daalden B4GALT3- en MMP2-signalen, werden barrière-eiwitten hersteld en nam de kankerceldood toe — zonder duidelijke schade aan normale netvlieslagen. Samen schetst het werk een helder beeld: B4GALT3 staat hoog in een keten die retinoblastoomcellen in staat stelt zich vast te grijpen, signalen te geven en zich een weg door de verdedigingen van het oog te banen. Voor niet-specialisten is de kernboodschap dat een suikerbindend enzym, ooit beschouwd als een achtergrondspeler, in feite een sleutelschakelaar is die deze kinderkanker invasiever maakt. Het richten op B4GALT3 met middelen zoals myricoside zou kunnen helpen voorkomen dat tumoren uit het oog uitbreken, en daarmee de kans vergroten dat kinderen zowel hun gezichtsvermogen als hun leven behouden.
Bronvermelding: Tang, J., Li, J., Wang, M. et al. β1,4-galactosyltransferase III drives retinoblastoma invasion via activation of integrin-FAK axis. Cell Death Dis 17, 336 (2026). https://doi.org/10.1038/s41419-026-08620-5
Trefwoorden: retinoblastoom, kankerinvasie, glycosylering, integrinesignalering, gerichte therapie