Clear Sky Science · zh
JAK 抑制剂扰乱代谢授权,限制 CD8 T 细胞激活与效应功能
这些免疫细胞为何与日常健康相关
用于抑制过度活跃免疫反应的药物已经极大改善了类风湿性关节炎及其他自身免疫病患者的生活质量。但许多这类药物——称为 JAK 抑制剂——也会使部分患者更容易感染带状疱疹或结核等病原体。本研究提出了一个简单却重要的问题:这些药物究竟如何影响我们的抗感染 T 细胞,尤其是负责清除被病毒感染细胞的 CD8 T 细胞?
关闭信号的药物
JAK 抑制剂阻断一类将免疫信使分子信号传入细胞内部的酶。该类不同药物针对不同的 JAK 酶,但共同目标是抑制炎症。作者研究了三种广泛使用的 JAK 抑制剂,以及一种阻断相关酶的药物,使用来自健康志愿者的外周血细胞作为模型。他们聚焦于尚未遇到病原体的初始 CD8 T 细胞(naive)和通常对既往遭遇的微生物反应迅速的记忆 CD8 T 细胞。在体外用模拟感染的刺激激活这些细胞时,研究团队加入了临床相关剂量的药物,并测量细胞激活、增殖及装备杀伤功能的能力。
看起来“清醒”但缺乏能量的细胞
乍看之下,药物处理的 CD8 T 细胞仍表现出一些唤醒迹象:它们在表面开启了常见的激活标志。但在内部,它们的行为截然不同。通常,激活的 T 细胞会迅速从环境中摄取葡萄糖,并通过一种高档位的代谢方式燃烧以支持分裂、产生毒性蛋白和产生警报性细胞因子。在存在 JAK 抑制剂时,葡萄糖摄取下降,细胞表面的主要葡萄糖转运蛋白减少,培养基中作为快速糖代谢终产物的乳酸积累变少。即便在那些明显开启了激活标志的细胞中,这种“代谢转换”也无法正常发生。CD4 T 细胞中也观察到类似模式,提示这一效应可能横跨多种 T 细胞类型。
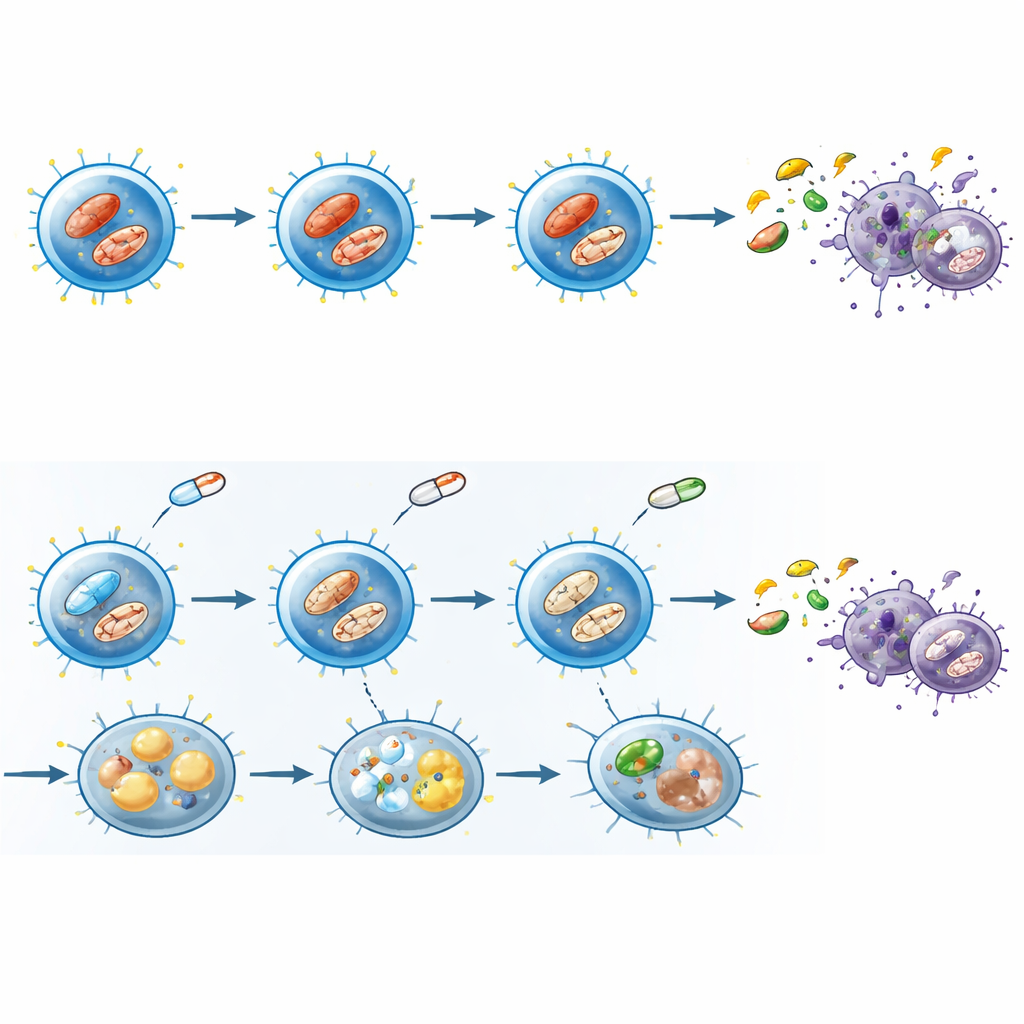
受损的发电厂与累积的脂滴
团队接着检查了细胞的内部发电厂——线粒体。健康且被激活的 T 细胞通常具有许多结构紧凑、膜电位较高的线粒体,这些线粒体既提供能量也发出重要的化学信号。在 JAK 抑制下,强极化线粒体的 CD8 T 细胞减少,线粒体膜电位降低,电子显微镜显示线粒体肿胀、受损,内部皱褶遭到破坏。同时,细胞中累积了脂滴,提示它们更倾向于储存而非高效燃烧脂质。线粒体来源的活性氧(ROS)的测量也随激活状态不同而改变,指向线粒体有益信号与有害信号之间平衡被扰乱。
抑制生长与努力的应激程序
为了解这些变化在基因层面如何连接,研究者对暴露于代表性 JAK 抑制剂的活化记忆 CD8 T 细胞进行了 RNA 测序。与快速糖代谢和氨基酸代谢相关的基因表达下调,而与线粒体呼吸和细胞饥饿相关的程序上调。同时,作为生长与生物合成主控的 mTOR 与 MYC 驱动基因被抑制,而应激反应蛋白 p53 调控的基因则增加。功能学测试证实总体蛋白合成减慢,细胞从依赖葡萄糖转向更多依赖线粒体,尽管线粒体本身已受损。总体而言,这些变化类似衰老样状态:细胞尚未死亡,但代谢受压、迟缓,执行任务的能力下降。
来自临床患者的证据
如果实验室结果无法在真实患者中得到验证,它们可能会误导临床判断。因此研究者检查了服用 JAK 抑制剂的类风湿性关节炎患者的血样,并与服用甲氨蝶呤(一种不同的免疫调节药)患者及健康志愿者进行了比较。温和刺激后,来自 JAK 抑制剂治疗患者的记忆 CD8 T 细胞较少达到完全激活状态,mTOR 通路活性较低,表达与高代谢需求相关的葡萄糖转运蛋白也较少。使用单细胞代谢检测,这些患者细胞显示蛋白质合成减少、对葡萄糖的依赖下降、对线粒体通路的依赖增加,近似重现了体外实验中的模式。
这对感染风险意味着什么
对普通读者来说,核心信息是:JAK 抑制剂不仅降低炎症信号,它们也削弱了关键杀伤性 T 细胞的能量供应和生长能力。药物允许这些细胞呈现外在的“激活制服”,但阻断了让它们奔跑、分裂并有效摧毁被感染靶标所需的代谢授权。这种受限且偏向应激的状态有助于解释为何服用 JAK 抑制剂的人在某些感染面前更为脆弱,并提示未来通过监测或支持 T 细胞代谢可能有助于个体化用药,降低这些风险。
引用: Onofrio, L.I., Abrate, C., Strusberg, I. et al. Disruption of metabolic licensing by JAK inhibitors constrains CD8 T cell activation and effector function. Cell Death Dis 17, 355 (2026). https://doi.org/10.1038/s41419-026-08610-7
关键词: JAK 抑制剂, CD8 T 细胞, 免疫代谢, 自身免疫治疗, 感染风险