Clear Sky Science · sv
Störning av metabolisk licensiering av JAK‑hämmare begränsar CD8‑T‑cellsaktivering och effektorfunktion
Varför dessa immunceller betyder något för vardagshälsan
Läkemedel som dämpar ett överaktivt immunsystem har förändrat livet för personer med reumatoid artrit och andra autoimmuna sjukdomar. Men många av dessa läkemedel, så kallade JAK‑hämmare, gör också att vissa patienter blir mer mottagliga för infektioner som bältros eller tuberkulos. Denna studie ställer en enkel men viktig fråga: vad gör dessa läkemedel egentligen med våra infektionsbekämpande T‑celler, särskilt CD8‑T‑cellerna som jagar virusinfekterade celler?
Läkemedel som stänger av signaler
JAK‑hämmare blockerar en familj enzymer som för signaler från immunsystemets budbärare in i cellerna. Olika läkemedel i denna klass siktar mot olika JAK‑enzymer, men alla syftar till att dämpa inflammation. Forskarna studerade tre mycket använda JAK‑hämmare, plus ett läkemedel som blockerar ett närliggande enzym, med blodceller från friska frivilliga. De fokuserade på naiiva CD8‑T‑celler, som ännu inte stött på en infektion, och minnes‑CD8‑T‑celler, som normalt svarar snabbt på mikrober de tidigare mött. När dessa celler stimulerades i laboratoriet för att efterlikna en infektion tillsatte teamet kliniskt realistiska doser av läkemedlen och mätte hur väl cellerna aktiverades, delade sig och rustade sig för att döda.
Celler som ser vakna ut men saknar energi
Vid en första anblick visade läkemedelsbehandlade CD8‑T‑celler fortfarande vissa tecken på att vakna: de tände vanliga aktiveringsmarkörer på ytan. Men under ytan betedde de sig mycket annorlunda. Normalt importerar en aktiverad T‑cell snabbt socker från omgivningen och använder det genom en högväxlad metabolism för att driva delning och produktion av toxiska proteiner och alarmhöjande cytokiner. Med JAK‑hämmare närvarande minskade glukosupptaget, den huvudsakliga glukostransportören på cellytan var reducerad och mindre laktat — en slutprodukt av snabb sockernedbrytning — ackumulerades i odlingsmedierna. Även bland celler som tydligt slagit på aktiveringsmarkörer inträffade inte detta ”metabola skifte” på rätt sätt. Samma mönster sågs i CD4‑T‑celler, vilket tyder på en bredare effekt över T‑cellstyper.
Ansträngda kraftverk och lagrad fett
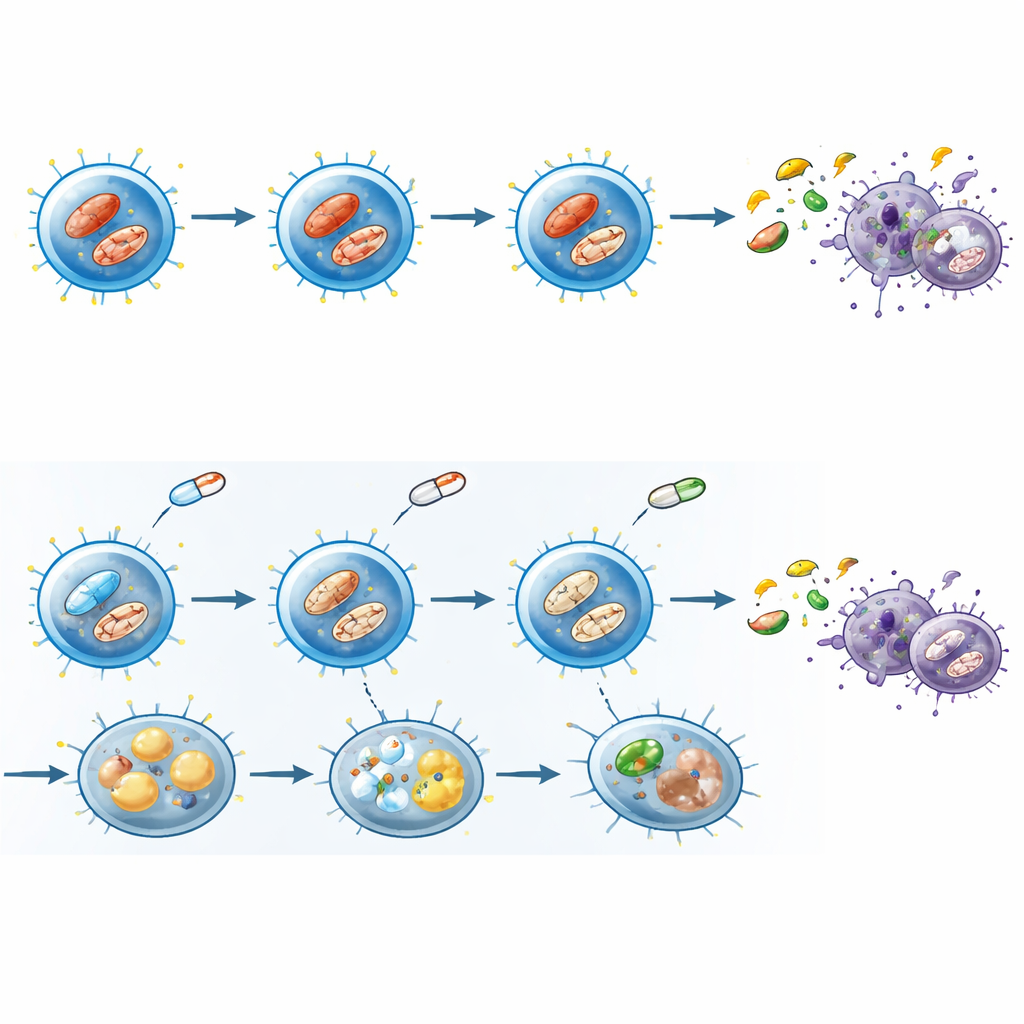
Teamet undersökte sedan cellernas inre kraftverk, mitokondrierna. Friska, aktiverade T‑celler visar vanligtvis många tätt strukturerade, starkt polariserade mitokondrier som hjälper till att förse energi och viktiga kemiska signaler. Vid JAK‑hämning hade färre CD8‑T‑celler starkt polariserade mitokondrier, mitokondriemembranets potential var lägre och detaljerad elektronmikroskopi visade svullna, skadade strukturer med störda inre veck. Samtidigt ackumulerade cellerna fettdroppar, vilket antyder att de lagrade snarare än effektivt förbrände lipider. Mätningar av mitokondrie‑deriverade reaktiva syrearter förändrades också på ett sätt som berodde på om cellerna var aktiverade, vilket pekar på en rubbad balans mellan hjälpsamma och skadliga mitokondriesignaler.
Stressprogram som hämmar tillväxt och ansträngning
För att förstå hur dessa förändringar kopplas på gen‑nivå sekvenserade forskarna RNA från aktiverade minnes‑CD8‑T‑celler exponerade för en representativ JAK‑hämmare. Genaktivitet kopplad till snabb sockeranvändning och aminosyrametabolism nedreglerades, medan program associerade med mitokondrierespiration och cellulär svält uppreglerades. Samtidigt undertrycktes gener som drivs av mTOR och MYC — huvudregulatorer för tillväxt och biosyntes — och gener styrda av stress‑proteinet p53 ökade. Funktionella tester bekräftade att den globala proteinsyntesen bromsades och att cellerna flyttade från att förlita sig på glukos till att i större utsträckning förlita sig på mitokondrier, trots deras komprometterade tillstånd. Sammantaget liknade dessa förändringar ett senescensliknande tillstånd: celler inte döda, men metaboliskt stressade, långsamma och mindre kapabla att utföra sina uppgifter.
Bevis från patienter i kliniken
Laboratorieresultat kan vara missvisande om de inte håller i verkliga människor, så forskarna undersökte blod från patienter med reumatoid artrit som tog JAK‑hämmare och jämförde dem med patienter på metotrexat, ett annat immunmodulerande läkemedel, och med friska frivilliga. Efter mild stimulering var minnes‑CD8‑T‑celler från patienter behandlade med JAK‑hämmare mindre benägna att nå ett fullt aktiverat tillstånd, visade lägre aktivitet i mTOR‑vägen och uttryckte mindre av glukostransportören kopplad till hög metabolisk efterfrågan. Med en enkelcellsmetabolisk analys visade dessa patientceller reducerad proteinsyntes, minskad beroende av glukos och ökat beroende av mitokondriella vägar, vilket nära speglade mönstren som observerats i laboratorieförsöken.
Vad detta betyder för infektionsrisken
För en lekmannaläsare är kärnbudskapet att JAK‑hämmare gör mer än att dämpa inflammatoriska signaler: de skär också av energiförsörjningen och tillväxtkapaciteten hos viktiga cytotoxiska T‑celler. Läkemedlen låter dessa celler ta på sig den yttre ”uniformen” av aktivering, men blockerar den metabola licensiering som gör att de kan röra sig, dela sig och effektivt förinta infekterade mål. Detta begränsade, stresspräglade tillstånd hjälper till att förklara varför personer som tar JAK‑hämmare kan vara mer sårbara för vissa infektioner, och antyder att övervakning eller stöd av T‑cellsmetabolismen en dag kan bidra till att skräddarsy behandlingar och minska dessa risker.
Citering: Onofrio, L.I., Abrate, C., Strusberg, I. et al. Disruption of metabolic licensing by JAK inhibitors constrains CD8 T cell activation and effector function. Cell Death Dis 17, 355 (2026). https://doi.org/10.1038/s41419-026-08610-7
Nyckelord: JAK‑hämmare, CD8‑T‑celler, immunmetabolism, autoimmun terapi, infektionsrisk