Clear Sky Science · de
Störung der metabolischen Freigabe durch JAK-Inhibitoren bremst die Aktivierung und Effektorfunktion von CD8-T-Zellen
Warum diese Immunzellen für die Alltagsgesundheit wichtig sind
Medikamente, die ein überaktives Immunsystem dämpfen, haben das Leben von Menschen mit rheumatoider Arthritis und anderen Autoimmunerkrankungen erheblich verbessert. Viele dieser Mittel, sogenannte JAK-Inhibitoren, erhöhen jedoch bei manchen Patienten die Anfälligkeit für Infektionen wie Gürtelrose oder Tuberkulose. Die Studie stellt eine einfache, aber wichtige Frage: Was genau bewirken diese Medikamente an unseren infektionabwehrenden T-Zellen, insbesondere an den CD8-T-Zellen, die virusinfizierte Zellen aufspüren und zerstören?
Medikamente, die Signale ausschalten
JAK-Inhibitoren blockieren eine Enzymfamilie, die Signale von Botenstoffen des Immunsystems in Zellen weiterleitet. Verschiedene Wirkstoffe dieser Klasse richten sich gegen unterschiedliche JAK-Enzyme, verfolgen aber alle das Ziel, Entzündungen zu reduzieren. Die Autoren untersuchten drei weit verbreitete JAK-Inhibitoren sowie ein Medikament, das ein verwandtes Enzym blockiert, anhand von Blutproben gesunder Freiwilliger. Sie konzentrierten sich auf naive CD8-T-Zellen, die noch keine Infektion gesehen haben, und auf Gedächtnis-CD8-T-Zellen, die normalerweise schnell auf frühere Erreger reagieren. Wurden diese Zellen im Labor zur Imitation einer Infektion stimuliert, fügten die Forscher klinisch realistische Wirkstoffdosen hinzu und maßen, wie gut die Zellen aktiviert wurden, sich vermehrten und sich zum Töten ausrüsteten.
Zellen, die wach aussehen, denen aber die Energie fehlt
Auf den ersten Blick zeigten medikamentenbehandelte CD8-T-Zellen noch einige Anzeichen des Erwachens: Sie setzten gängige Aktivierungsmarker an ihrer Oberfläche. Unter der Oberfläche verhielten sie sich jedoch sehr anders. Normalerweise nimmt eine aktivierte T-Zelle schnell Zucker aus der Umgebung auf und verwertet ihn in einer hochgefahrenen Stoffwechsellage, um Teilung, die Produktion toxischer Proteine und die Freisetzung alarmierender Zytokine zu ermöglichen. In Gegenwart von JAK-Inhibitoren sank die Glukoseaufnahme, der wichtigste Glukosetransporter an der Zelloberfläche war reduziert, und es bildete sich weniger Laktat — ein Endprodukt schnellen Zuckerstoffwechsels — in den Kulturschalen. Selbst unter den Zellen, die klar Aktivierungsmarker zeigten, fand diese „metabolische Umschaltung“ nicht richtig statt. Derselbe Befund zeigte sich auch bei CD4-T-Zellen, was auf einen breiteren Effekt über T-Zell-Typen hinweg hindeutet.
Gestrengte Kraftwerke und gespeicherte Fette
Die Forscher untersuchten anschließend die inneren Kraftwerke der Zellen, die Mitochondrien. Gesunde, aktivierte T-Zellen weisen normalerweise viele eng strukturierte, hochpolarisierte Mitochondrien auf, die Energie und wichtige chemische Signale bereitstellen. Unter JAK-Hemmung hatten weniger CD8-T-Zellen stark polarisierte Mitochondrien, die mitochondriale Membranladung war reduziert, und die Elektronenmikroskopie zeigte geschwollene, beschädigte Strukturen mit gestörten inneren Faltungen. Gleichzeitig häuften die Zellen Fetttropfen an, was darauf hindeutet, dass sie Lipide eher speicherten als effizient verbrannten. Messungen mitochondrienabhängiger reaktiver Sauerstoffspezies veränderten sich ebenfalls in einer Weise, die davon abhängte, ob die Zellen aktiviert waren, und deuteten auf ein gestörtes Gleichgewicht zwischen nützlichen und schädlichen mitochondrialen Signalen hin.
Stressprogramme, die Wachstum und Einsatz bremsen
Um zu verstehen, wie diese Veränderungen genetisch verankert sind, sequenzierten die Forschenden RNA aus aktivierten Gedächtnis-CD8-T-Zellen, die einem repräsentativen JAK-Inhibitor ausgesetzt waren. Gene, die mit schnellem Zuckerstoffwechsel und Aminosäuremetabolismus verknüpft sind, wurden herunterreguliert, während Programme, die mit mitochondrialer Atmung und zellulärem Hungern einhergehen, hochgefahren wurden. Gleichzeitig waren Gene, die von mTOR und MYC — zentralen Steuerern von Wachstum und Biosynthese — angetrieben werden, unterdrückt, und Gene, die durch das Stressantwortprotein p53 gesteuert werden, waren erhöht. Funktionelle Tests bestätigten, dass die globale Proteinsynthese verlangsamte und die Zellen sich weg von der Glukoseabhängigkeit und hin zu einer stärkeren Nutzung mitochondrieller Wege verlagerten, trotz ihres beeinträchtigten Zustands. Insgesamt ähnelten diese Veränderungen einem seneszenzähnlichen Zustand: die Zellen waren nicht tot, aber metabolisch gestresst, träge und weniger leistungsfähig.
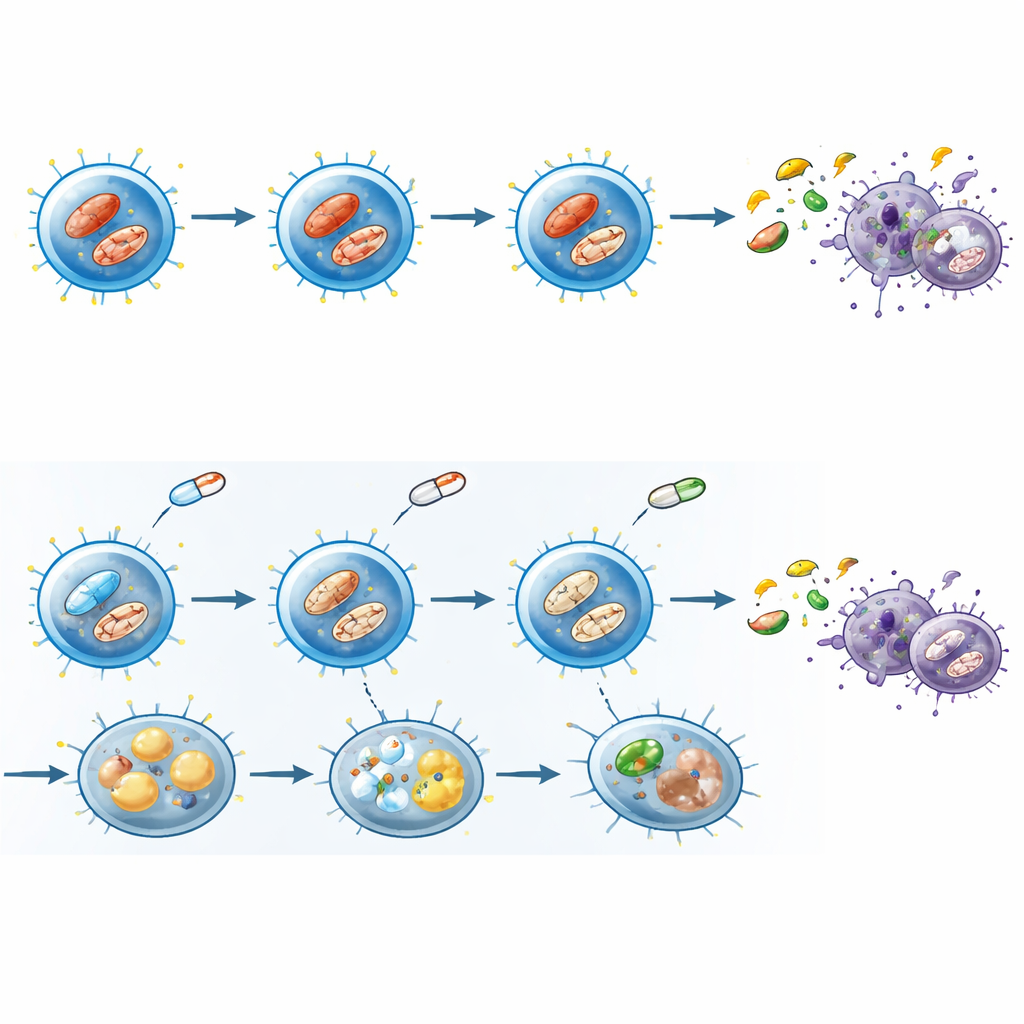
Hinweise aus Patientenproben
Laborergebnisse können irreführend sein, wenn sie sich nicht im Menschen bestätigen, daher untersuchten die Forscher Blutproben von Patienten mit rheumatoider Arthritis, die JAK-Inhibitoren einnahmen, und verglichen diese mit Patienten unter Methotrexat, einem anderen immunmodulierenden Medikament, sowie mit gesunden Freiwilligen. Nach milder Stimulation erreichten Gedächtnis-CD8-T-Zellen aus JAK-Inhibitor-therapierten Patienten seltener einen vollständig aktivierten Zustand, zeigten eine geringere mTOR-Aktivität und exprimierten weniger des Glukosetransporters, der mit hohem metabolischem Bedarf assoziiert ist. Mithilfe eines Einzelzellstoffwechseltests zeigten diese Patienten-Zellen reduzierte Proteinsynthese, verringerte Glukoseabhängigkeit und eine vermehrte Nutzung mitochondrialer Wege, was die im Labor beobachteten Muster eng widerspiegelte.
Was das für das Infektionsrisiko bedeutet
Für Nichtfachleute lautet die Kernbotschaft: JAK-Inhibitoren dimmen nicht nur Entzündungssignale, sie kappen auch die Energiezufuhr und die Wachstumskapazität von wichtigen Killer-T-Zellen. Die Medikamente erlauben diesen Zellen, die äußere "Uniform" der Aktivierung anzulegen, blockieren jedoch die metabolische Freigabe, die ihnen das Rennen, die Teilung und das effektive Zerstören infizierter Zielzellen ermöglicht. Dieser eingeschränkte, stressbetonte Zustand erklärt zum Teil, warum Menschen unter JAK-Inhibitoren anfälliger für bestimmte Infektionen sind, und legt nahe, dass das Überwachen oder Unterstützen des T-Zell-Stoffwechsels künftig helfen könnte, die Behandlung zu individualisieren und solche Risiken zu reduzieren.
Zitation: Onofrio, L.I., Abrate, C., Strusberg, I. et al. Disruption of metabolic licensing by JAK inhibitors constrains CD8 T cell activation and effector function. Cell Death Dis 17, 355 (2026). https://doi.org/10.1038/s41419-026-08610-7
Schlüsselwörter: JAK-Inhibitoren, CD8-T-Zellen, Immunstoffwechsel, Therapie bei Autoimmunerkrankungen, Infektionsrisiko