Clear Sky Science · nl
Verstoring van metabole permissie door JAK-remmers beperkt CD8-T-celactivatie en effectorfunctie
Waarom deze immuuncellen van belang zijn voor alledaagse gezondheid
Geneesmiddelen die een overactief immuunsysteem kalmeren, hebben het leven voor mensen met reumatoïde artritis en andere auto-immuunziekten ingrijpend veranderd. Maar veel van deze middelen, aangeduid als JAK-remmers, maken sommige patiënten ook vatbaarder voor infecties zoals gordelroos of tuberculose. Deze studie stelt een eenvoudige maar belangrijke vraag: wat doen deze geneesmiddelen precies met onze infectiebestrijdende T-cellen, en in het bijzonder de CD8-T-cellen die geïnfecteerde cellen opsporen en doden?
Geneesmiddelen die signalen uitschakelen
JAK-remmers blokkeren een familie enzymen die signalen van immuunsysteem-boodschappers binnen de cel doorgeven. Verschillende middelen in deze klasse richten zich op verschillende JAK-enzymen, maar allemaal hebben ze tot doel ontsteking terug te schroeven. De auteurs bestudeerden drie veelgebruikte JAK-remmers, plus één middel dat een gerelateerd enzym blokkeert, met behulp van bloedcellen van gezonde vrijwilligers. Ze concentreerden zich op naïeve CD8-T-cellen, die nog geen infectie hebben gezien, en op geheugen-CD8-T-cellen, die normaal gesproken snel reageren op eerder ontmoet microben. Wanneer deze cellen in het laboratorium werden gestimuleerd om een infectie na te bootsen, voegde het team klinisch realistische doses van de medicijnen toe en mat hoe goed de cellen werden geactiveerd, zich vermenigvuldigden en bewapenden om te doden.
Cellen die wakker lijken maar energie missen
Op het eerste gezicht toonden door geneesmiddelen behandelde CD8-T-cellen nog steeds enkele tekenen van ontwaken: ze zetten veelvoorkomende activeringsmarkeringen op hun oppervlak aan. Maar onder de motorkap gedroegen ze zich heel anders. Normaal neemt een geactiveerde T-cel snel suiker op uit haar omgeving en verbrandt die via een hoog-vermogen metabolisme om deling en de productie van toxische eiwitten en alarmserende cytokinen aan te drijven. In aanwezigheid van JAK-remmers daalde de glucoseopname, nam de belangrijkste glucose-transporter op het celoppervlak af, en bouwde zich minder lactaat op—een eindproduct van snelle suikerverbranding—in de kweekvloeistof. Zelfs onder de cellen die duidelijk activeringsmarkers aanzetten, trad deze “metabole verschuiving” niet goed op. Hetzelfde patroon verscheen in CD4-T-cellen, wat wijst op een bredere impact over T-celtypen heen.
Belaste energiecentrales en opgeslagen vet
Het team onderzocht vervolgens de interne energiecentrales van de cellen, de mitochondriën. Gezonde, geactiveerde T-cellen vertonen doorgaans veel strak gestructureerde, hooggepolariseerde mitochondriën die energie en belangrijke chemische signalen leveren. Onder JAK-remming hadden minder CD8-T-cellen sterk gepolariseerde mitochondriën, was de mitochondriale membraanpotentiaal lager, en onthulde detail-elektronenmicroscopie gezwollen, beschadigde structuren met verstoorde interne vouwen. Tegelijkertijd stapelden de cellen vetdruppels op, wat suggereert dat ze vetten opslaan in plaats van die efficiënt te verbranden. Metingen van mitochondriale reactieve zuurstofsoorten verschoven ook op een manier die afhankelijk was van de activatiestatus van de cellen, wat wijst op een verstoorde balans tussen behulpzame en schadelijke mitochondriale signalen.
Stressprogramma's die groei en inzet afremmen
Om te begrijpen hoe deze veranderingen op genetisch niveau zijn gekoppeld, sekwenceerden de onderzoekers RNA van geactiveerde geheugen-CD8-T-cellen die werden blootgesteld aan een representatieve JAK-remmer. Genactiviteit gekoppeld aan snelle suikerverwerking en aminozuurmetabolisme werd teruggeschroefd, terwijl programma’s die samenhangen met mitochondriale ademhaling en cellulaire hongertoestanden werden opgevoerd. Tegelijkertijd werden genen aangedreven door mTOR en MYC—meesterregelaars van groei en biosynthese—onderdrukt, en namen genen gereguleerd door het stress-responseiwit p53 toe. Functionele tests bevestigden dat de algehele eiwitsynthese vertraagde en dat cellen verschoven van afhankelijkheid van glucose naar een grotere afhankelijkheid van mitochondriën, ondanks hun aangetaste staat. Alles bij elkaar leken deze veranderingen op een senescentieachtig stadium: cellen die niet dood zijn, maar metabool gestrest, traag en minder goed in staat hun taken uit te voeren.
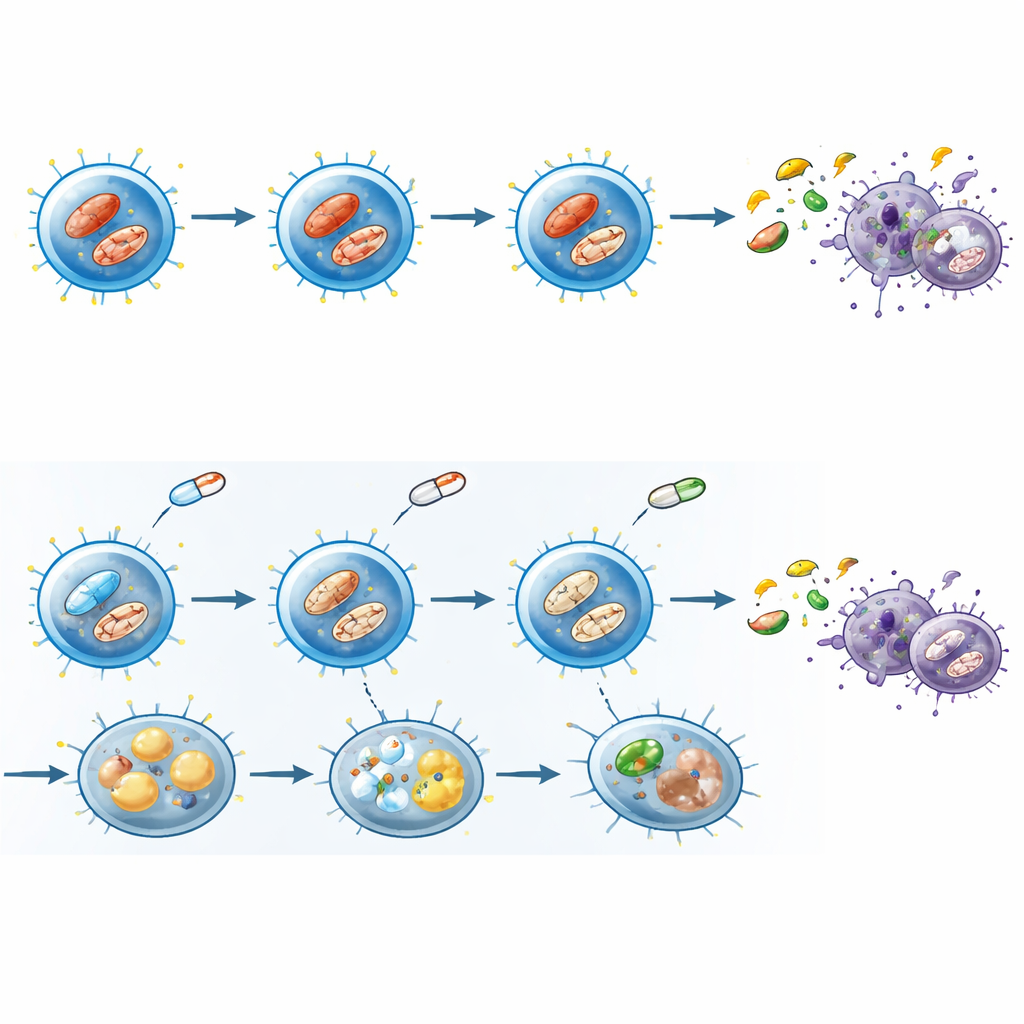
Bewijs uit patiënten in de kliniek
Laboratoriumresultaten kunnen misleidend zijn als ze niet ook bij echte mensen opgaan, dus onderzochten de onderzoekers bloed van patiënten met reumatoïde artritis die JAK-remmers gebruikten en vergeleken die met patiënten op methotrexaat, een ander immuunmodulerend middel, en met gezonde vrijwilligers. Na milde stimulatie bereikten geheugen-CD8-T-cellen van JAK-remmer-behandelde patiënten minder vaak een volledig geactiveerde toestand, toonden ze een lagere activiteit van het mTOR-pad en brachten ze minder van de glucose-transporter tot expressie die geassocieerd is met hoge metabole vraag. Met een enkelcel-metabool assay lieten deze patiëntcellen verminderde eiwitsynthese, afgenomen afhankelijkheid van glucose en verhoogde reliance op mitochondriale paden zien, wat de patronen in de laboratoriumexperimenten nauwkeurig weerspiegelde.
Wat dit betekent voor infectierisico
Voor de leek is de kernboodschap dat JAK-remmers meer doen dan alleen ontstekingssignalen dempen: ze snijden ook in de energievoorziening en groeicapaciteit van belangrijke dodelijke T-cellen. De middelen laten deze cellen wel het uiterlijke “uniform” van activatie aantrekken, maar blokkeren de metabole permissie die hen in staat stelt te rennen, te delen en geïnfecteerde doelwitten effectief te vernietigen. Deze beperkte, stress-gevoelige staat helpt verklaren waarom mensen die JAK-remmers gebruiken vatbaarder kunnen zijn voor bepaalde infecties, en suggereert dat het monitoren of ondersteunen van T-celmetabolisme op termijn behandelingen zou kunnen helpen afstemmen en die risico’s verminderen.
Bronvermelding: Onofrio, L.I., Abrate, C., Strusberg, I. et al. Disruption of metabolic licensing by JAK inhibitors constrains CD8 T cell activation and effector function. Cell Death Dis 17, 355 (2026). https://doi.org/10.1038/s41419-026-08610-7
Trefwoorden: JAK-remmers, CD8 T-cellen, immuunmetabolisme, auto-immuuntherapie, infectierisico