Clear Sky Science · zh
NAT10介导的ac4C RNA乙酰化通过稳定CXCL5/DEK mRNA促进肺腺癌的增殖和转移
这项研究对肺癌患者为何重要
肺腺癌是最常见的肺癌类型,尽管有现代药物,许多患者仍面临疾病早期扩散的问题。本研究揭示了癌细胞内部的一层被忽视的调控:RNA上的微小化学标记,这些分子承载遗传信息。通过展示一种酶如何帮助肺肿瘤生长并在体内迁移,研究指向了一类新的药物靶点,未来可能减缓或阻止转移。
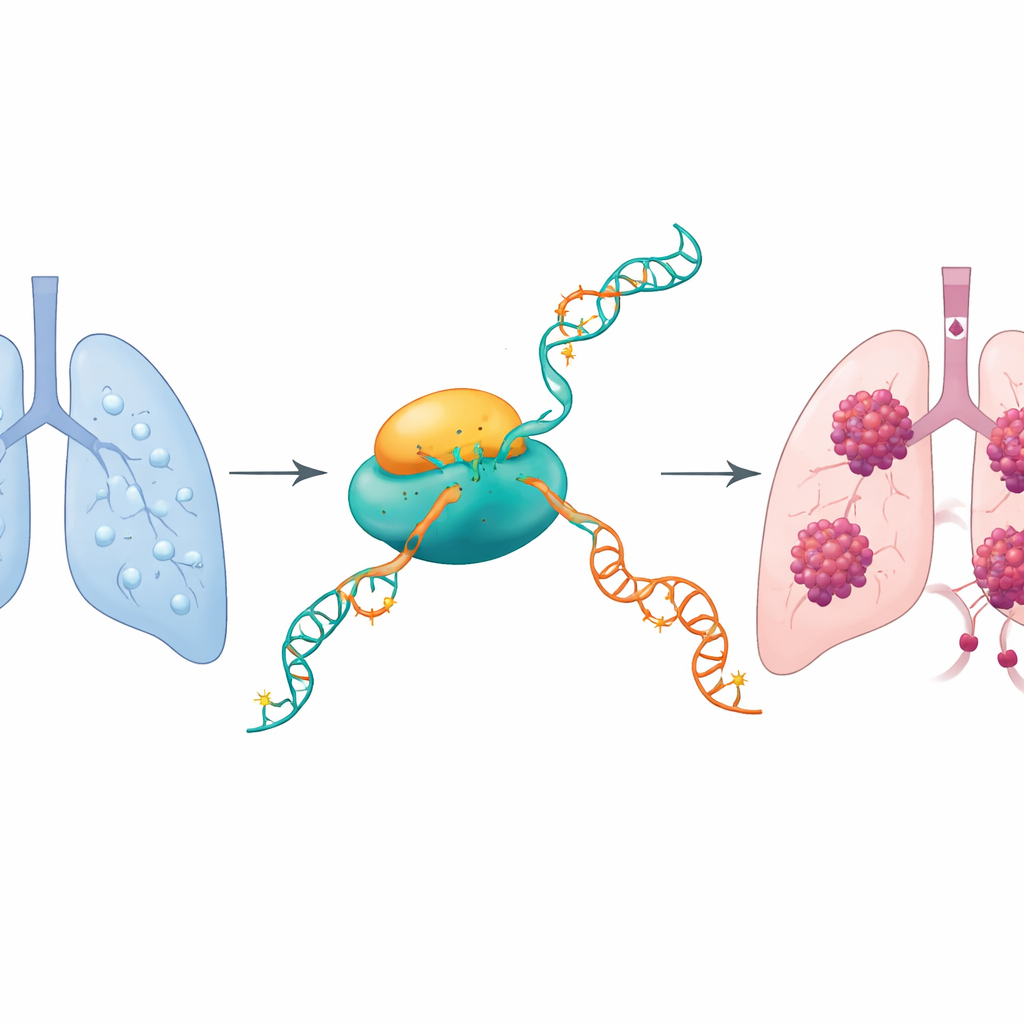
细胞信息上的化学开关
我们的细胞持续读取DNA并将其复制为指示细胞合成何种蛋白的RNA信息。作者关注RNA上的一种微妙化学修饰——N4-乙酰胞苷(ac4C)。已知只有一种酶,NAT10,能添加这种标记。其他肿瘤研究提示NAT10会使肿瘤细胞更具侵袭性。本研究探讨NAT10是否在肺腺癌中发挥类似作用,以及它具体改变哪些RNA信息以驱动肿瘤生长和扩散。
肺肿瘤中NAT10表达上调
研究团队利用大规模公共癌症数据库和患者样本发现,肺腺癌组织中NAT10水平明显高于邻近正常肺组织。随着肿瘤进展到更晚期,其活性上升,且肿瘤中NAT10含量较高的患者生存期倾向于更短。在患者样本和肺癌细胞系中,RNA上的总体ac4C标记与NAT10同时升高,提示该酶在整体上重编程了癌细胞处理遗传信息的方式。
寻找NAT10保护的关键信息
为观察去除NAT10的后果,科学家在A549肺癌细胞中使用CRISPR–Cas9基因编辑敲除NAT10。随后他们结合了两种全局方法:RNA测序以衡量基因表达变化,以及acRIP-seq以绘制RNA上ac4C标记的分布。数百个基因在NAT10被删除后既丧失了表达又失去了ac4C标记,其中许多与细胞黏附和迁移——转移的核心过程——相关。两个突出基因是CXCL5,一种吸引并调控免疫细胞的信号因子,以及DEK,一种帮助组织DNA并在多种癌症中影响肿瘤行为的蛋白。
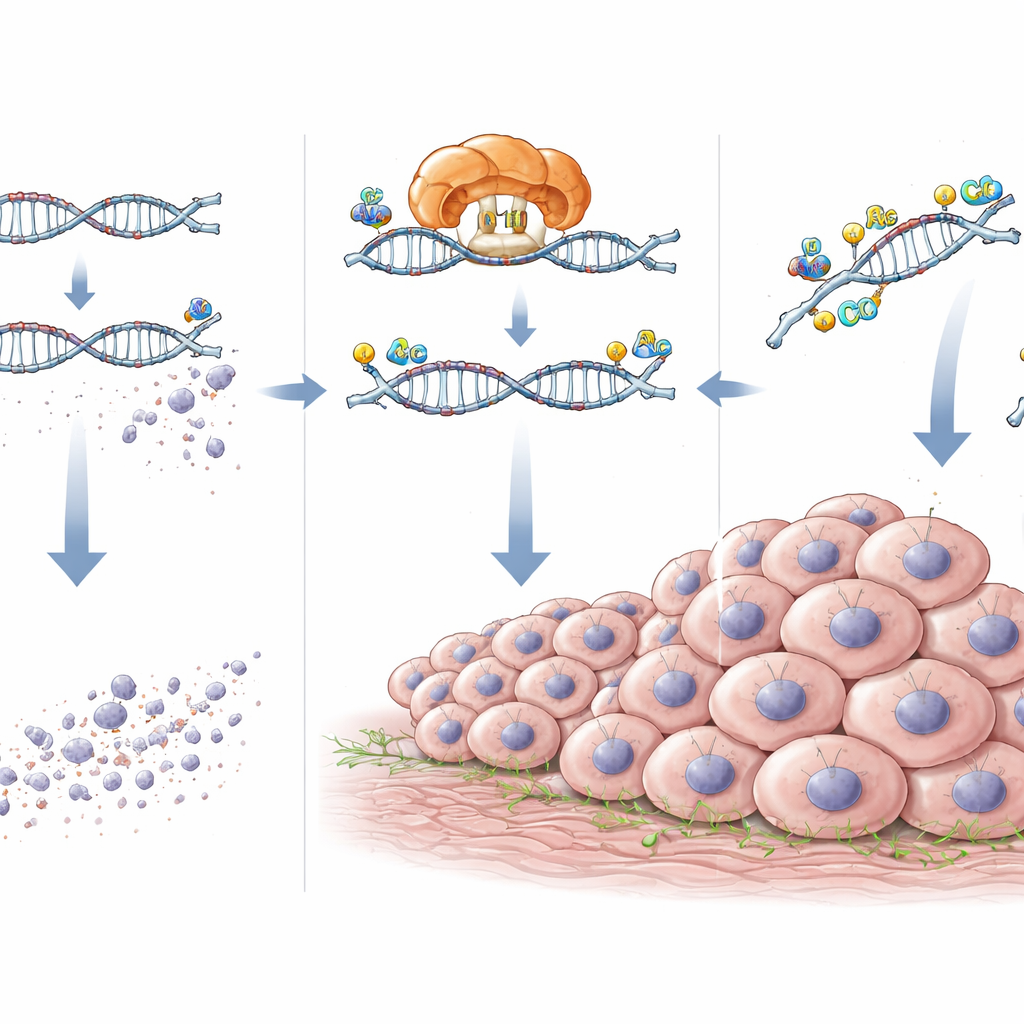
NAT10如何保持促瘤RNA的稳定
深入研究中,团队绘制了CXCL5和DEK RNA上的具体ac4C位点,并证实这些位点依赖于NAT10。当敲低NAT10时,这些化学标记以及CXCL5和DEK的RNA和蛋白水平均下降。报告基因实验中精确突变这些ac4C位点表明,失去这些位点会使RNA对NAT10的响应减弱。RNA降解测定显示,没有NAT10时,CXCL5和DEK的信息更快被分解。换言之,NAT10像一种保护涂层,通过添加ac4C标记使这些RNA在细胞内更持久。
从更强的附着到更快的扩散
这些分子层面的改变对癌细胞行为意味何在?在培养皿中,缺乏NAT10的肺癌细胞增殖更慢,迁移和侵袭能力下降,与组织支架不同成分(如胶原蛋白和纤维连接蛋白)的粘附力也减弱。它们的肌动蛋白纤维骨架变得更紧凑,反映出运动性降低。重新引入CXCL5或DEK,尤其是两者共同补充,可部分恢复细胞的增殖、运动和粘附能力,表明这两种受NAT10控制的基因是促成侵袭性特征的主要驱动因子。在通过尾静脉注射肺癌细胞的老鼠模型中,缺失NAT10的细胞在肺内形成的转移灶显著减少,动物体重增加更多、肿瘤负担也低于注射正常癌细胞的对照组。
对未来治疗的意义
综合这些结果,作者提出了一个简单模型:在肺腺癌中,NAT10将ac4C标记加到CXCL5和DEK的RNA上,使其稳定并高表达。升高的CXCL5和DEK随后增强肿瘤细胞的黏附力、增殖能力和远处转移的便捷性。因此阻断NAT10或其添加ac4C标记的能力,可能使这些促转移的信息失稳,从而削弱肿瘤的粘附与生长。尽管在将该策略用于患者之前仍需更多研究,这项研究突出了RNA乙酰化——尤其是NAT10——作为诊断、预后判断和最终治疗肺腺癌的有前景的新靶点。
引用: Hu, X., Feng, M., Qi, C. et al. NAT10-mediated ac4C RNA acetylation stabilizes CXCL5/DEK mRNA to drive proliferation and metastasis in lung adenocarcinoma. Cell Death Dis 17, 326 (2026). https://doi.org/10.1038/s41419-026-08568-6
关键词: 肺腺癌, RNA乙酰化, NAT10, 转移, CXCL5 DEK