Clear Sky Science · sv
NAT10-medierad ac4C-RNA-acetylering stabiliserar CXCL5/DEK-mRNA för att driva proliferation och metastas i lungadenokarcinom
Varför denna forskning är viktig för personer med lungcancer
Lungadenokarcinom är den vanligaste formen av lungcancer, och även med moderna läkemedel drabbas många patienter fortfarande av tidig spridning av sin sjukdom. Denna studie blottlägger ett dolt kontrolllager inne i cancercellerna: små kemiska märkningar på RNA, molekylerna som bär de genetiska budskapen. Genom att visa hur ett enzym hjälper lungtumörer att växa och sprida sig i kroppen pekar arbetet ut en ny typ av läkemedelsmål som en dag skulle kunna bromsa eller stoppa metastasering.
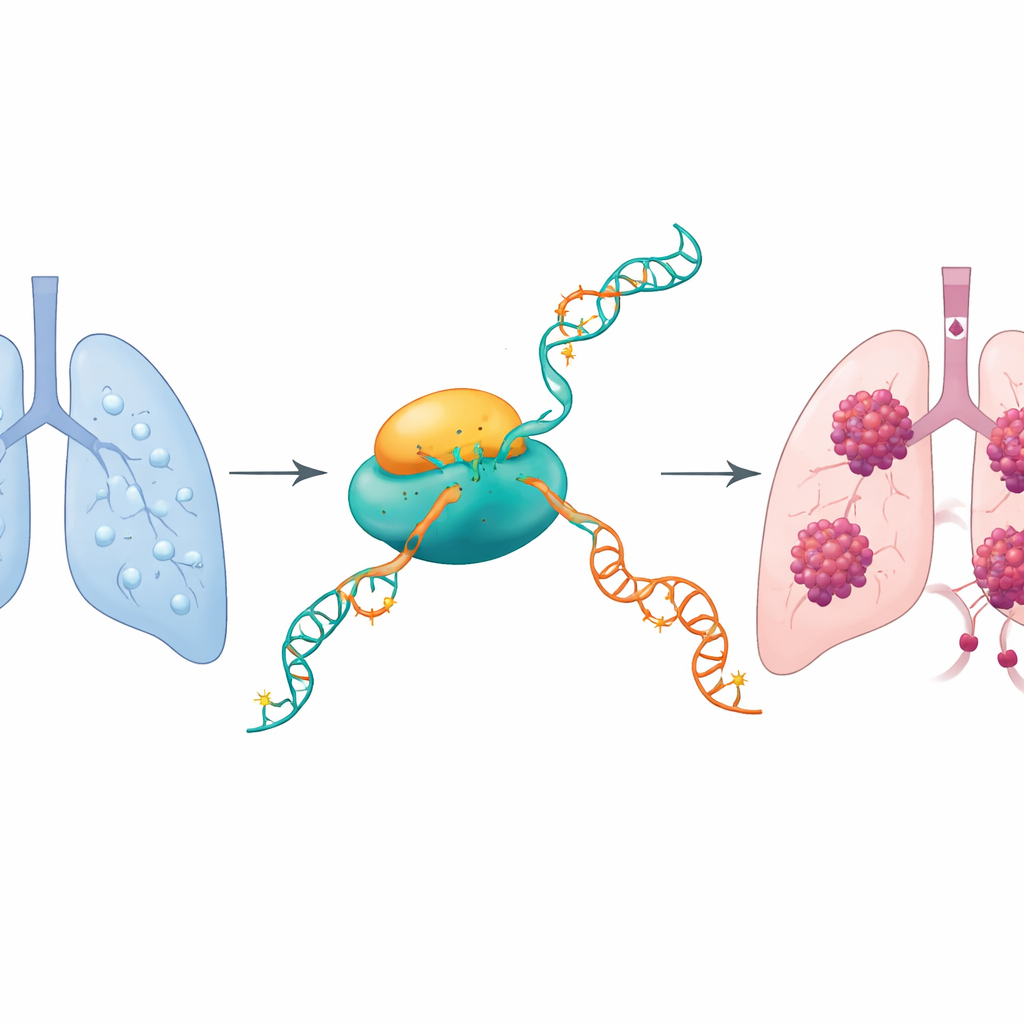
En kemisk strömbrytare på cellens budskap
Våra celler läser ständigt av DNA och kopierar det till RNA-budskap som berättar vilka proteiner cellen ska tillverka. Författarna fokuserade på en subtil kemisk markering på RNA som kallas N4-acetylcytidin (ac4C). Endast ett känt enzym, NAT10, kan lägga dit denna markering. Tidigare studier i andra cancerformer antydde att NAT10 gör tumörceller mer aggressiva. Här frågade forskarna om NAT10 spelar en liknande roll i lungadenokarcinom och, i så fall, vilka specifika RNA-budskap det ändrar för att driva tumörtillväxt och spridning.
NAT10 är uppreglerat i lungtumörer
Genom att använda stora offentliga cancer-databaser och patientprover fann teamet att NAT10-nivåerna är mycket högre i lungadenokarcinomvävnad än i närliggande normal lunga. Dess aktivitet ökar i takt med att tumörer utvecklas till mer avancerade stadium, och patienter vars tumörer har mer NAT10 tenderar att ha kortare överlevnad. I både patientprover och lungcancercellinjer var de totala ac4C-markeringarna på RNA förhöjda tillsammans med NAT10, vilket antyder att detta enzym i stort omprogrammerar hur cancerceller hanterar sina genetiska budskap.
Att hitta de nyckelbudskap som NAT10 skyddar
För att se vad som händer när NAT10 tas bort använde forskarna CRISPR–Cas9-genredigering för att slå ut NAT10 i A549-lungcancerceller. De kombinerade sedan två globala angreppssätt: RNA-sekvensering för att mäta vilka gener som ändrade aktivitet, och acRIP-seq för att kartlägga var ac4C-markeringar förekom på RNA. Hundratals gener förlorade både uttryck och ac4C-markeringar efter att NAT10 raderats, och många av dessa kopplades till hur celler fäster vid sin omgivning och migrerar — processer som är centrala för metastasering. Två framträdande var CXCL5, en signalfaktor som attraherar och formar immunceller, och DEK, ett protein som hjälper organisera DNA och påverkar tumörbeteende i flera cancerformer.
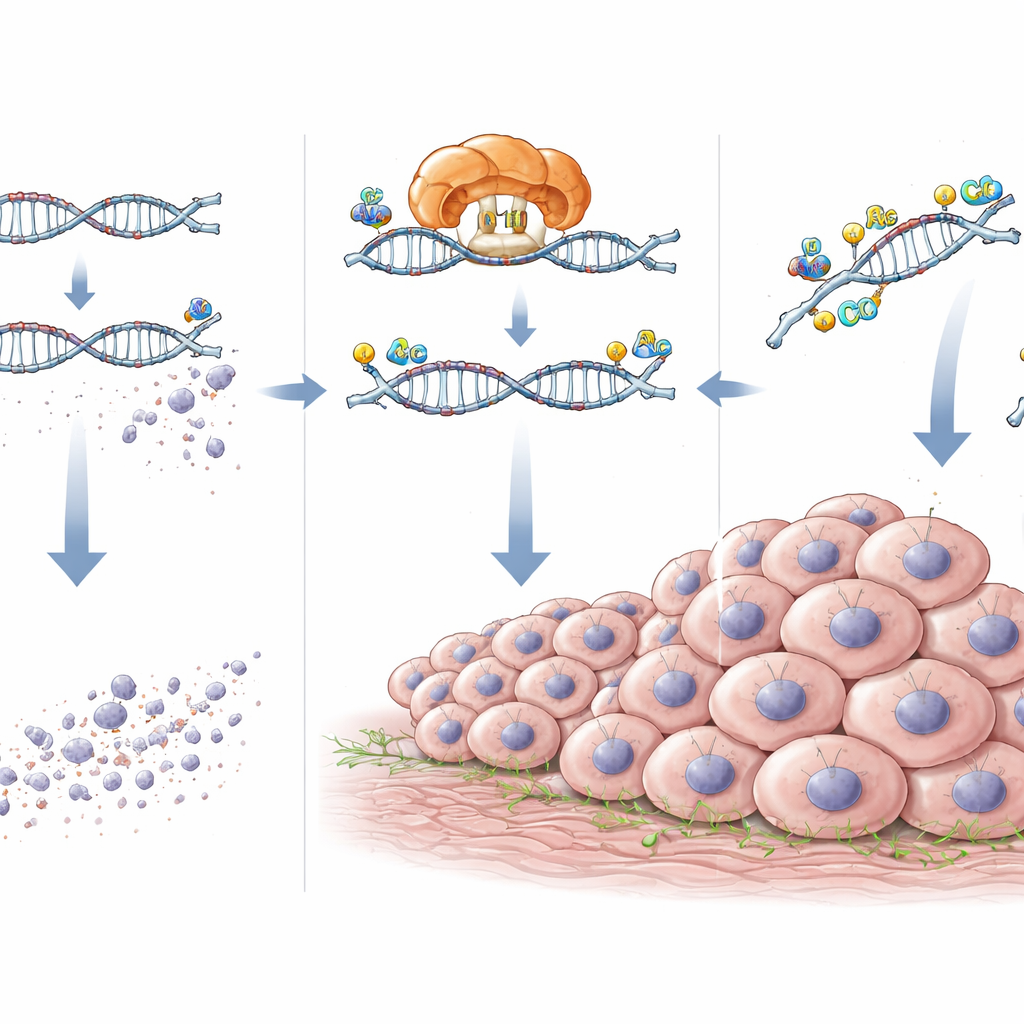
Hur NAT10 håller tumörfrämjande RNA vid liv
Genom att gå djupare kartlade teamet specifika ac4C-ställen på RNA för CXCL5 och DEK och bekräftade att de var beroende av NAT10. När NAT10 slogs ner sjönk både dessa kemiska markeringar och nivåerna av CXCL5- och DEK-RNA samt motsvarande proteiner. Reporterexperiment, där ac4C-ställena exakt muterades, visade att förlust av dessa platser gjorde RNA mindre responsiva på NAT10. Mätningar av RNA-nedbrytning visade att utan NAT10 bröts CXCL5- och DEK-budskapen ned snabbare. Med andra ord fungerar NAT10 som ett skyddande skikt som sätter ac4C-markeringar som stabiliserar dessa RNA så att de kvarstår längre i cellen.
Från starkare fäste till snabbare spridning
Vad betyder dessa molekylära justeringar för cancercellernas beteende? I odlingsskålar växte lungcancerceller utan NAT10 långsammare, migrerade och invaderade mindre, och fäste sig mindre stabilt vid olika komponenter i vävnadens stödstruktur, såsom kollagen och fibronectin. Deras interna skelett av aktinfilament blev också mer kompakt, vilket speglar minskad rörlighet. Att återintroducera CXCL5 eller DEK, och särskilt båda tillsammans, återställde delvis cellernas förmåga att proliferera, röra sig och fästa, vilket visar att dessa två NAT10-styrda gener är huvuddrivkrafter för de aggressiva egenskaperna. I möss som injicerades med lungcancerceller via svansvenen bildade NAT10-defekta celler mycket färre metastatiska fläckar i lungorna, och djuren gick upp mer i vikt och bar en lägre tumörbörda än de som injicerats med normala cancerceller.
Vad detta betyder för framtida behandlingar
Genom att lägga ihop dessa fynd föreslår författarna en enkel modell: i lungadenokarcinom lägger NAT10 till ac4C-markeringar på RNA-budskapen för CXCL5 och DEK, vilket håller dem stabila och högt uttryckta. Förhöjda nivåer av CXCL5 och DEK ökar då hur tätt tumörceller fäster, hur lätt de växer och hur enkelt de sprider sig till avlägsna platser. Att blockera NAT10 eller dess förmåga att sätta ac4C-markeringar skulle därför kunna destabilisera dessa pro-metastatiska budskap och försvaga tumörens fäste och tillväxt. Även om mer arbete krävs innan denna strategi kan testas på patienter, lyfter studien fram RNA-acetylering — och NAT10 i synnerhet — som ett lovande nytt grepp för att diagnostisera, förutsäga och i slutändan behandla lungadenokarcinom.
Citering: Hu, X., Feng, M., Qi, C. et al. NAT10-mediated ac4C RNA acetylation stabilizes CXCL5/DEK mRNA to drive proliferation and metastasis in lung adenocarcinoma. Cell Death Dis 17, 326 (2026). https://doi.org/10.1038/s41419-026-08568-6
Nyckelord: lungadenokarcinom, RNA-acetylering, NAT10, metastas, CXCL5 DEK