Clear Sky Science · nl
NAT10-gemedieerde ac4C-RNA-acetylatie stabiliseert CXCL5/DEK-mRNA om proliferatie en metastase bij longadenocarcinoom te stimuleren
Waarom dit onderzoek belangrijk is voor mensen met longkanker
Longadenocarcinoom is de meest voorkomende vorm van longkanker, en zelfs met moderne medicijnen krijgen veel patiënten nog steeds vroegtijdige uitzaaiingen. Deze studie onthult een verborgen regellaag in kankercellen: kleine chemische markeringen op RNA, de moleculen die genetische boodschappen overdragen. Door te laten zien hoe één enzym longtumoren helpt groeien en zich door het lichaam te verspreiden, wijst het werk op een nieuw soort medicijndoelwit dat mogelijk ooit metastase kan vertragen of stoppen.
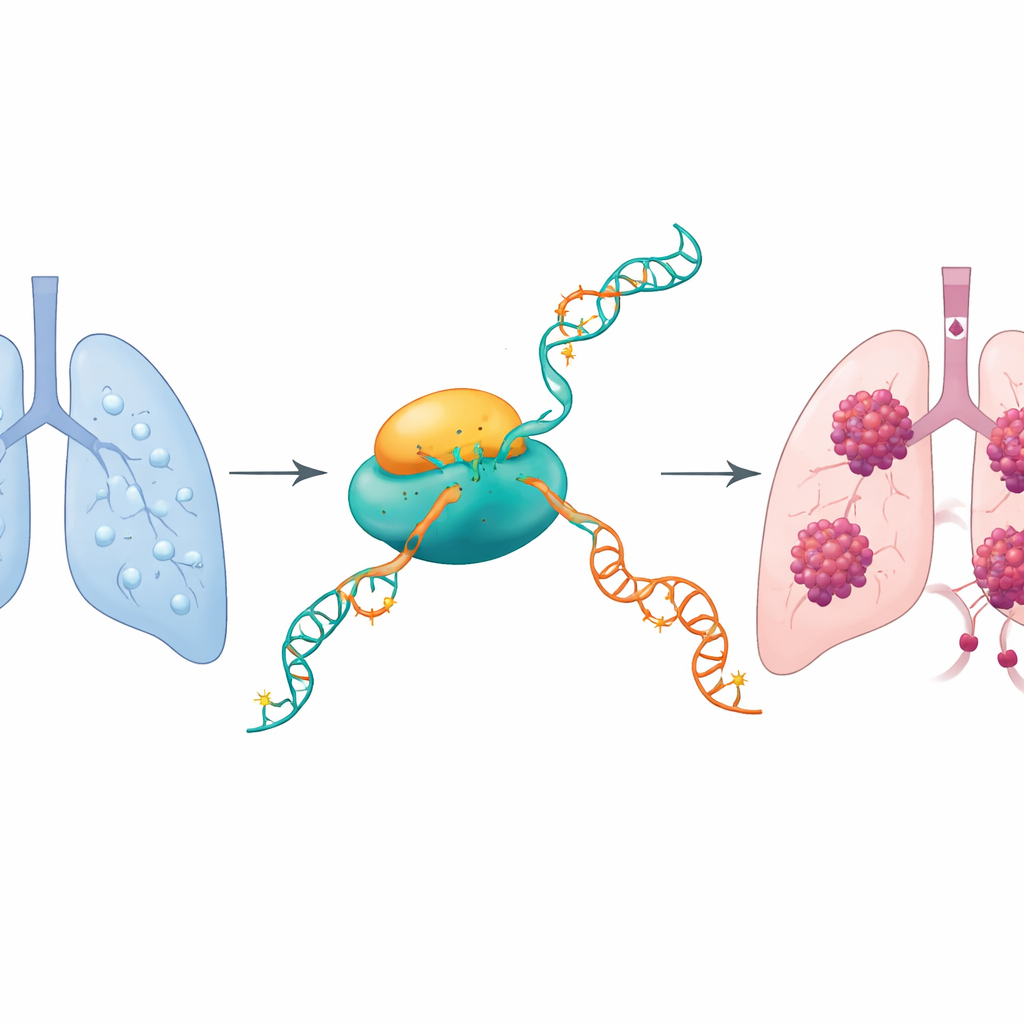
Een chemische schakelaar op de boodschappen van de cel
Onze cellen lezen voortdurend DNA en kopiëren het naar RNA-boodschappen die de cel vertellen welke eiwitten moeten worden gemaakt. De auteurs concentreerden zich op een subtiele chemische markering op RNA genaamd N4-acetylcytidine (ac4C). Slechts één bekend enzym, NAT10, kan deze markering toevoegen. Vorig onderzoek in andere kankers suggereerde dat NAT10 tumorcellen agressiever maakt. Hier onderzochten de onderzoekers of NAT10 een vergelijkbare rol speelt bij longadenocarcinoom en, zo ja, welke specifieke RNA-boodschappen het verandert om tumor groei en verspreiding aan te sturen.
NAT10 is verhoogd in longtumoren
Met behulp van grote openbare kankerdatabases en patiëntmonsters vond het team dat NAT10-niveaus veel hoger zijn in longadenocarcinoomweefsel dan in aangrenzend normaal longweefsel. De activiteit neemt toe naarmate tumoren in meer gevorderde stadia komen, en patiënten waarvan de tumoren meer NAT10 bevatten hebben doorgaans een kortere overleving. In zowel patiëntextracten als longkankercellijnen waren de algemene ac4C-markeringen op RNA verhoogd samen met NAT10, wat suggereert dat dit enzym in brede zin herbedrading van de verwerking van genetische boodschappen in kankercellen veroorzaakt.
De sleutelboodschappen vinden die NAT10 beschermt
Om te zien wat er gebeurt als NAT10 wordt verwijderd, gebruikten de wetenschappers CRISPR–Cas9-genbewerking om NAT10 uit te schakelen in A549-longkankercellen. Zij combineerden vervolgens twee globale benaderingen: RNA-sequencing om te meten welke genen in activiteit veranderden, en acRIP-seq om in kaart te brengen waar ac4C-markeringen op RNA verschenen. Honderden genen verloren zowel expressie als ac4C-markeringen nadat NAT10 was verwijderd, en veel daarvan waren gekoppeld aan hoe cellen zich hechten aan hun omgeving en migreren — processen die centraal staan bij metastase. Twee opvallende voorbeelden waren CXCL5, een signaalmolecuul dat immuuncellen aantrekt en vormt, en DEK, een eiwit dat helpt bij de organisatie van DNA en het gedrag van tumoren in verschillende kankers beïnvloedt.
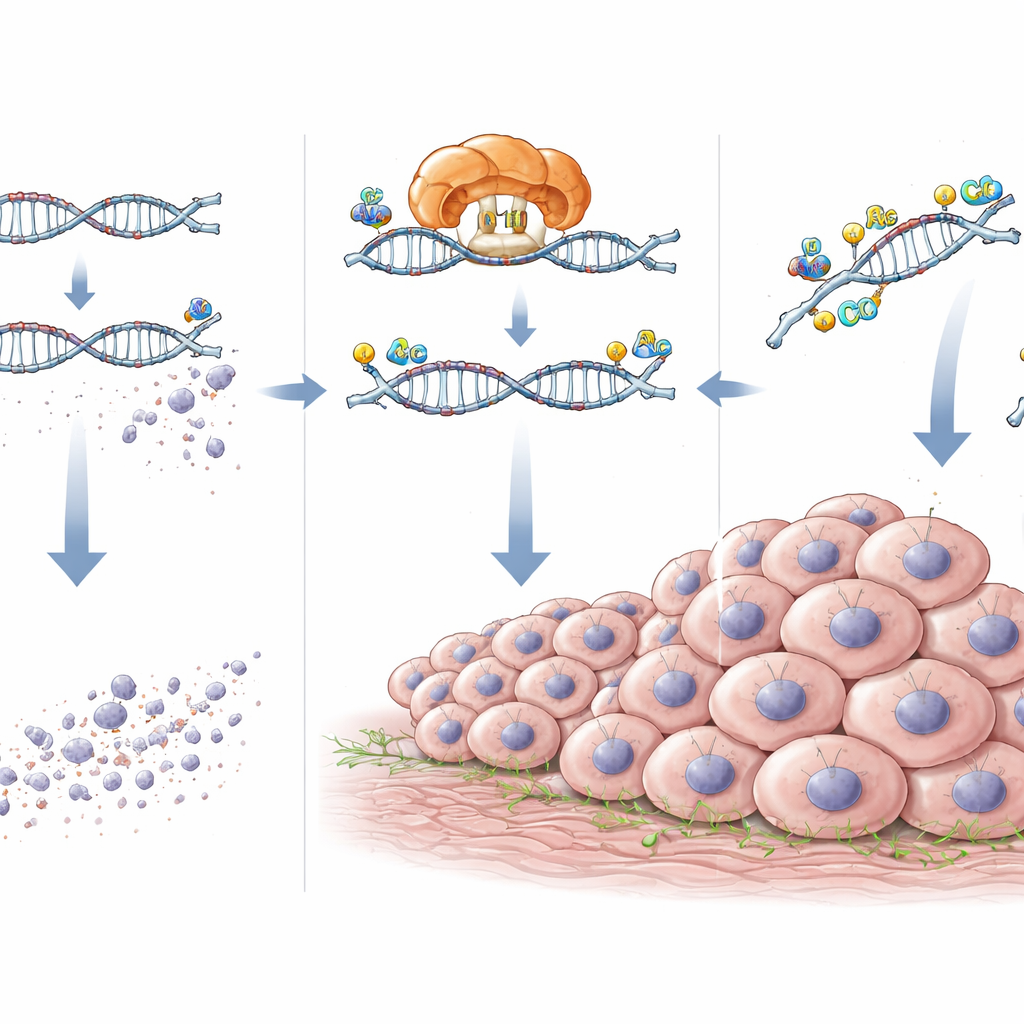
Hoe NAT10 tumorbevorderende RNA’s in leven houdt
Dieper gravend bracht het team specifieke ac4C-sites in het RNA van CXCL5 en DEK in kaart en bevestigde dat deze afhankelijk waren van NAT10. Wanneer NAT10 werd geremd, daalden zowel deze chemische markeringen als de niveaus van CXCL5- en DEK-RNA en -eiwit. Reporterexperimenten, waarbij de ac4C-sites precies werden gemuteerd, toonden aan dat het verlies van deze sites de RNA’s minder responsief maakte op NAT10. Metingen van RNA-afbraak toonden aan dat zonder NAT10 de boodschappen van CXCL5 en DEK sneller uiteen vielen. Met andere woorden fungeert NAT10 als een beschermende laag die ac4C-markeringen plaatst die deze RNA’s stabiliseren zodat ze langer in de cel aanwezig blijven.
Van sterkere hechting naar snellere verspreiding
Wat betekenen deze moleculaire aanpassingen voor het gedrag van kankercellen? In kweekschalen groeiden longkankercellen zonder NAT10 langzamer, migreerden en invadeerden ze minder en hechtten ze minder stevig aan verschillende componenten van het weefselraamwerk, zoals collageen en fibronectine. Hun interne skelet van actinevezels werd ook compacter, wat duidt op verminderde beweeglijkheid. Het opnieuw inbrengen van CXCL5 of DEK, en vooral beide samen, herstelde gedeeltelijk het vermogen van de cellen om te prolifereren, te bewegen en te hechten, wat laat zien dat deze twee NAT10-gestuurde genen belangrijke drijvende krachten zijn achter de agressieve eigenschappen. In muizen die via de staartader werden geïnjecteerd met longkankercellen vormden NAT10-deficiënte cellen veel minder metastatische plekken in de longen, en de dieren kwamen meer aan in gewicht en hadden een lagere tumorlast dan zij die met normale kankercellen waren geïnjecteerd.
Wat dit betekent voor toekomstige behandelingen
Door deze resultaten samen te voegen, stellen de auteurs een eenvoudig model voor: bij longadenocarcinoom voegt NAT10 ac4C-markeringen toe aan de RNA-boodschappen voor CXCL5 en DEK, waardoor ze stabiel en sterk tot expressie blijven komen. Verhoogde CXCL5 en DEK versterken vervolgens hoe stevig tumorcellen zich hechten, hoe gemakkelijk ze groeien en hoe eenvoudig ze zich naar verre plekken verspreiden. Het blokkeren van NAT10 of zijn vermogen om ac4C-markeringen te plaatsen zou deze prometastatische boodschappen dus kunnen destabiliseren en de grip en groei van de tumor kunnen verzwakken. Hoewel er meer onderzoek nodig is voordat deze strategie bij patiënten kan worden getest, benadrukt de studie RNA-acetylatie — en in het bijzonder NAT10 — als een veelbelovende nieuwe aanzet voor diagnose, voorspelling en uiteindelijk behandeling van longadenocarcinoom.
Bronvermelding: Hu, X., Feng, M., Qi, C. et al. NAT10-mediated ac4C RNA acetylation stabilizes CXCL5/DEK mRNA to drive proliferation and metastasis in lung adenocarcinoma. Cell Death Dis 17, 326 (2026). https://doi.org/10.1038/s41419-026-08568-6
Trefwoorden: longadenocarcinoom, RNA-acetylatie, NAT10, metastase, CXCL5 DEK