Clear Sky Science · pl
Acetylacja RNA ac4C zależna od NAT10 stabilizuje mRNA CXCL5/DEK, napędzając proliferację i przerzuty w gruczolakoraku płuca
Dlaczego to badanie ma znaczenie dla osób z rakiem płuca
Gruczolakorak płuca jest najczęstszą postacią raka płuca, a mimo nowoczesnych leków wielu pacjentów wciąż doświadcza wczesnego rozsiewu choroby. Badanie ujawnia ukrytą warstwę regulacji w komórkach nowotworowych: drobne chemiczne znaczniki na RNA, cząsteczkach przenoszących genetyczne przekazy. Pokazując, jak jeden enzym pomaga guzom płucnym rosnąć i rozprzestrzeniać się w organizmie, praca wskazuje nowy typ celu terapeutycznego, który w przyszłości mógłby spowolnić lub zatrzymać przerzuty.
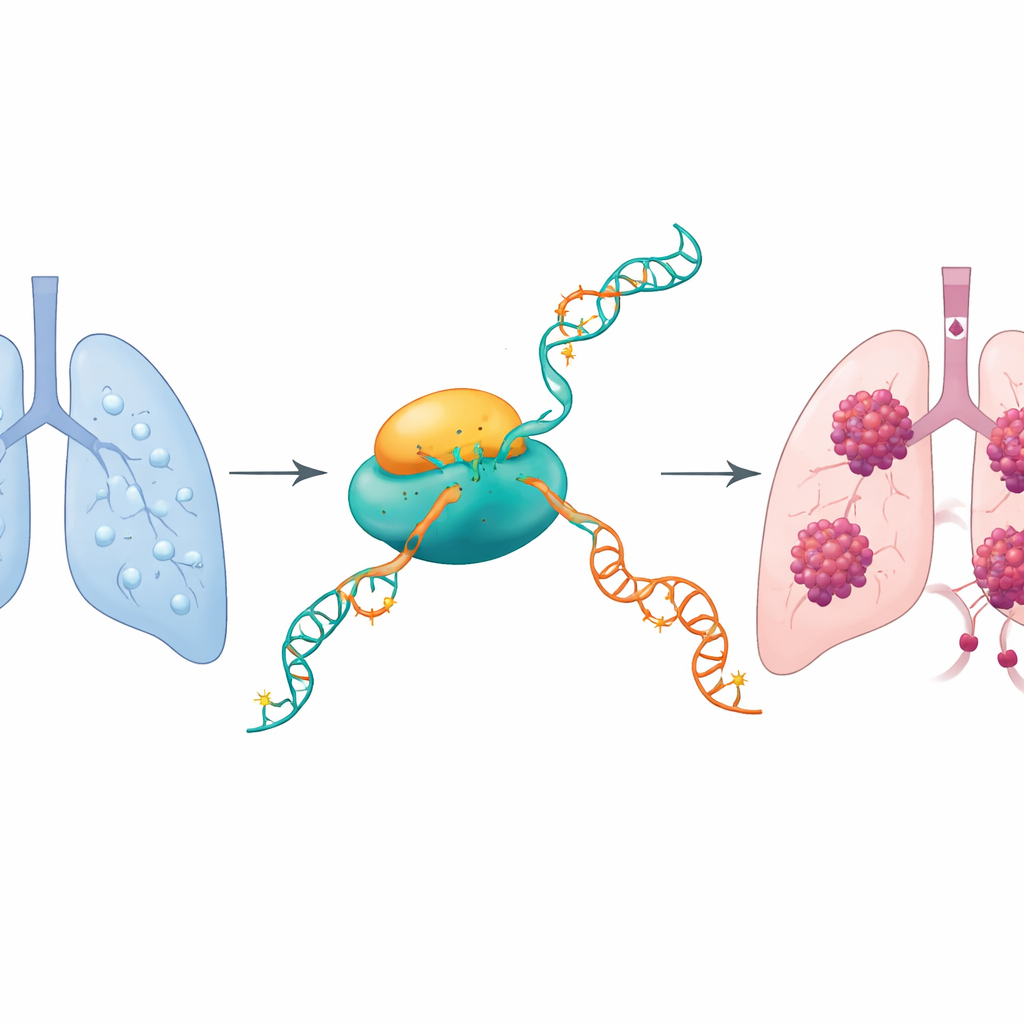
Chemiczny przełącznik na komórkowych przekazach
Nasze komórki nieustannie odczytują DNA i przepisują je na wiadomości RNA, które mówią komórce, jakie białka produkować. Autorzy skoncentrowali się na subtelnym chemicznym oznaczeniu na RNA zwanym N4-acetylocytydyną (ac4C). Tylko jeden znany enzym, NAT10, potrafi dodać tę modyfikację. Wcześniejsze badania w innych nowotworach sugerowały, że NAT10 zwiększa złośliwość komórek nowotworowych. W tej pracy badacze sprawdzili, czy NAT10 odgrywa podobną rolę w gruczolakoraku płuca i jeśli tak, które konkretne wiadomości RNA modyfikuje, by napędzać wzrost i rozsiew guza.
NAT10 jest zwiększony w guzach płuca
Wykorzystując duże publiczne bazy danych onkologicznych oraz próbki od pacjentów, zespół stwierdził, że poziomy NAT10 są znacznie wyższe w tkance gruczolakoraka płuca niż w przylegającej prawidłowej tkance płucnej. Aktywność enzymu rośnie w miarę postępu nowotworu do bardziej zaawansowanych stadiów, a pacjenci, których guzy mają wyższe poziomy NAT10, mają zwykle krótsze przeżycie. Zarówno w próbkach pacjentów, jak i w liniach komórkowych raka płuca ogólne oznaczenia ac4C na RNA były zwiększone wraz z NAT10, co sugeruje, że enzym ten szeroko przebudowuje sposób, w jaki komórki nowotworowe zarządzają swoimi genetycznymi wiadomościami.
Wyszukiwanie kluczowych wiadomości chronionych przez NAT10
Aby zobaczyć, co się dzieje po usunięciu NAT10, naukowcy użyli edycji genów CRISPR–Cas9 do wyłączenia NAT10 w komórkach A549 raka płuca. Następnie połączyli dwa globalne podejścia: sekwencjonowanie RNA, by zmierzyć, które geny zmieniły aktywność, oraz acRIP-seq, by zmapować, gdzie pojawiają się oznaczenia ac4C na RNA. Setki genów straciły zarówno ekspresję, jak i oznaczenia ac4C po usunięciu NAT10, a wiele z nich wiązało się z przyleganiem komórek do otoczenia i migracją — procesami kluczowymi dla przerzutów. Dwoma wyróżniającymi się były CXCL5, czynnik sygnałowy przyciągający i kształtujący komórki układu odpornościowego, oraz DEK, białko pomagające organizować DNA i wpływające na zachowanie guza w kilku nowotworach.
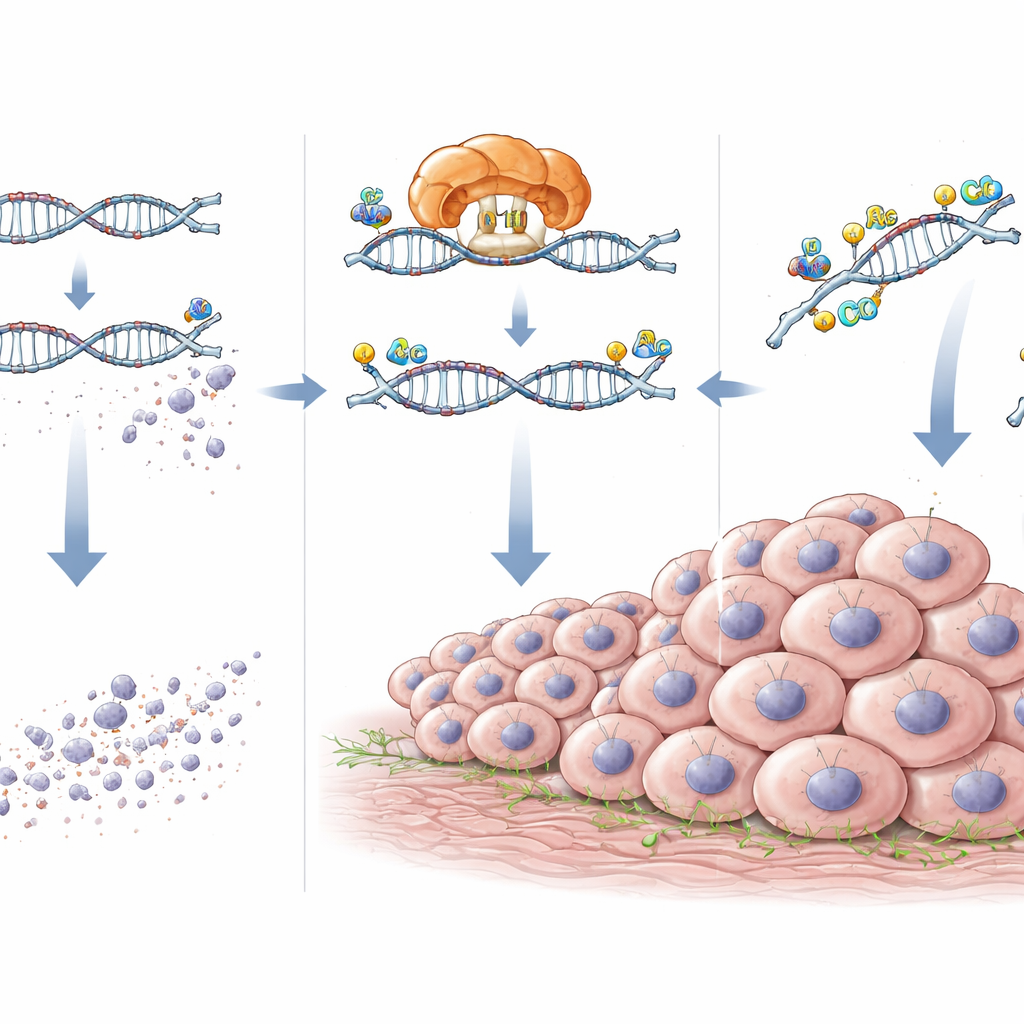
Jak NAT10 utrzymuje przy życiu RNA sprzyjające nowotworowi
Zagłębiając się dalej, zespół zmapował konkretne miejsca ac4C na RNA CXCL5 i DEK i potwierdził, że zależą one od NAT10. Gdy NAT10 został zredukowany, te chemiczne znaczniki oraz poziomy RNA i białek CXCL5 i DEK spadły. Doświadczenia z reporterami, w których miejsca ac4C zostały precyzyjnie zmutowane, wykazały, że utrata tych miejsc sprawia, iż RNA są mniej podatne na działanie NAT10. Pomiar rozpadu RNA ujawnił, że bez NAT10 wiadomości CXCL5 i DEK ulegają rozkładowi szybciej. Innymi słowy, NAT10 działa jak powłoka ochronna, umieszczając znaczniki ac4C, które stabilizują te RNA, dzięki czemu utrzymują się dłużej w komórce.
Od silniejszego przyczepienia do szybszego rozsiewu
Co te molekularne zmiany oznaczają dla zachowania komórek nowotworowych? W hodowlach komórkowych komórki raka płuca pozbawione NAT10 rosły wolniej, mniej migrowały i inwadowały oraz mniej mocno przylegały do różnych składników rusztowania tkankowego, takich jak kolagen i fibryonektyna. Ich wewnętrzny szkielet z filamentów aktynowych stał się również bardziej skondensowany, co odzwierciedla zmniejszoną ruchliwość. Ponowne wprowadzenie CXCL5 lub DEK, a szczególnie obu jednocześnie, częściowo przywróciło zdolność komórek do proliferacji, przemieszczania się i przylegania, pokazując, że te dwa geny kontrolowane przez NAT10 są głównymi czynnikami napędzającymi złośliwe cechy. U myszy, którym podano dożylnie komórki raka płuca przez żyłę ogonową, komórki deficytowe w NAT10 tworzyły znacznie mniej miejsc przerzutowych w płucach, a zwierzęta przybierały na wadze i miały mniejsze obciążenie guzem niż te, którym podano normalne komórki nowotworowe.
Co to oznacza dla przyszłych terapii
Składając te wyniki w jedną całość, autorzy proponują prosty model: w gruczolakoraku płuca NAT10 dodaje znaczniki ac4C do wiadomości RNA dla CXCL5 i DEK, utrzymując je stabilne i wysoko eksprymowane. Podwyższone CXCL5 i DEK zwiększają następnie przyczepność komórek nowotworowych, ich skłonność do wzrostu oraz łatwość, z jaką rozprzestrzeniają się na odległe miejsca. Zablokowanie NAT10 lub jego zdolności do umieszczania znaczników ac4C mogłoby więc destabilizować te pro-przerzutowe wiadomości i osłabić przyczepność oraz wzrost guza. Choć potrzeba więcej pracy, zanim tę strategię będzie można przetestować u pacjentów, badanie podkreśla acetylację RNA — a w szczególności NAT10 — jako obiecujące nowe narzędzie do diagnozowania, prognozowania i ostatecznie leczenia gruczolakoraka płuca.
Cytowanie: Hu, X., Feng, M., Qi, C. et al. NAT10-mediated ac4C RNA acetylation stabilizes CXCL5/DEK mRNA to drive proliferation and metastasis in lung adenocarcinoma. Cell Death Dis 17, 326 (2026). https://doi.org/10.1038/s41419-026-08568-6
Słowa kluczowe: gruczolakorak płuca, acetylacja RNA, NAT10, przerzuty, CXCL5 DEK