Clear Sky Science · zh
ANGPTL2通过经IGFBP5调控线粒体自噬抑制巨噬细胞焦亡并缓解类风湿性关节炎进展
这对酸痛关节为何重要
类风湿性关节炎不仅仅是僵硬和疼痛的关节——它是一种自身免疫攻击,会慢慢破坏软骨和骨质。许多现有药物是广泛抑制免疫系统,这可能让人更易感染,同时也不能完全阻止关节损伤。这项研究揭示了一种内在的保护性蛋白ANGPTL2,能帮助免疫细胞维持其内部“发电厂”——线粒体的良好功能。通过这一作用,它抑制了一种与关节破坏相关的爆发性细胞死亡形式(焦亡),提示了一种更有针对性、从内部保护关节的新思路。
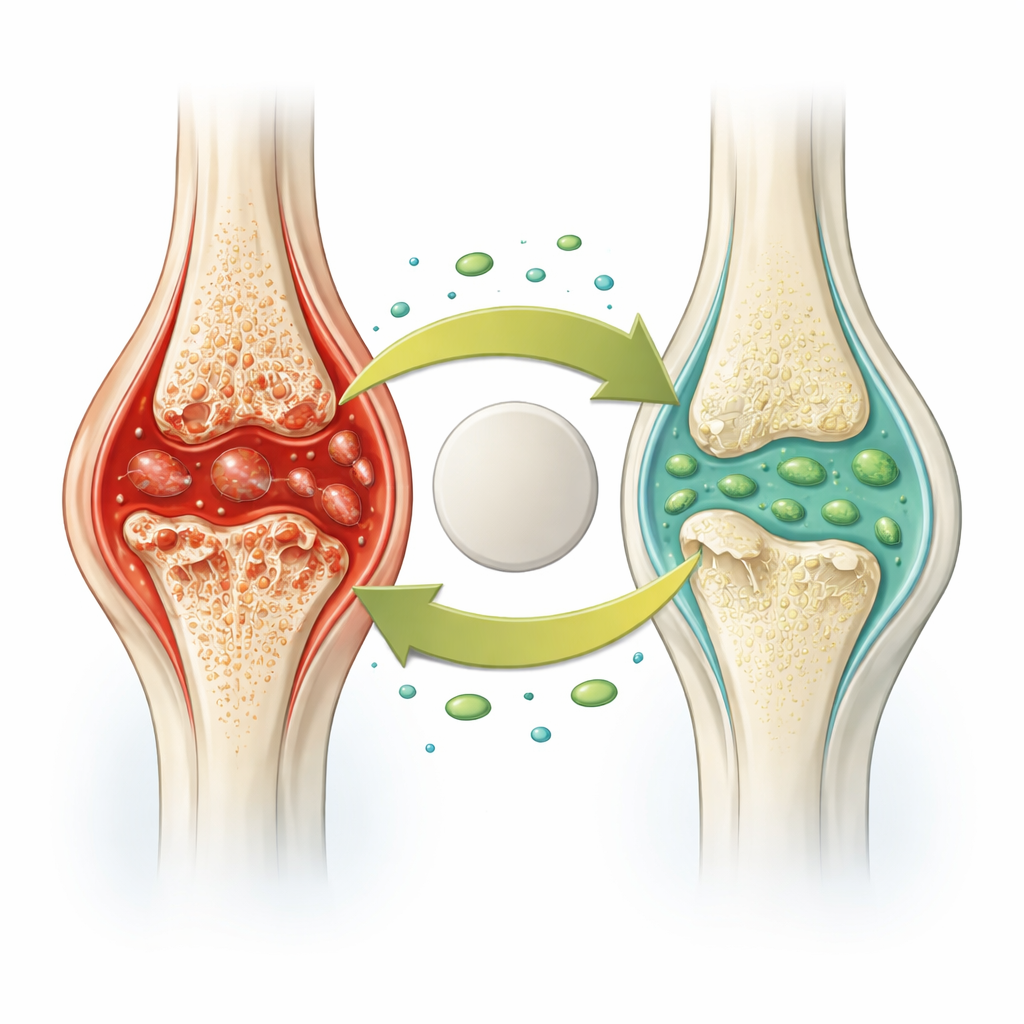
当免疫细胞从帮手变成破坏者
在类风湿性关节炎中,被称为巨噬细胞的免疫细胞大量浸润关节衬里并处于持续激活状态。有些细胞并非安静地清理碎屑,而是经历一种称为焦亡的剧烈细胞死亡。在焦亡过程中,细胞内的蛋白复合体在细胞膜上打孔,导致细胞破裂并释放强烈的炎性分子。这会加剧肿胀并吸引更多免疫细胞,形成侵蚀软骨和骨组织的恶性循环。作者探究了此前与骨骼健康和牙周病相关的蛋白ANGPTL2是否能帮助打破关节炎中的这一循环。
病变关节中缺失的保护性蛋白
研究人员使用模拟人类类风湿性关节炎的小鼠模型,比对了正常动物与基因敲除ANGPTL2的动物。缺失该蛋白的小鼠出现更严重的关节炎:爪部更肿胀,骨扫描显示更深的侵蚀,组织切片显示更多免疫细胞浸润和更多活跃的破骨细胞。在显微层面,这些小鼠的巨噬细胞携带更高水平的关键焦亡相关蛋白并释放更多炎性信号。在体外培养并暴露于细菌触发物的巨噬细胞中,ANGPTL2水平下降的同时焦亡标志物激增,提示ANGPTL2的丧失移除了对有害炎症的重要抑制。
作为隐藏杠杆的线粒体清理
进一步研究显示,ANGPTL2有助于巨噬细胞执行线粒体自噬——选择性清除受损线粒体的过程。缺乏ANGPTL2的巨噬细胞表现出线粒体膜电位下降、活性氧过多以及线粒体自噬标志减弱。受损线粒体已知会泄露危险信号,激活推动焦亡的相同蛋白机械。当研究者向巨噬细胞补充纯化的ANGPTL2时,细胞恢复了线粒体自噬、稳定了线粒体并降低了焦亡——但如果用化学方法阻断自噬,这一益处便消失了。这将ANGPTL2的保护作用直接与细胞清除故障线粒体的能力联系起来。
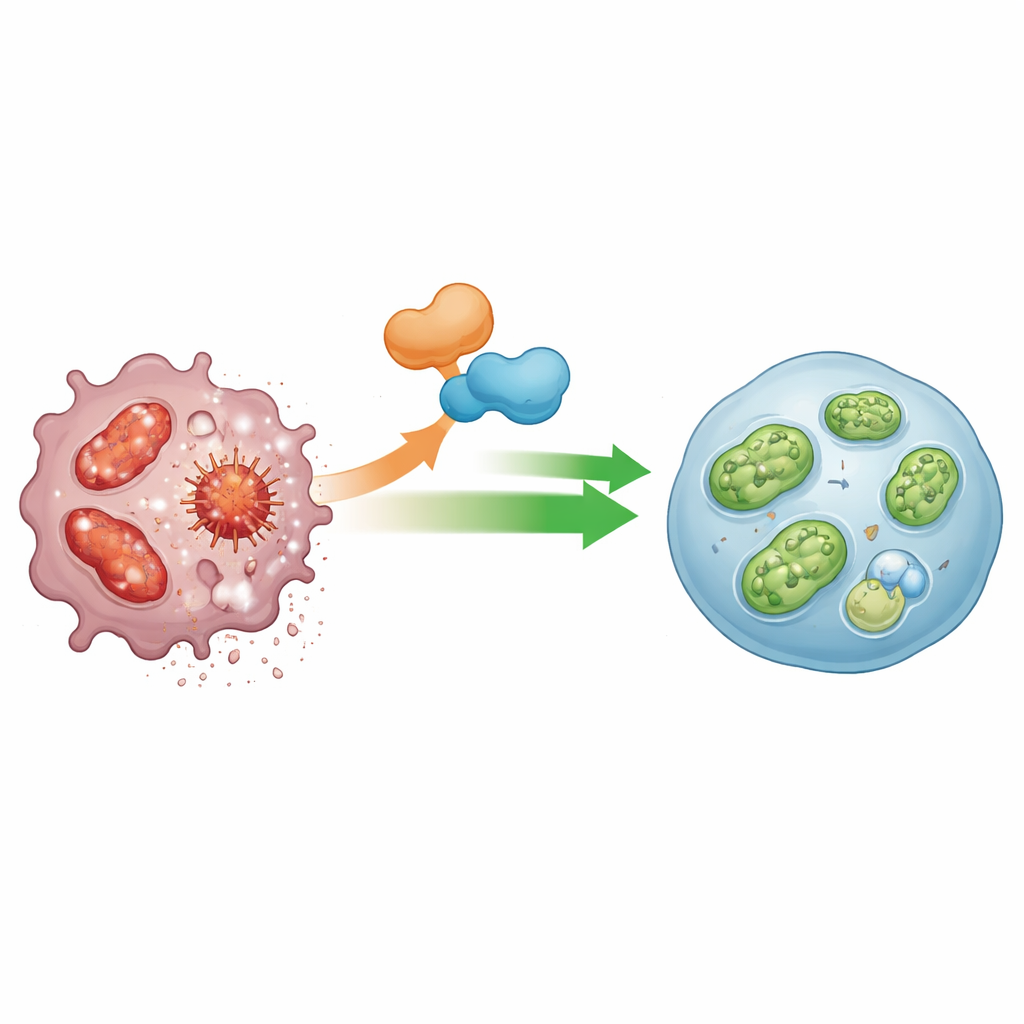
团队协作:ANGPTL2及其分子伙伴
基因表达谱分析指出了另一个参与者:IGFBP5,一种参与生长因子信号并日益与细胞回收通路相关联的蛋白。缺失ANGPTL2的巨噬细胞中IGFBP5显著下降,而单独沉默IGFBP5就足以削弱线粒体自噬并增强炎症小体活性。研究者显示ANGPTL2能提升IGFBP5水平,并且两者在巨噬细胞内存在物理相互作用。当敲低IGFBP5时,ANGPTL2不再能挽救线粒体自噬,表明这两种蛋白作为一个分子开关协同工作,维持线粒体健康并抑制炎症小体活性。
从机制到潜在新疗法
为测试提升ANGPTL2是否能实际保护炎性关节,研究团队将携带Angptl2基因的无害病毒直接输送到小鼠踝关节。接受治疗的关节表现出更少的肿胀、较完好的骨结构、更少的破骨细胞和更多的成骨细胞。这些关节中的巨噬细胞显示出较低的焦亡标志物和更强的线粒体自噬信号。通俗地说,局部补充额外的ANGPTL2帮助关节衬里平息炎症,恢复了线粒体整理功能,并减缓了不可逆损伤的进程。虽然这些实验是在小鼠中完成,尚未在人类中验证,但它们表明微调ANGPTL2–IGFBP5–线粒体自噬通路,可能提供一种更精确的保护关节的途径——通过重新训练过度活跃的免疫细胞,而不是简单地压制它们。
引用: Liu, Y., Yang, Q., Huang, Z. et al. ANGPTL2 inhibits macrophage pyroptosis and alleviates rheumatoid arthritis progression by regulating mitophagy via IGFBP5. Cell Death Dis 17, 309 (2026). https://doi.org/10.1038/s41419-026-08537-z
关键词: 类风湿性关节炎, 巨噬细胞, 线粒体自噬, 焦亡, ANGPTL2