Clear Sky Science · he
ANGPTL2 מעכב פיירופטוזיס במקרופגים ומקל על התקדמות דלקת מפרקים שגרונית על ידי ויסות מיטופאגיה באמצעות IGFBP5
מדוע זה חשוב לכאבים במפרקים
דלקת מפרקים שגרונית היא יותר מרק נוקשות וכאב במפרקים — זו מתקפה אוטואימונית שמאיטה ואוכלת לאט את הסחוס והעצם. תרופות רבות כיום מדכאות את המערכת החיסונית באופן רחב, מה שעלול לחשוף אנשים לזיהומים ועדיין אינו עוצר לחלוטין את נזקי המפרק. המחקר מצביע על חלבון מגן טבעי, ANGPTL2, שעוזר לתאי החיסון לשמור על תחנות הכוח הפנימיות שלהם — המיטוכונדריות — במצב תקין. בכך הוא מרסן צורת מוות תאי מתפרצת שקושרת להרס מפרקים, ומצביע על דרך ממוקדת יותר להגן על המפרקים מבפנים החוצה.
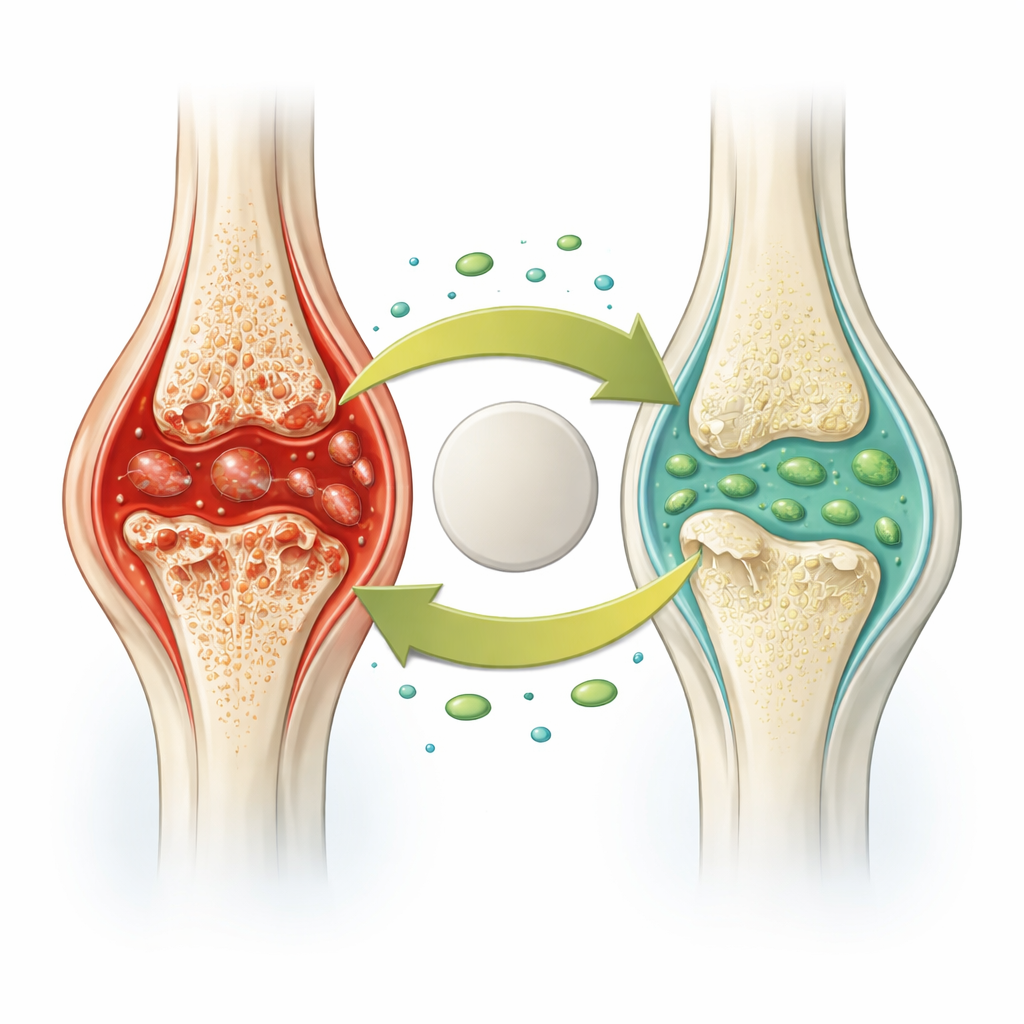
כשתאי חיסון הופכים מסייעים להורסים
בדלקת מפרקים שגרונית, תאי חיסון הנקראים מקרופגים מציפים את רירית המפרק ונשארים במצב תוקפני. במקום לנקות בעדינות שאריות, חלק מהתאים הללו עוברים צורת מוות תאי בוערת הידועה כפיירופטוזיס. במהלך פיירופטוזיס, קומפלקסים חלבוניים בתוך התא חורטים חורים בממברנת התא, גורמים לתא להתפוצץ ולשחרר מולקולות דלקת חזקות. זה מדליק נפיחות ומושך עוד תאי חיסון, ויוצר מעגל אלים שמאכלס את הסחוס והעצם. החוקרים שאלו האם ANGPTL2, חלבון שקושר בעבר לבריאות העצם ולמחלות חניכיים, עשוי לשבור את המעגל הזה במפרקים חולים.
חלבון מגן החסר במפרקים חולים
בעזרת מודל עכברים המדמה דלקת מפרקים שגרונית אנושית, השוו החוקרים בעלי חיים רגילים לעכברים שהונדסו גנטית כך שחסרים להם ANGPTL2. עכברים ללא החלבון פיתחו דלקת מפרקים חמורה יותר: כפותיהם היו נפוחות יותר, סריקות עצם הראו שחיקה עמוקה יותר ונקודות חיתוך של רקמות חשפו פלישה כבדה יותר של תאי חיסון ועוד תאים פעילי ספיגת עצם. ברמה המיקרוסקופית, מקרופגים בעכברים אלו נשאו רמות גבוהות יותר של חלבוני פיירופטוזיס עיקריים ושחררו יותר אותות דלקתיים. במקרופגים שגודלו במנהרות ונחשפו לעורר חיידקי, רמות ANGPTL2 ירדו בעוד שסימני פיירופטוזיס עלו, מה שמעיד שאובדן ANGPTL2 מסיר מעצור חשוב מפני דלקת מזיקה.
ניהול מיטוכונדריות כידית הנסתרת
בהעמקה, הקבוצה גילתה ש-ANGPTL2 מסייעת למקרופגים לבצע מיטופאגיה — ניקוי סלקטיבי של מיטוכונדריות פגועות. ללא ANGPTL2, המקרופגים הראו פגיעה בפוטנציאל ממברנת המיטוכונדריה, רמות עודפות של מולקולות חמצון פעילות וסימנים מוחלשים של מיטופאגיה. ידוע שמיטוכונדריות פגומות דולפות אותות סכנה שמפעילים את אותו מכניזם חלבוני שמניע את הפיירופטוזיס. כשהחוקרים הוסיפו חלבון ANGPTL2 מטוהר חזרה למקרופגים, התאים שאבו מחדש את המיטופאגיה, ייצובו את המיטוכונדריות והורידו את רמת הפיירופטוזיס — אלא שאם האוטופאגיה נחסמה כימית, היתרון נעלם. ממצא זה קישר את אפקט ההגנה של ANGPTL2 ישירות ליכולת התא לנקות מיטוכונדריות פגומות.
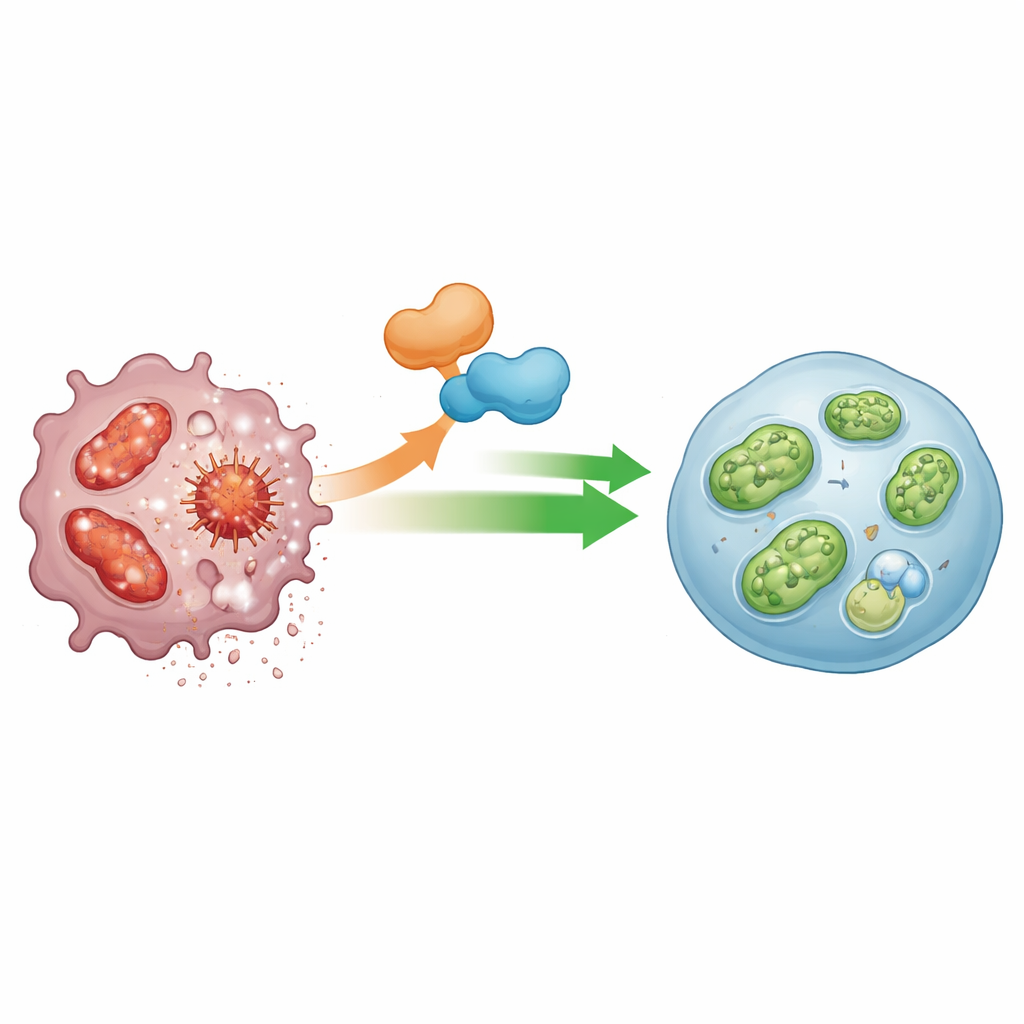
מאמץ צוותי: ANGPTL2 ושותפו המולקולרי
פרופיל ביטוי גני הצביע על שחקן נוסף: IGFBP5, חלבון המעורב באיתות גורמי גדילה ושנקשר יותר ויותר לנתיבי מיחזור תאיים. במקרופגים חסרי ANGPTL2 נצפו רמות IGFBP5 נמוכות בהרבה, ושתקת IGFBP5 לבדה הספיקה להחליש מיטופאגיה ולהגביר פעילות אינפלמיסום. החוקרים הראו ש-ANGPTL2 מעלה את רמות IGFBP5 ושהשניים פועלים באינטראקציה פיזית בתוך המקרופגים. כשנחלש IGFBP5, ANGPTL2 כבר לא יכלה להציל את המיטופאגיה, מה שמרמז שהחלבונים הללו פועלים יחד כמפסק מולקולרי שמחזיק את המיטוכונדריות בריאות ואת פעילות האינפלמיסום תחת שליטה.
ממכניזם לטיפול אפשרי חדש
כדי לבדוק האם הגברת ANGPTL2 יכולה באמת להגן על מפרקים ארתריטיים, הצוות הזריק וירוס בלתי מזיק שנושא את הגן Angptl2 ישירות למפרקי הקרסול של העכברים. המפרקים המטופלים הראו פחות נפיחות, מבנה עצם משומר טוב יותר, פחות תאי סחיפה של עצם ועוד תאי יצירת עצם. במקרופגים של מפרקים אלה הופיעו סימנים נמוכים יותר של פיירופטוזיס וסיגנלים חזקים יותר של מיטופאגיה. במילים פשוטות, מתן ANGPTL2 בצורה מקומית עזר לרירית המפרק להירגע, שיקם את ניהול המיטוכונדריות ועכב את ההתקדמות לנזק בלתי הפיך. בעוד הניסויים נערכו בעכברים ועדיין לא בבני אדם, הם מציעים כי כיוונון עדין של ציר ANGPTL2–IGFBP5–מיטופאגיה עשוי להציע דרך מדויקת יותר להגן על מפרקים — על ידי הרתמת תאי חיסון פעילות יתר במקום להשתיקם באופן גורף.
ציטוט: Liu, Y., Yang, Q., Huang, Z. et al. ANGPTL2 inhibits macrophage pyroptosis and alleviates rheumatoid arthritis progression by regulating mitophagy via IGFBP5. Cell Death Dis 17, 309 (2026). https://doi.org/10.1038/s41419-026-08537-z
מילות מפתח: דלקת מפרקים שגרונית, מקרופגים, מיטופאגיה, פיירופטוזיס, ANGPTL2