Clear Sky Science · es
ANGPTL2 inhibe la piroptosis de macrófagos y atenúa la progresión de la artritis reumatoide regulando la mitofagia vía IGFBP5
Por qué importa para las articulaciones doloridas
La artritis reumatoide es más que articulaciones rígidas y dolorosas: es un ataque autoinmune que desgasta lentamente el cartílago y el hueso. Muchos fármacos actuales deprimen el sistema inmunitario de forma general, lo que puede dejar a las personas vulnerables a infecciones y aun así no detener por completo el daño articular. Este estudio descubre una proteína protectora endógena, ANGPTL2, que ayuda a las células inmunitarias a mantener en buen estado sus centrales energéticas internas—las mitocondrias. Al hacerlo, modera una forma explosiva de muerte celular vinculada a la destrucción articular, y apunta hacia una manera más dirigida de proteger las articulaciones desde dentro.
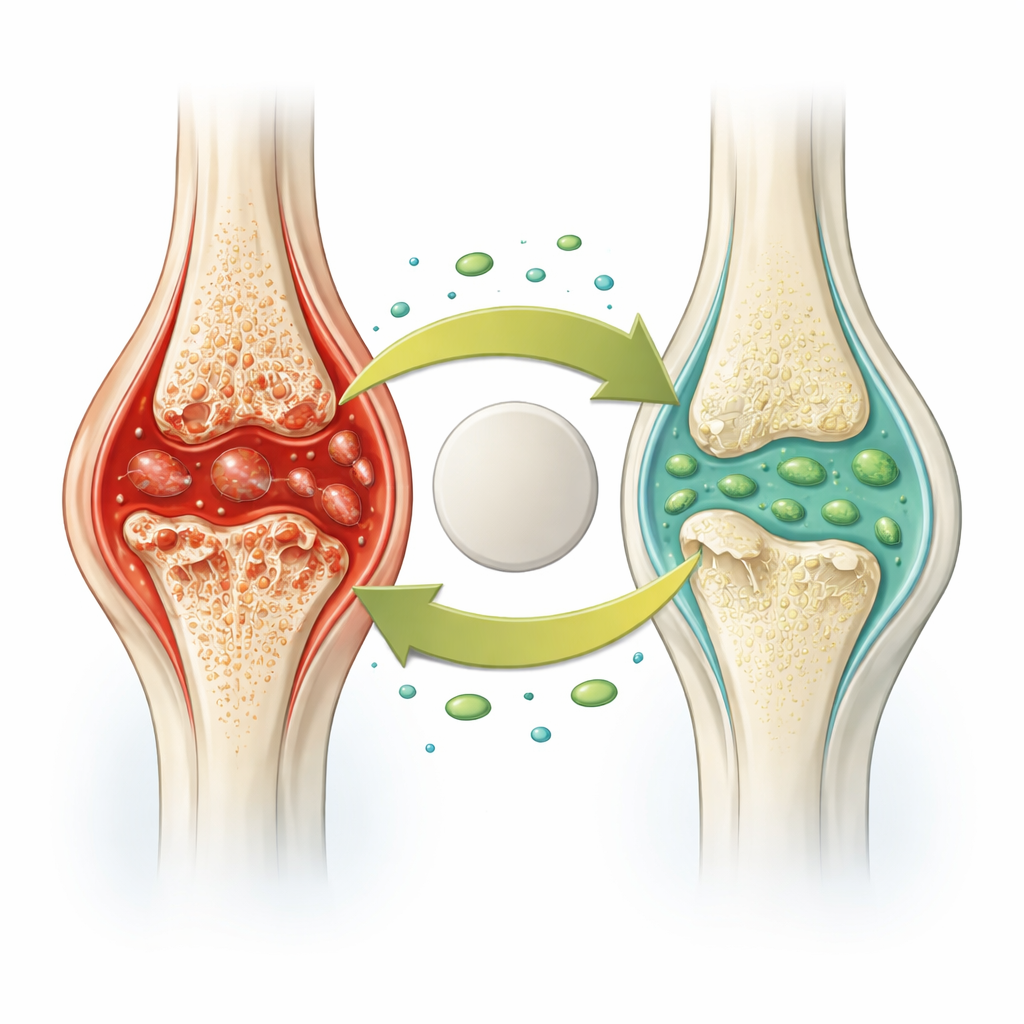
Cuando las células inmunitarias dejan de ser aliadas y se vuelven destructoras
En la artritis reumatoide, células inmunitarias llamadas macrófagos invaden el revestimiento articular y quedan atrapadas en un estado agresivo. En lugar de limpiar desechos con calma, algunas de estas células sufren un tipo inflamatorio de muerte celular conocido como piroptosis. Durante la piroptosis, complejos proteicos dentro de la célula perforan la membrana celular, provocando que la célula estalle y libere potentes moléculas inflamatorias. Esto alimenta la inflamación y atrae a más células inmunitarias, instaurando un ciclo vicioso que erosiona cartílago y hueso. Los autores se preguntaron si ANGPTL2, una proteína previamente vinculada con la salud ósea y la enfermedad periodontal, podría ayudar a romper este ciclo en articulaciones artríticas.
Una proteína protectora que falta en articulaciones enfermas
Usando un modelo murino que imita la artritis reumatoide humana, los investigadores compararon animales normales con otros modificados genéticamente para carecer de ANGPTL2. Los ratones sin esta proteína desarrollaron artritis más grave: sus patas estaban más hinchadas, las exploraciones óseas mostraron erosiones más profundas y los cortes de tejido revelaron una mayor invasión de células inmunes y más células que reabsorben hueso. A nivel microscópico, los macrófagos en estos ratones presentaban niveles elevados de proteínas clave de la piroptosis y liberaban más señales inflamatorias. En macrófagos cultivados en placa expuestos a desencadenantes bacterianos, los niveles de ANGPTL2 disminuyeron mientras los marcadores de piroptosis aumentaban, lo que sugiere que la pérdida de ANGPTL2 elimina un freno importante sobre la inflamación dañina.
La limpieza mitocondrial como palanca oculta
Profundizando, el equipo descubrió que ANGPTL2 ayuda a los macrófagos a realizar mitofagia—la limpieza selectiva de mitocondrias dañadas. Sin ANGPTL2, los macrófagos mostraron un potencial de membrana mitocondrial defectuoso, exceso de moléculas reactivas de oxígeno y marcadores de mitofagia debilitados. Se sabe que las mitocondrias dañadas filtran señales de peligro que activan la misma maquinaria proteica que impulsa la piroptosis. Cuando los investigadores añadieron ANGPTL2 purificada a macrófagos, las células restauraron la mitofagia, estabilizaron sus mitocondrias y redujeron la piroptosis—salvo cuando la autofagia fue bloqueada químicamente, en cuyo caso el beneficio desapareció. Esto vinculó el efecto protector de ANGPTL2 directamente con la capacidad celular de eliminar mitocondrias defectuosas.
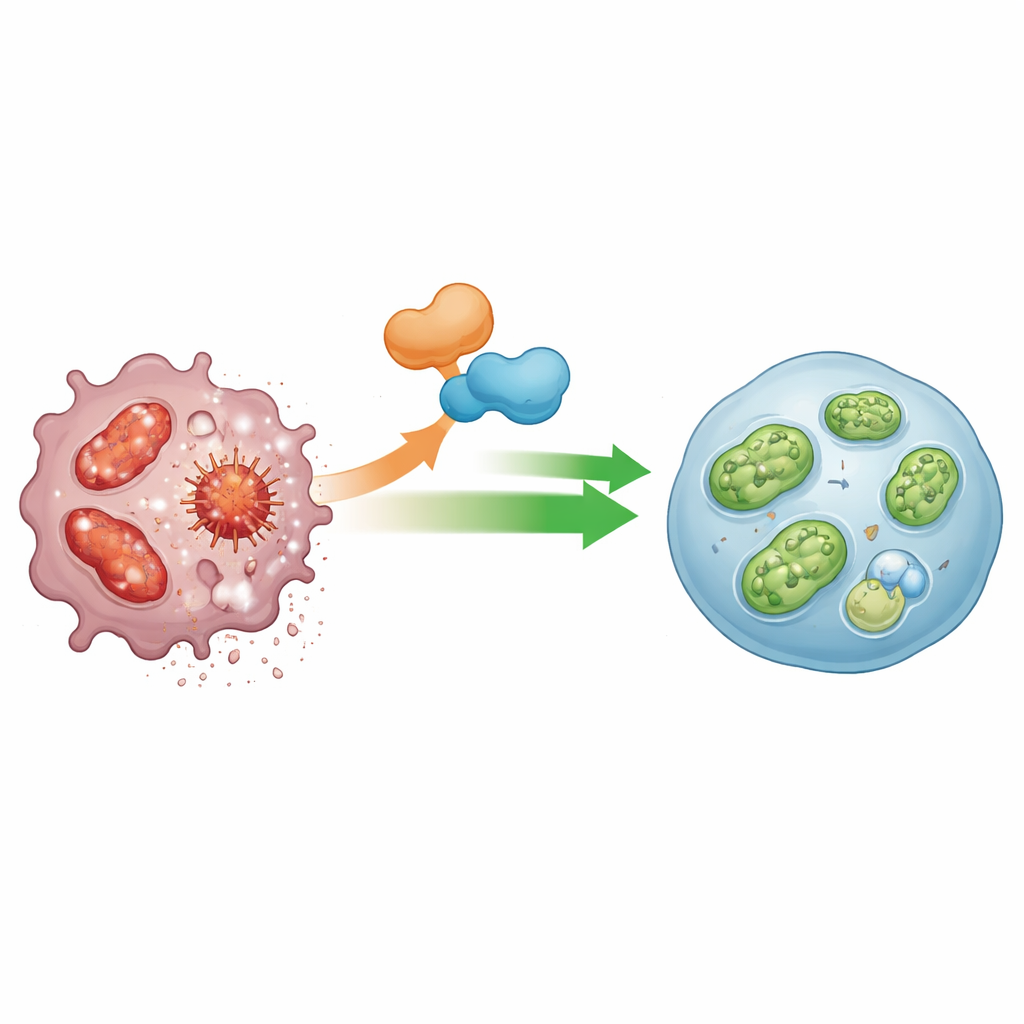
Un esfuerzo en equipo: ANGPTL2 y su socio molecular
El perfilado de la expresión génica señaló a otro protagonista: IGFBP5, una proteína implicada en la señalización de factores de crecimiento y cada vez más asociada a vías de reciclaje celular. Los macrófagos deficientes en ANGPTL2 presentaban niveles marcadamente reducidos de IGFBP5, y silenciar solo IGFBP5 fue suficiente para atenuar la mitofagia y potenciar la actividad del inflamasoma. Los investigadores demostraron que ANGPTL2 eleva los niveles de IGFBP5 y que ambas proteínas interactúan físicamente dentro de los macrófagos. Cuando IGFBP5 fue suprimido, ANGPTL2 ya no pudo rescatar la mitofagia, lo que sugiere que estas proteínas actúan juntas como un interruptor molecular que mantiene las mitocondrias sanas y controla la actividad del inflamasoma.
Del mecanismo a un posible nuevo tratamiento
Para probar si aumentar ANGPTL2 podía proteger realmente las articulaciones artríticas, el equipo administró un virus inofensivo que transportaba el gen Angptl2 directamente en las articulaciones del tobillo de ratones. Las articulaciones tratadas mostraron menos hinchazón, mejor preservación de la estructura ósea, menos células que degradan el hueso y más células formadoras de hueso. Los macrófagos en estas articulaciones exhibieron marcadores de piroptosis más bajos y señales de mitofagia más fuertes. En términos sencillos, suministrar ANGPTL2 adicional de forma local ayudó a calmar el revestimiento articular, restauró su mantenimiento mitocondrial y ralentizó el avance hacia un daño irreversible. Aunque estos experimentos se realizaron en ratones y aún no en humanos, sugieren que afinar la vía ANGPTL2–IGFBP5–mitofagia podría ofrecer una forma más precisa de proteger las articulaciones—reentrenando las células inmunitarias hiperactivas en lugar de silenciarlas simplemente.
Cita: Liu, Y., Yang, Q., Huang, Z. et al. ANGPTL2 inhibits macrophage pyroptosis and alleviates rheumatoid arthritis progression by regulating mitophagy via IGFBP5. Cell Death Dis 17, 309 (2026). https://doi.org/10.1038/s41419-026-08537-z
Palabras clave: artritis reumatoide, macrófagos, mitofagia, piroptosis, ANGPTL2