Clear Sky Science · nl
ANGPTL2 remt pyroptose van macrofagen en vertraagt de progressie van reumatoïde artritis door mitofagie te reguleren via IGFBP5
Waarom dit ertoe doet voor pijnlijke gewrichten
Reumatoïde artritis is meer dan stijve, pijnlijke gewrichten—het is een auto-immuunaanval die langzaam het kraakbeen en bot weghaalt. Veel huidige geneesmiddelen dempen het immuunsysteem breed, wat mensen vatbaar kan maken voor infecties en toch niet volledig stopt met gewrichtsschade. Deze studie onthult een ingebouwd beschermend eiwit, ANGPTL2, dat immuuncellen helpt hun interne energiecentrales—de mitochondriën—goed te laten functioneren. Daarmee remt het een explosieve vorm van celdood die in verband wordt gebracht met gewrichtsvernietiging, en wijst het op een nieuwe, meer gerichte manier om gewrichten van binnenuit te beschermen.
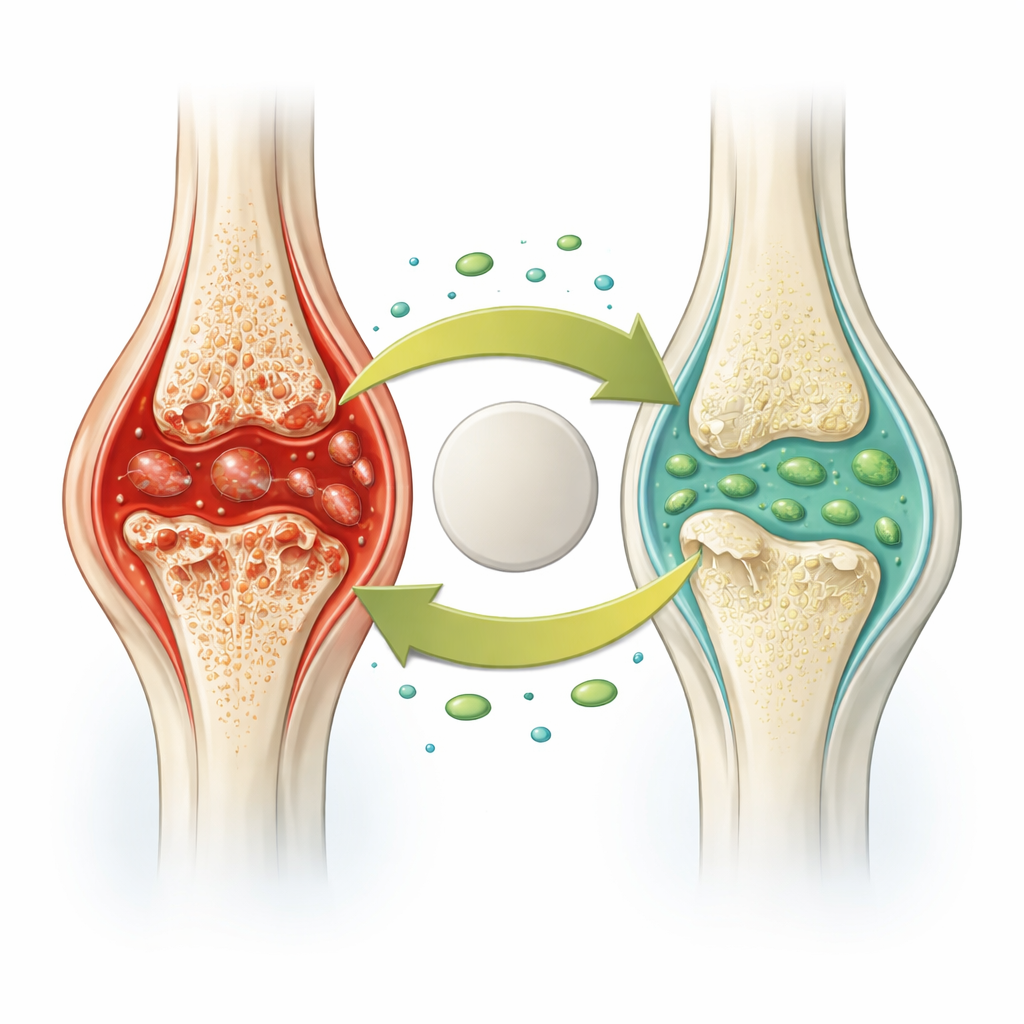
Wanneer immuuncellen van helpers in verwoesters veranderen
Bij reumatoïde artritis stromen immuuncellen die macrofagen worden genoemd de gewrichtsslijmvliezen binnen en blijven daar in een agressieve staat hangen. In plaats van rustig afval op te ruimen, ondergaan sommige van deze cellen een vurige vorm van celdood die bekendstaat als pyroptose. Tijdens pyroptose slaan eiwitcomplexen in de cel gaten in het celmembraan, waardoor de cel barst en krachtige ontstekingsmoleculen vrijgeeft. Dit voedt zwelling en trekt nog meer immuuncellen aan, waardoor een vicieuze cirkel ontstaat die kraakbeen en bot wegvreet. De auteurs vroegen zich af of ANGPTL2, een eiwit dat eerder in verband werd gebracht met botgezondheid en tandvleesziekten, deze cyclus in artritische gewrichten zou kunnen doorbreken.
Een beschermend eiwit ontbreekt in zieke gewrichten
Met een muismodel dat menselijke reumatoïde artritis nabootst, vergeleken de onderzoekers normale dieren met anderen die genetisch zo waren aangepast dat ze geen ANGPTL2 hebben. Muizen zonder dit eiwit ontwikkelden ernstigere artritis: hun poten waren meer gezwollen, botbeelden toonden diepere erosies en weefselsneden lieten zwaardere invasie door immuuncellen en meer actieve botafbrekende cellen zien. Op microscopisch niveau droegen macrofagen in deze muizen hogere niveaus van kernproteïnen betrokken bij pyroptose en gaven ze meer ontstekingssignalen af. In in-vitro gekweekte macrofagen die werden blootgesteld aan bacteriële triggers, daalden ANGPTL2-niveaus terwijl pyroptosekenmerken stegen, wat suggereert dat verlies van ANGPTL2 een belangrijke rem op schadelijke ontsteking wegneemt.
Mitochondriaal onderhoud als de verborgen hefboom
Dieper gravend ontdekten de onderzoekers dat ANGPTL2 macrofagen helpt bij mitofagie—de selectieve opruiming van beschadigde mitochondriën. Zonder ANGPTL2 vertoonden macrofagen een verzwakt mitochondriaal membraanpotentiaal, een overschot aan reactieve zuurstofmoleculen en verlaagde markers van mitofagie. Beschadigde mitochondriën lekken bekende waarschuwingssignalen die dezelfde eiwitmachinerie kunnen activeren die pyroptose aandrijft. Wanneer de onderzoekers gezuiverd ANGPTL2 aan macrofagen teruggaven, herstelden de cellen mitofagie, stabiliseerden hun mitochondriën en dempten pyroptose—tenzij autofagie chemisch werd geblokkeerd, in welk geval het voordeel verdween. Dit verbond ANGPTL2’s beschermende effect direct aan het vermogen van de cel om defecte mitochondriën te verwijderen.
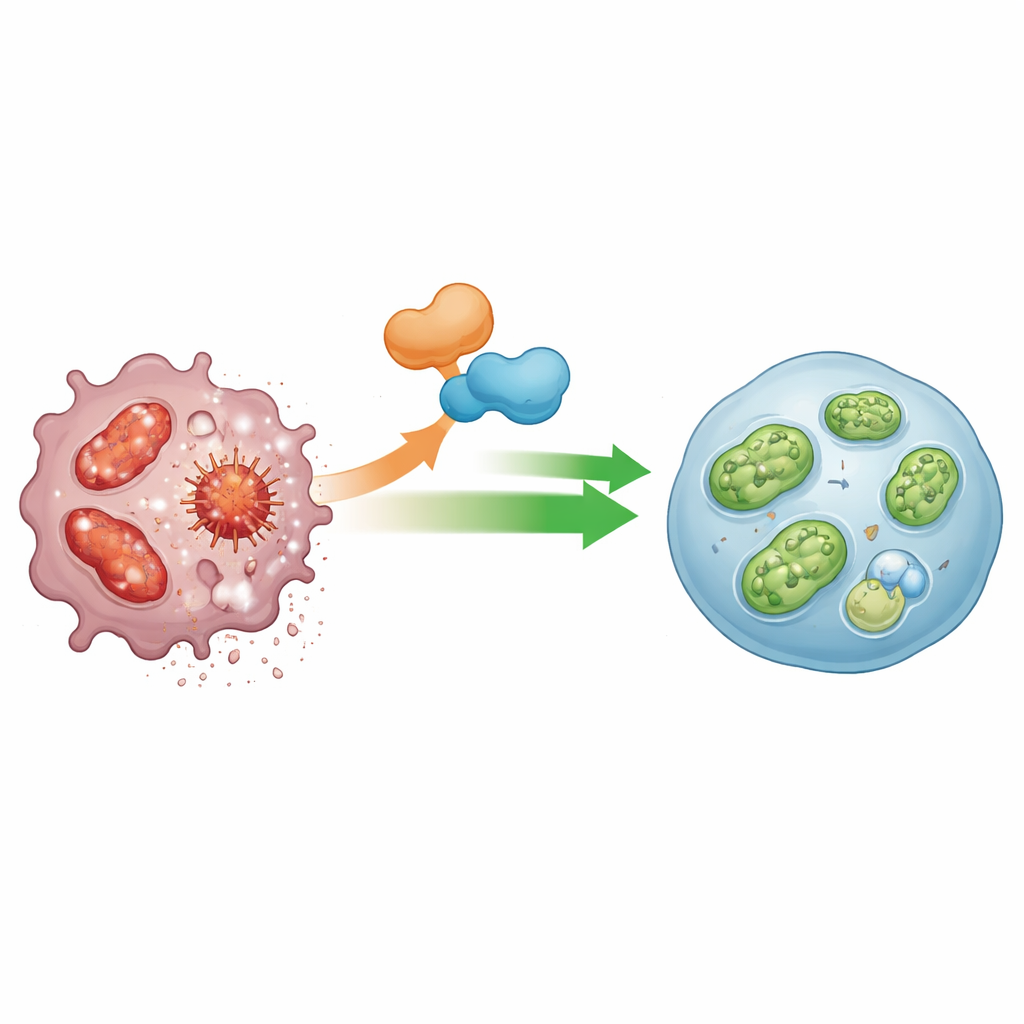
Een teaminspanning: ANGPTL2 en zijn moleculair partner
Genexpressieprofilering wees op een andere speler: IGFBP5, een eiwit dat betrokken is bij groeifactor-signaling en dat steeds vaker wordt gelinkt aan cellulaire recyclingroutes. ANGPTL2-deficiënte macrofagen hadden sterk verminderde IGFBP5, en het stilleggen van IGFBP5 alleen was al genoeg om mitofagie te verzwakken en inflammasoomactiviteit te verhogen. De onderzoekers toonden aan dat ANGPTL2 IGFBP5-niveaus verhoogt en dat de twee eiwitten fysiek met elkaar interageren binnen macrofagen. Wanneer IGFBP5 werd onderdrukt, kon ANGPTL2 mitofagie niet meer herstellen, wat suggereert dat deze eiwitten samen als een moleculaire schakel werken die mitochondriën gezond houdt en inflammasoomactiviteit in toom houdt.
Van mechanisme naar een potentiële nieuwe behandeling
Om te testen of het verhogen van ANGPTL2 daadwerkelijk artritische gewrichten kon beschermen, brachten de onderzoekers een onschadelijk virus dat het Angptl2-gen droeg rechtstreeks in muisenkelgewrichten. Behandelde gewrichten toonden minder zwelling, beter behouden botstructuur, minder botafbrekende cellen en meer botvormende cellen. Macrofagen in deze gewrichten toonden lagere pyroptosemarkers en krachtigere mitofagiesignalen. Simpel gezegd: lokaal extra ANGPTL2 toedienen hielp het gewrichtsslijmvlies te kalmeren, herstelde het mitochondriale onderhoud en vertraagde de opmars naar onomkeerbare schade. Hoewel deze experimenten in muizen en nog niet bij mensen zijn uitgevoerd, suggereren ze dat het fijnregelen van de ANGPTL2–IGFBP5–mitofagie-route een preciezere manier kan bieden om gewrichten te beschermen—door overactieve immuuncellen te hertrainen in plaats van ze simpelweg te onderdrukken.
Bronvermelding: Liu, Y., Yang, Q., Huang, Z. et al. ANGPTL2 inhibits macrophage pyroptosis and alleviates rheumatoid arthritis progression by regulating mitophagy via IGFBP5. Cell Death Dis 17, 309 (2026). https://doi.org/10.1038/s41419-026-08537-z
Trefwoorden: reumatoïde artritis, macrofagen, mitofagie, pyroptose, ANGPTL2