Clear Sky Science · fr
ANGPTL2 inhibe la pyroptose des macrophages et ralentit la progression de la polyarthrite rhumatoïde en régulant la mitophagie via IGFBP5
Pourquoi cela compte pour les articulations douloureuses
La polyarthrite rhumatoïde n’est pas seulement une raideur et des douleurs articulaires : c’est une attaque auto-immune qui ronge progressivement le cartilage et l’os. De nombreux médicaments actuels suppriment de façon large le système immunitaire, ce qui peut exposer les personnes aux infections et ne prévient pas entièrement les lésions articulaires. Cette étude met en lumière une protéine protectrice endogène, ANGPTL2, qui aide les cellules immunitaires à maintenir en bon état leurs centrales énergétiques — les mitochondries. Ce faisant, elle freine une forme explosive de mort cellulaire liée à la destruction articulaire, ouvrant la voie à une approche plus ciblée pour protéger les articulations de l’intérieur.
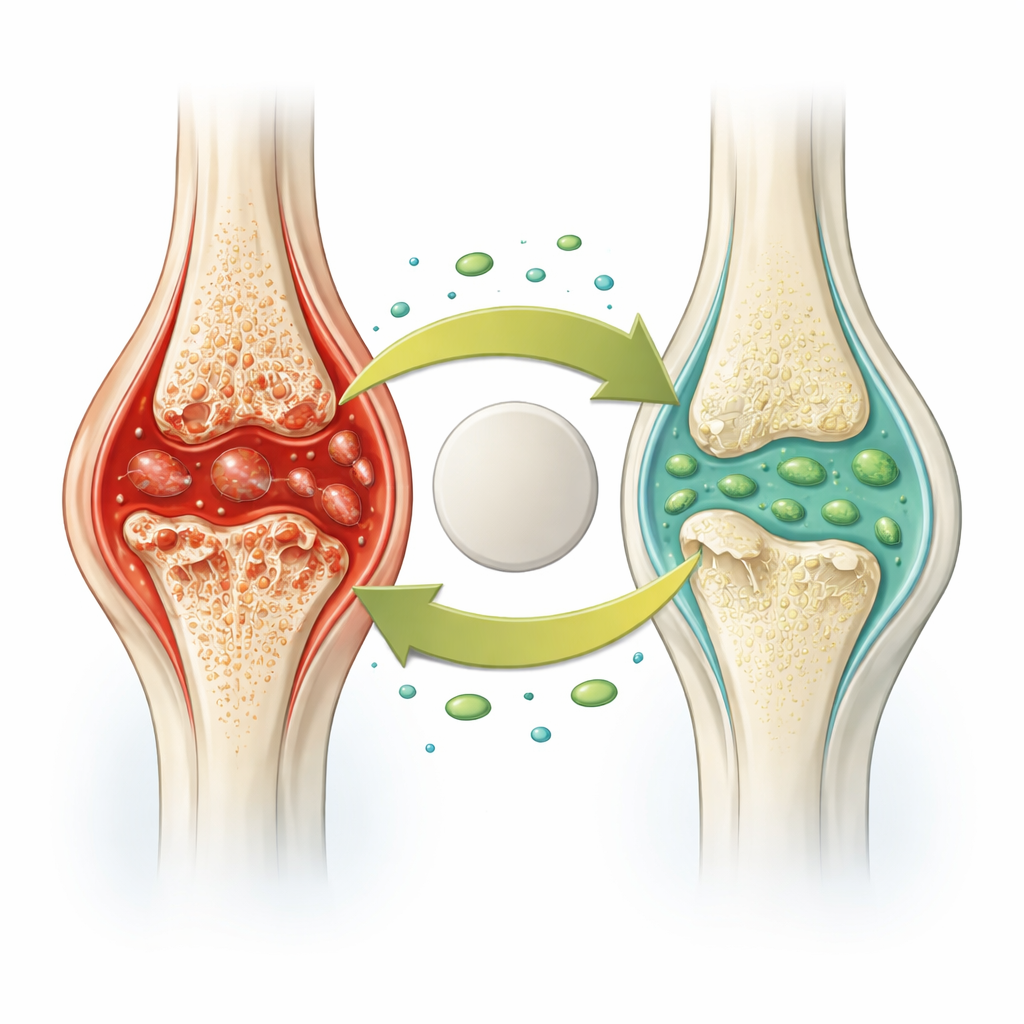
Quand les cellules immunitaires passent de secouristes à destructrices
Dans la polyarthrite rhumatoïde, des cellules immunitaires appelées macrophages envahissent la membrane articulaire et restent bloquées dans un état agressif. Au lieu de nettoyer discrètement les débris, une partie de ces cellules subit une forme enflammée de mort cellulaire appelée pyroptose. Lors de la pyroptose, des complexes protéiques forent des trous dans la membrane cellulaire, provoquant l’éclatement de la cellule et la libération de molécules inflammatoires puissantes. Cela alimente le gonflement et attire encore plus de cellules immunitaires, installant un cercle vicieux qui érode le cartilage et l’os. Les auteurs ont cherché à savoir si ANGPTL2, une protéine déjà associée à la santé osseuse et aux maladies des gencives, pouvait aider à rompre ce cycle dans les articulations arthritiques.
Une protéine protectrice absente dans les articulations malades
À l’aide d’un modèle murin reproduisant la polyarthrite rhumatoïde humaine, les chercheurs ont comparé des animaux normaux à d’autres dépourvus génétiquement d’ANGPTL2. Les souris sans cette protéine ont développé une arthrite plus sévère : leurs pattes étaient plus enflées, les scans osseux montraient une érosion plus profonde, et les coupes de tissu révélaient une invasion immune plus massive et davantage d’ostéoclastes actifs. Au niveau microscopique, les macrophages de ces souris présentaient des taux plus élevés de protéines clés de la pyroptose et libéraient plus de signaux inflammatoires. Dans des macrophages cultivés exposés à des déclencheurs bactériens, les niveaux d’ANGPTL2 chutaient tandis que les marqueurs de pyroptose augmentaient, suggérant que la perte d’ANGPTL2 supprime un frein important sur l’inflammation délétère.
L’entretien mitochondrial, levier caché
En approfondissant, l’équipe a découvert qu’ANGPTL2 aide les macrophages à effectuer la mitophagie — le recyclage sélectif des mitochondries endommagées. En l’absence d’ANGPTL2, les macrophages montraient une dégradation du potentiel de membrane mitochondrial, un excès d’espèces réactives de l’oxygène et une faiblesse des marqueurs de mitophagie. Les mitochondries abîmées sont connues pour fuir des signaux de danger qui activent la même machinerie protéique responsable de la pyroptose. Lorsque les chercheurs ont réintroduit de l’ANGPTL2 purifiée dans les macrophages, les cellules ont rétabli la mitophagie, stabilisé leurs mitochondries et réduit la pyroptose — sauf si l’autophagie était bloquée chimiquement, auquel cas le bénéfice disparaissait. Cela relie directement l’effet protecteur d’ANGPTL2 à la capacité cellulaire d’éliminer les mitochondries défectueuses.
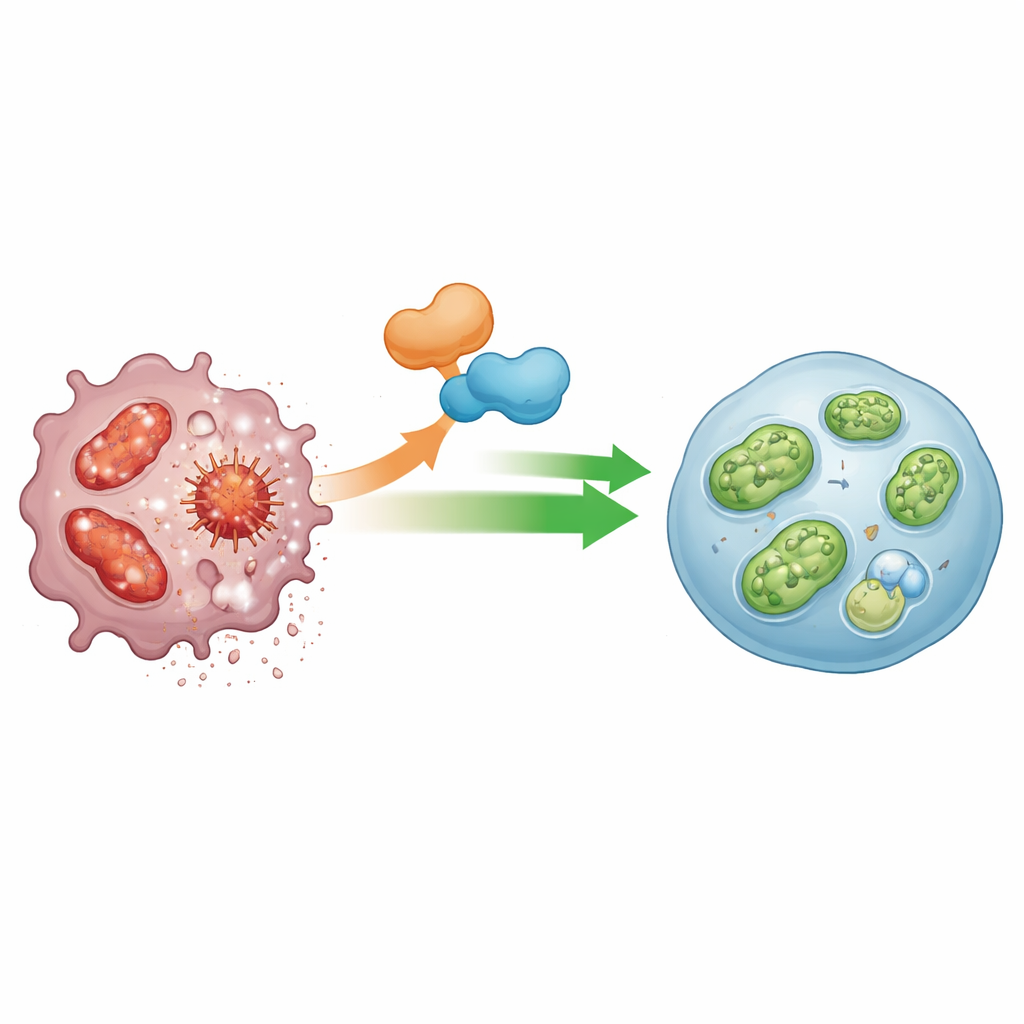
Un effort d’équipe : ANGPTL2 et son partenaire moléculaire
Le profilage de l’expression génique a désigné un autre intervenant : IGFBP5, une protéine impliquée dans la signalisation des facteurs de croissance et de plus en plus associée aux voies de recyclage cellulaire. Les macrophages déficients en ANGPTL2 présentaient des niveaux fortement réduits d’IGFBP5, et l’inhibition d’IGFBP5 à elle seule suffisait à affaiblir la mitophagie et à stimuler l’activité de l’inflammasome. Les chercheurs ont montré qu’ANGPTL2 augmente les niveaux d’IGFBP5 et que ces deux protéines interagissent physiquement à l’intérieur des macrophages. Lorsque IGFBP5 était réduit, ANGPTL2 ne pouvait plus restaurer la mitophagie, suggérant que ces protéines agissent de concert comme un interrupteur moléculaire qui maintient les mitochondries en bonne santé et limite l’activité de l’inflammasome.
Du mécanisme à un traitement potentiel
Pour tester si l’augmentation d’ANGPTL2 pouvait effectivement protéger les articulations arthritiques, l’équipe a délivré un virus inoffensif portant le gène Angptl2 directement dans les articulations de la cheville de souris. Les articulations traitées présentaient moins d’enflure, une structure osseuse mieux préservée, moins d’ostéoclastes et davantage d’ostéoblastes. Les macrophages de ces articulations montraient des marqueurs de pyroptose réduits et des signaux de mitophagie renforcés. En termes simples, un apport local supplémentaire d’ANGPTL2 aida la membrane articulaire à se calmer, rétablit son entretien mitochondrial et ralentit la progression vers des lésions irréversibles. Bien que ces expériences aient été réalisées chez la souris et pas encore chez l’homme, elles suggèrent que la modulation de la voie ANGPTL2–IGFBP5–mitophagie pourrait offrir une manière plus précise de protéger les articulations — en rééduquant les cellules immunitaires hyperactives plutôt qu’en les étouffant simplement.
Citation: Liu, Y., Yang, Q., Huang, Z. et al. ANGPTL2 inhibits macrophage pyroptosis and alleviates rheumatoid arthritis progression by regulating mitophagy via IGFBP5. Cell Death Dis 17, 309 (2026). https://doi.org/10.1038/s41419-026-08537-z
Mots-clés: polyarthrite rhumatoïde, macrophages, mitophagie, pyroptose, ANGPTL2