Clear Sky Science · zh
ENO2驱动肿瘤细胞诱导M2型巨噬细胞极化以促进结直肠癌肝转移
这项研究为何重要
当结直肠癌扩散至肝脏时,治疗难度大幅增加,也是许多患者死亡的主要原因。本研究探讨了一个具有重要临床意义的基础问题:肿瘤细胞如何说服机体的免疫细胞“倒戈”,在肝脏中帮助癌症生长?通过锁定一种推动这种有害联盟的肿瘤蛋白,研究为一种新型靶向治疗打开了可能性。
更近一步观察扩散到肝脏的结肠肿瘤
研究者首先构建了结直肠癌肝转移的细胞级“逐细胞图谱”,并将其与未发生转移的肿瘤进行比较。利用单细胞RNA测序,他们分析了来自原发结肠肿瘤、邻近正常组织和肝转移灶的数千个单细胞。结果显示,肝转移灶中的癌细胞在基因组上更不稳定、增殖更快,而且比原发结肠肿瘤中的细胞更能适应低氧环境。这证实了肝转移灶并非原发肿瘤的简单复制品,而包含更具侵袭性和适应生存的癌细胞群体。
发现危险的肿瘤细胞亚群
为了解哪些癌细胞更易发生转移,研究团队基于基因表达模式对肿瘤细胞进行分组。一个与患者较差生存相关的基因模块格外突出。在该模块内,一部分肿瘤细胞显示出强烈的“上皮-间质转化”(EMT)程序,这有助于细胞脱落并迁移。在该模块的十个候选基因中,一种酶ENO2与更差的预后呈独特关联。肿瘤中ENO2水平较高的患者生存期明显缩短,且独立的患者队列证实,与正常组织相比,ENO2在原发肿瘤和肝转移灶中均升高。
肿瘤如何“教”免疫细胞为其效劳
接下来要弄清的是ENO2阳性癌细胞如何影响周围环境。利用可推断细胞间信号的计算工具,研究者发现富含ENO2的肿瘤细胞充当主要“广播枢纽”,尤其通过涉及一种名为MIF的蛋白的通路发挥作用。他们发现ENO2在癌细胞内与MIF发生物理结合,并保护MIF免于被标记降解,使MIF在细胞内累积。反过来,这激活了肿瘤细胞的生长与生存通路,并向邻近巨噬细胞发出强烈信号——巨噬细胞可表现为攻击肿瘤的M1样状态,或以M2样状态支持肿瘤生长并抑制其他免疫反应。在共培养实验和动物模型中,ENO2高表达的癌细胞持续将巨噬细胞推向这种有利于肿瘤的M2状态。
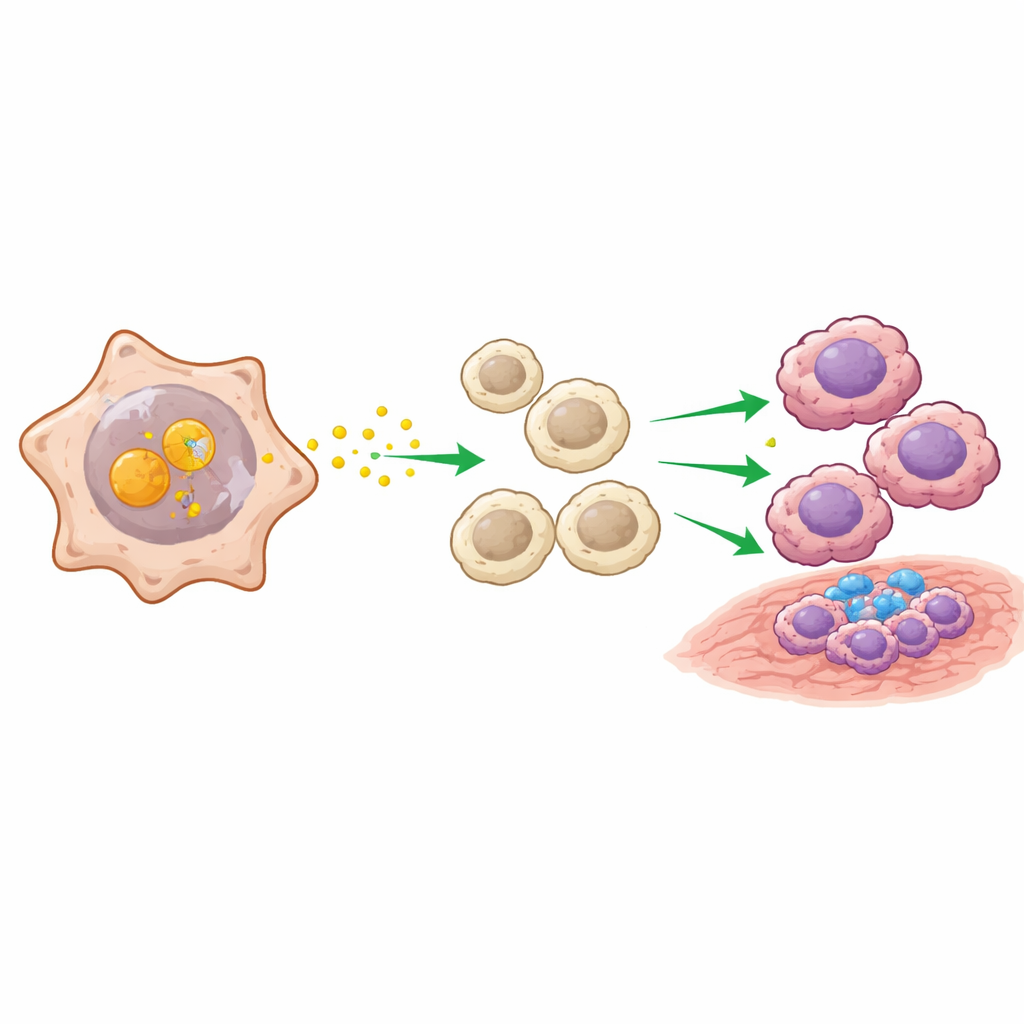
从机制到潜在药物
基于这一机制洞见,团队寻找能够破坏ENO2–MIF互作的药物。通过对6000多种小分子进行计算筛选并随后在实验室验证,他们鉴定出吡硫啶(pyrithioxin)为一种能嵌入ENO2与MIF接触位点的化合物。在癌细胞中,吡硫啶破坏了两者的相互作用,恢复了MIF的降解,并削弱了下游的生长信号。在将结肠癌细胞注入以形成肝转移的小鼠模型中,经口给予吡硫啶显著减少了肝脏肿瘤的数量和体积,并降低了转移灶中M2样巨噬细胞的标志物水平。
对患者意味着什么
简言之,本研究表明一种酶ENO2通过保护信号蛋白MIF免于降解,帮助结肠癌细胞在肝脏将周围免疫细胞“重编程”为支持肿瘤的M2型。这形成了一个自我强化的免疫抑制与转移生长回路。研究还显示,阻断ENO2–MIF相互作用可在小鼠中缩小肝转移灶,提示一种有前景的新治疗策略:与其仅直接杀伤癌细胞,不如破坏那些让癌细胞将免疫系统变成同谋的隐蔽“对话”。
引用: Tang, J., Chen, Z., Zhang, D. et al. ENO2 drives tumor cell-induced M2 macrophage polarization to promote colorectal cancer liver metastasis. Sig Transduct Target Ther 11, 166 (2026). https://doi.org/10.1038/s41392-026-02732-2
关键词: 结直肠癌肝转移, 肿瘤微环境, 巨噬细胞极化, ENO2–MIF轴, 癌症免疫治疗