Clear Sky Science · ja
ENO2は腫瘍細胞によるM2マクロファージ分極を駆動し、大腸癌の肝転移を促進する
この研究が重要な理由
大腸がんが肝臓に転移すると治療が格段に難しくなり、多くの患者が亡くなる主因となります。本研究は臨床的意義の大きい基本的な問いに迫ります:腫瘍細胞はどのようにして身体の免疫細胞を味方につけ、肝臓でがんの増殖を助けさせるのか? 単一の腫瘍タンパク質がこの有害な協力関係を推進することを特定することで、新たな標的治療の可能性が開かれます。
肝転移を起こす大腸腫瘍を詳しく見る
研究者らはまず、肝転移した大腸がんと転移していない腫瘍を比較し、詳細な「細胞ごとの地図」を作成しました。単細胞RNAシーケンシングを用いて、原発性大腸腫瘍、周辺の正常組織、肝転移巣から得た何千もの個々の細胞を解析しました。その結果、肝転移巣のがん細胞は遺伝的不安定性が高く、増殖が速く、低酸素環境への適応力が高いことが明らかになりました。これは、肝転移が単なる原発腫瘍のコピーではなく、より攻撃的で生存に強いがん細胞集団を含むことを裏付けます。
危険な腫瘍細胞サブセットの発見
どのがん細胞が転移に適しているかを理解するために、研究チームは遺伝子発現パターンの類似に基づいて腫瘍細胞を分類しました。患者予後不良と関連する特定の遺伝子モジュールが際立ちました。その中のサブセットは、細胞が分離して移動するのを助ける上皮間葉転換(EMT)と呼ばれる強い“形質変換”プログラムを示していました。このモジュールの上位候補遺伝子10種のうち、酵素であるENO2が特に予後不良と結びついていました。ENO2の発現が高い患者は有意に生存期間が短く、独立した患者コホートでもENO2が正常組織に比べて原発腫瘍および肝転移で上昇していることが確認されました。
腫瘍が免疫細胞を“教育”して助けさせる仕組み
次に、ENO2陽性のがん細胞が周囲にどのように影響するかを調べました。細胞間シグナルを推定する計算ツールを用いると、ENO2豊富ながん細胞は特にMIFというタンパク質を介した経路を通じて、主要な“送信ハブ”として働くことが示されました。研究者らは、ENO2ががん細胞内でMIFに物理的に結合し、分解のための標識からMIFを守ることでMIFが蓄積することを発見しました。これにより腫瘍細胞の増殖・生存経路が活性化され、近傍のマクロファージに強いシグナルが送られます。マクロファージは腫瘍を攻撃するM1様状態にもなり得ますが、M2様状態では腫瘍成長を助け、他の免疫反応を抑制します。共培養実験や動物モデルにおいて、ENO2高発現のがん細胞は一貫してマクロファージをこの腫瘍助長的なM2状態へと誘導しました。
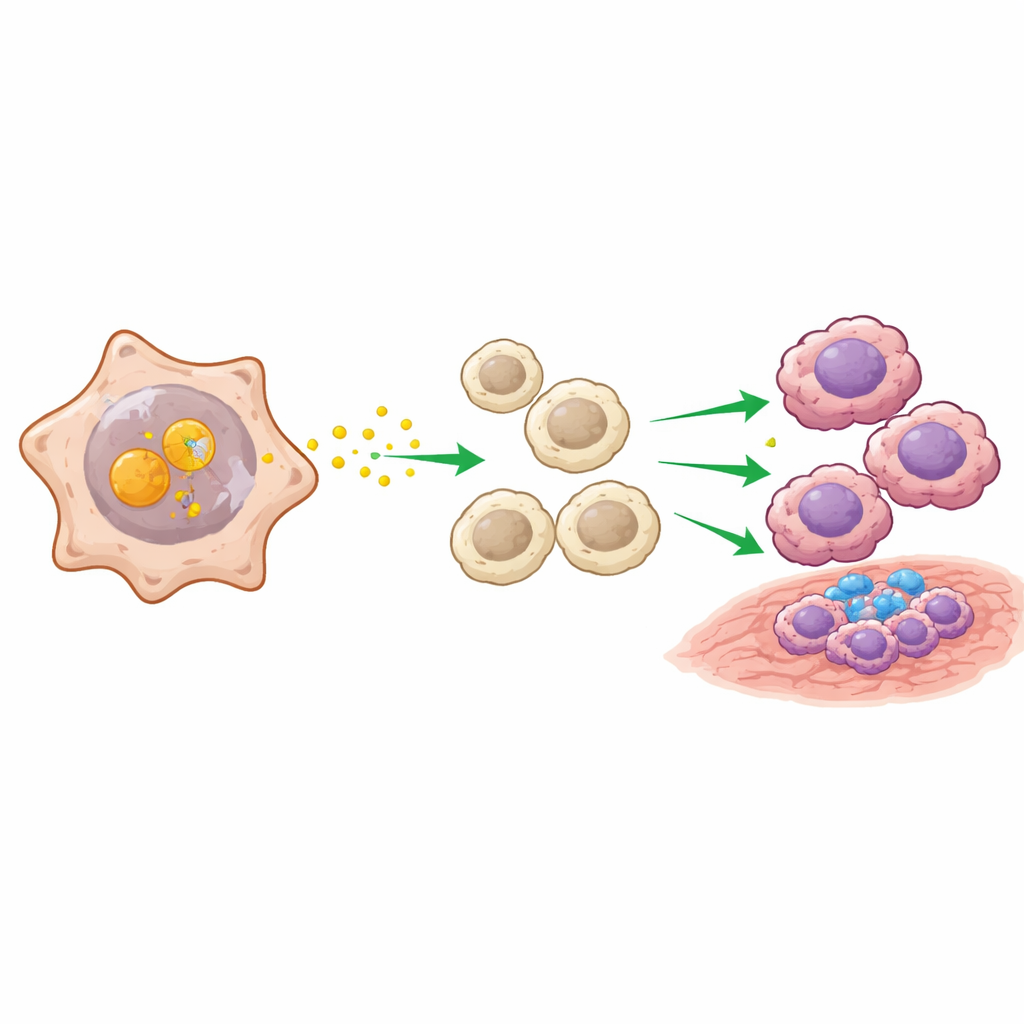
メカニズムから治療へ
このメカニズム的知見をもとに、研究チームはENO2–MIFの結合を断ち切る薬剤を探索しました。6,000を超える小分子の計算スクリーニングと実験検証を経て、ピリチオキシンがENO2とMIFの接触部位に楔を打ち込む化合物として同定されました。がん細胞では、ピリチオキシンが両者の相互作用を阻害し、MIFの分解を回復させ、下流の増殖シグナルを弱めました。大腸がん細胞を注入して肝転移を形成させたマウスモデルでは、経口投与されたピリチオキシンが肝腫瘍の数と大きさを劇的に減少させ、転移巣におけるM2様マクロファージの指標を低下させました。
患者にとっての意義
簡潔に言えば、本研究は単一の酵素ENO2が、シグナルタンパク質MIFを分解から保護することで大腸がん細胞が周囲の免疫細胞を肝臓で“再プログラム”し、腫瘍を育むM2様の役割へと導くことを示しています。これにより免疫抑制と転移成長の自己強化ループが生まれます。ENO2–MIF相互作用を阻害することでマウスの肝転移を縮小できることを示したこの成果は、がん細胞を直接攻撃するだけでなく、彼らが免疫系を共犯に変えてしまう“隠れた会話”を断つ新しい治療戦略の有望性を示しています。
引用: Tang, J., Chen, Z., Zhang, D. et al. ENO2 drives tumor cell-induced M2 macrophage polarization to promote colorectal cancer liver metastasis. Sig Transduct Target Ther 11, 166 (2026). https://doi.org/10.1038/s41392-026-02732-2
キーワード: 大腸がんの肝転移, 腫瘍微小環境, マクロファージの分極, ENO2–MIF軸, がん免疫療法