Clear Sky Science · tr
ENO2, tümör hücresi kaynaklı M2 makrofaj polarizasyonunu yönlendirerek kolorektal kanser karaciğer metastazını destekler
Bu araştırma neden önemli
Kolorektal kanser karaciğere yayıldığında tedavisi çok daha güçleşir ve birçok hastanın hastalıktan ölümünün başlıca nedenini oluşturur. Bu çalışma, klinik açıdan büyük sonuçları olan temel bir soruyu araştırıyor: tümör hücreleri vücudun bağışıklık hücrelerini nasıl ikna ederek karaciğerde kanserin büyümesine yardım ettiriyor? Zararlı bu işbirliğini tetikleyen tek bir tümör proteinini tanımlayarak, çalışma yeni bir hedefe yönelik tedavi olanağının yolunu açıyor.
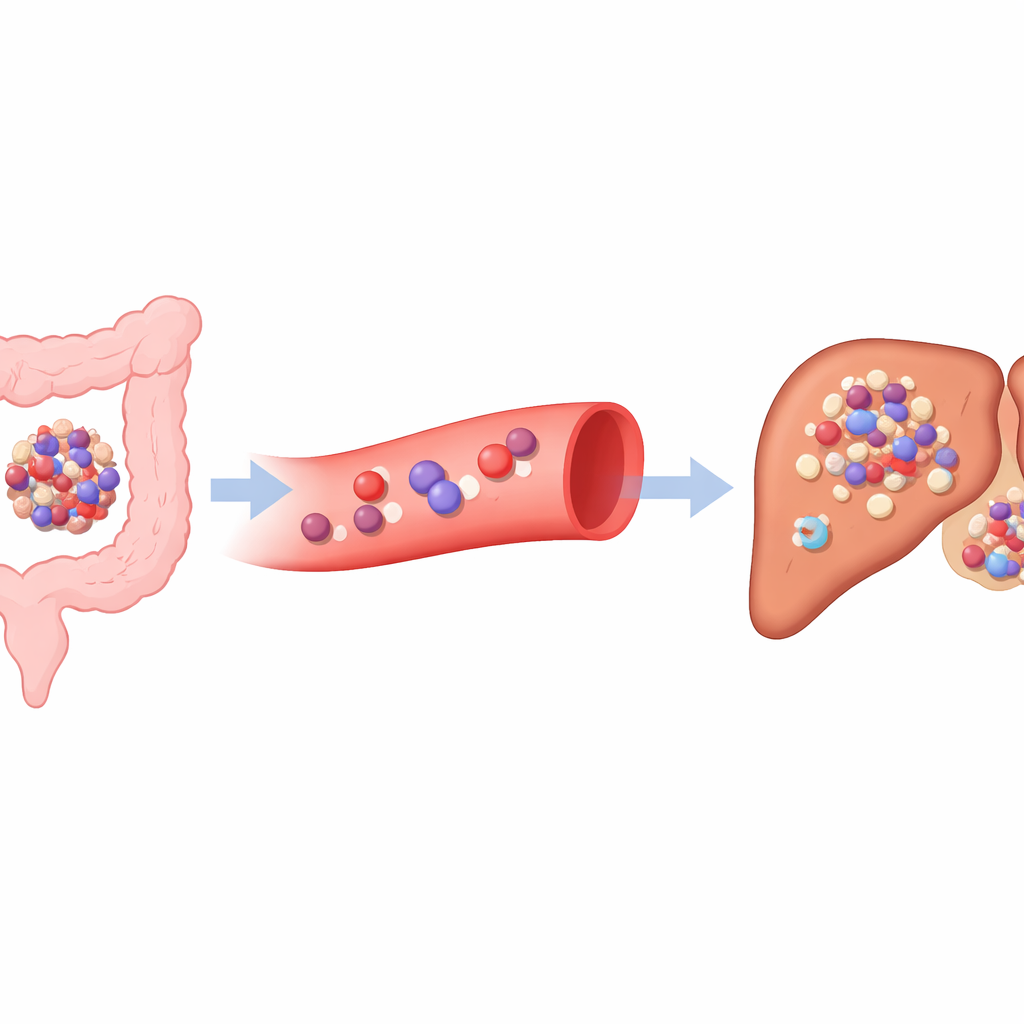
Karaciğere yayılan kolon tümörlerine daha yakından bakış
Araştırmacılar, karaciğere metastaz yapmış kolorektal kanserleri metastaz yapmamış tümörlerle karşılaştırarak ayrıntılı bir “hücre hücre haritası” oluşturarak başladılar. Tek hücreli RNA dizilemesi kullanarak birincil kolon tümörleri, çevresindeki normal doku ve karaciğer metastazlarından binlerce bireysel hücreyi analiz ettiler. Karaciğer odaklarındaki kanser hücrelerinin genetik olarak daha kararsız, daha hızlı bölünen ve orijinal kolon tümörlerindekilere göre düşük oksijen koşullarına daha iyi uyum sağlayan özellikler taşıdığını buldular. Bu, karaciğer metastazlarının yalnızca birincil tümörün kopyaları olmadığını, daha saldırgan ve hayatta kalma açısından sertleşmiş bir kanser hücresi popülasyonu içerdiğini doğruladı.
Tehlikeli bir tümör hücresi alt kümesini bulmak
Hangi kanser hücrelerinin yayılmaya yatkın olduğunu anlamak için ekip, tümör hücrelerini ortak gen etkinliği desenlerine göre gruplandırdı. Zayıf hasta sağkalımıyla ilişkili olan belirli bir gen modülü öne çıktı. Bu modül içinde, hücrelerin ayrılmasını ve göç etmesini kolaylaştıran epiteliyal-mezenkimal geçiş adlı güçlü bir “şekil değiştirme” programı gösteren bir tümör hücresi alt kümesi vardı. Bu modülde öne çıkan on aday gen arasında ENO2 adlı bir enzim, özellikle daha kötü sonuçlarla ilişkilendirildi. Tümörlerinde daha yüksek ENO2 düzeyleri olan hastalar belirgin şekilde daha kısa süre yaşadı ve bağımsız hasta grupları ENO2’nin normal dokuya kıyasla hem birincil tümörlerde hem de karaciğer metastazlarında yükselmiş olduğunu doğruladı.
Tümörler bağışıklık hücrelerini nasıl yönlendirir
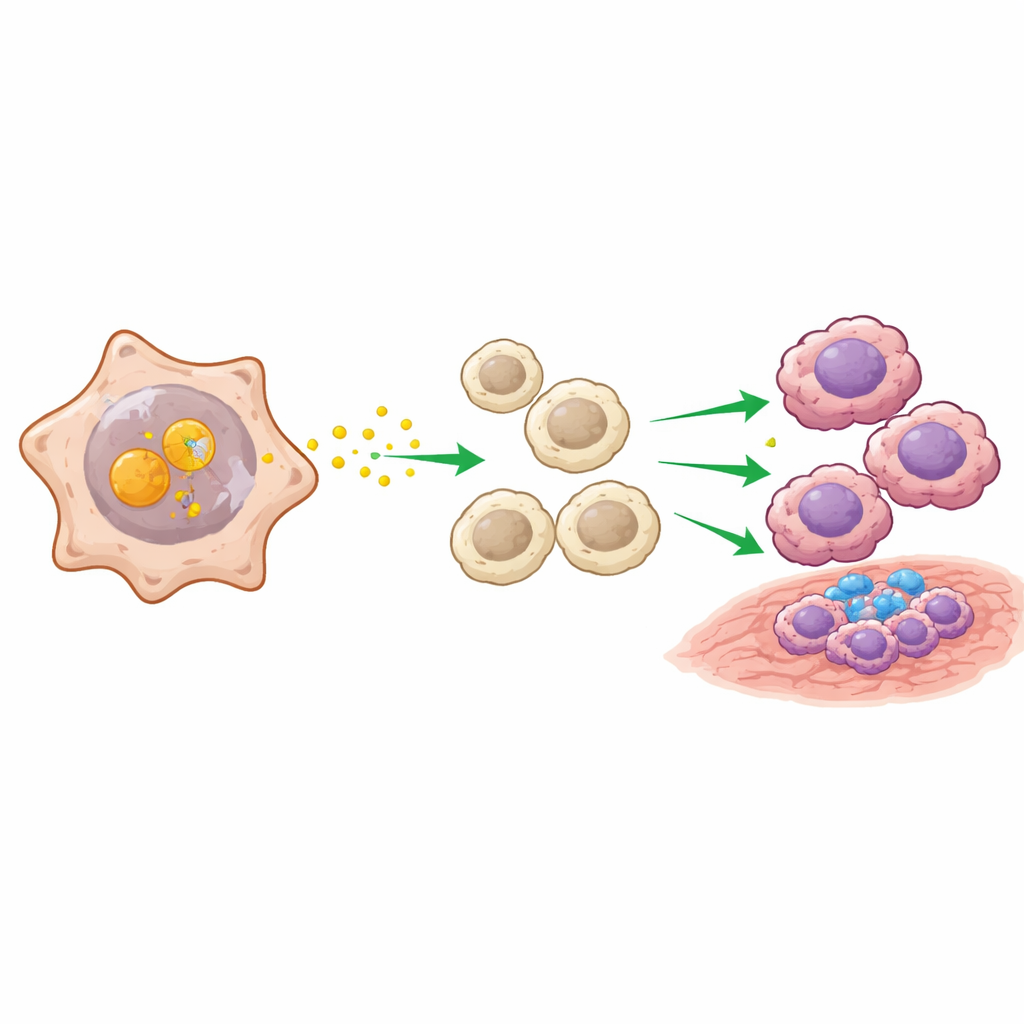
Sıradaki soru, ENO2-pozitif kanser hücrelerinin çevrelerini nasıl etkilediğiydi. Hücre tipleri arasındaki sinyalleşmeyi çıkaran hesaplamalı araçlar kullanılarak, ENO2 bakımından zengin tümör hücrelerinin özellikle MIF adlı bir proteini içeren yol aracılığıyla büyük “yayın merkezleri” gibi davrandığı bulundu. ENO2’nin kanser hücreleri içinde MIF’e fiziksel olarak bağlandığı ve MIF’in yok edilmek üzere etiketlenmesinden koruyarak birikmesine izin verdiği keşfedildi. Bu da, tümör hücrelerinde büyüme ve hayatta kalma yollarını aktif hale getiriyor ve yakındaki makrofajlara—tümörlere saldırabilen (M1-benzeri) veya M2-benzeri formunda tümör büyümesini destekleyip diğer bağışıklık yanıtlarını baskılayabilen bağışıklık hücrelerine—güçlü sinyaller gönderiyordu. Eş kültür deneylerinde ve hayvan modellerinde ENO2 yüksek olan kanser hücreleri tutarlı şekilde makrofajları bu tümöre yardımcı M2 durumuna yönlendirdi.
Mekanizmadan potansiyel bir ilaca
Bu mekanistik anlayışla ekip, ENO2–MIF ortaklığını bozabilecek bir ilaç aradı. 6.000’den fazla küçük molekülün bilgisayar destekli taramasını ve ardından laboratuvar testlerini takiben, pyrithioxin adlı bileşiği ENO2 ile MIF arasındaki temas bölgesine giren bir madde olarak belirlediler. Kanser hücrelerinde pyrithioxin, etkileşimi bozdu, MIF’in parçalanmasını geri getirdi ve aşağı yönlü büyüme sinyallerini zayıflattı. Kolon kanseri hücrelerinin karaciğer metastazlarını oluşturmak üzere enjekte edildiği fare modellerinde oral pyrithioxin tedavisi, karaciğerdeki tümörlerin sayısını ve boyutunu keskin şekilde azalttı ve metastatik bölgelerde M2-benzeri makrofaj belirteçlerini düşürdü.
Bu hastalar için ne anlama geliyor
Basitçe ifade etmek gerekirse, bu çalışma tek bir enzim olan ENO2’nin, sinyal proteini MIF’i yok edilmekten koruyarak kolon kanseri hücrelerinin yakınlardaki bağışıklık hücrelerini karaciğerde besleyici, tümörü destekleyen bir role “yeniden programlamasına” yardımcı olduğunu ortaya koyuyor. Bu, bağışıklık baskılama ve metastatik büyümenin kendini güçlendiren bir döngüsünü yaratıyor. ENO2–MIF etkileşiminin engellenmesinin farelerde karaciğer metastazlarını küçültebildiğini göstererek, çalışma yalnızca kanser hücrelerine doğrudan saldırmak yerine, onların bağışıklık sistemini suç ortağına dönüştürmelerine olanak veren gizli konuşmaları bozmanın umut verici bir tedavi stratejisi olduğunu vurguluyor.
Atıf: Tang, J., Chen, Z., Zhang, D. et al. ENO2 drives tumor cell-induced M2 macrophage polarization to promote colorectal cancer liver metastasis. Sig Transduct Target Ther 11, 166 (2026). https://doi.org/10.1038/s41392-026-02732-2
Anahtar kelimeler: kolorektal kanser karaciğer metastazı, tümör mikroçevresi, makrofaj polarizasyonu, ENO2 MIF ekseni, kanser immünoterapisi