Clear Sky Science · he
ENO2 ממריץ קיבוע מאקרופאגים במצב M2 המושרה על־ידי תאים סרטניים לקידום גרורות כבדיות של סרטן המעי הגס
מדוע מחקר זה חשוב
כאשר סרטן המעי הגס מתפשט אל הכבד, הוא נעשה הרבה יותר קשה לטיפול ומהווה את הסיבה העיקרית למותם של מטופלים רבים. המחקר חוקר שאלה בסיסית עם השלכות קליניות גדולות: כיצד תאי הגידול משכנעים את תאי המערכת החיסונית של הגוף לשנות צד ולעזור לסרטן לשרוד ולהתפתח בכבד? על־ידי זיהוי חלבון בודד בתא הסרטני שמניע את הברית המזיקה הזו, העבודה פותחת אפשרות לגישה טיפולית ממוקדת חדשה.
מבט מעמיק על גידולים של המעי הגס שמתפשטים לכבד
החוקרים התחילו בבניית "מפת תאים" מפורטת של סרטן המעי הגס שגרם לגרורות בכבד, והשוו אותה עם גידולים שלא התפשטו. באמצעות רצף RNA בתא יחיד הם ניתחו אלפי תאים בודדים מתוך גידולים ראשוניים של המעי, מרקמות סמוכות תקינות וגרורות בכבד. הם מצאו שתאי הסרטן בגרורות הכבד מראים חוסר יציבות גנטית גדול יותר, מתחלקים בקצב מהיר יותר ומותאמים יותר לתנאי חוסר חמצן בהשוואה לתאים בגידול הראשוני במעי. ממצא זה אישר שגרורות כבדיות אינן רק העתקים של הגידול הראשוני, אלא מכילות אוכלוסיית תאים סרטניים אגרסיבית וחסינת הישרדות.
זיהוי תת־אוכלוסייה סרטנית מסוכנת
כדי להבין אילו תאים סרטניים מוכנים להתפשט, הקבצה של תאי הגידול נעשתה על בסיס דפוסי ביטוי גנים משותפים. מודול גנים אחד בלט, והוא נקשר להישרדות גרועה של מטופלים. בתוכו, תת־אוכלוסייה של תאים הציגה תוכנית עוצמתית של "החלפת אפיתל–מזנכימה" (EMT), שמסייעת לתאים להשתחרר ולהנדוד. מבין עשרה גנים מועמדים מובילים במודול הזה, אנזים אחד — ENO2 — נקשר באופן ייחודי לתוצאות גרועות. מטופלים שלגידוליהם היה ביטוי ENO2 גבוה חיו זמן קצר יותר באופן מובהק, וקבוצות מטופלים בלתי תלויות אישרו כי ENO2 היה מוגבר הן בגידולים הראשוניים והן בגרורות הכבד בהשוואה לרקמה תקינה.
כיצד הגידולים מאמנים תאי חיסון לעזור להם
השאלה הבאה הייתה כיצד תאי סרטניים חיוביים ל‑ENO2 משפיעים על סביבתם. באמצעות כלים חישוביים שמסיקים איתות בין סוגי תאים, החוקרים גילו שתאי גידול עשירים ב‑ENO2 פועלים כ"מרכזי שידור" חשובים, במיוחד דרך מסלול הכולל את החלבון MIF. הם גילו כי ENO2 נקשר פיזית ל‑MIF בתוך תאי הסרטן ומגן עליו מפני סימון להרס, מה שמאפשר ל‑MIF להצטבר. זה, בתורו, מפעיל מסלולי גדילה והישרדות בתאי הגידול ומשדר אותות חזקים למאקרופאגים סמוכים — תאי חיסון שיכולים לתקוף גידולים (מצב M1־דומה) או, בצורתם הדומה ל‑M2, לתמוך בצמיחת הגידול ולדכא תגובות חיסוניות אחרות. בניסויי תרבית משותפת ובמודלים בחיות מעבדה, תאי גידול עם רמות גבוהות של ENO2 דחפו בעקביות את המאקרופאגים לעבר מצב M2 התומך בגידול.
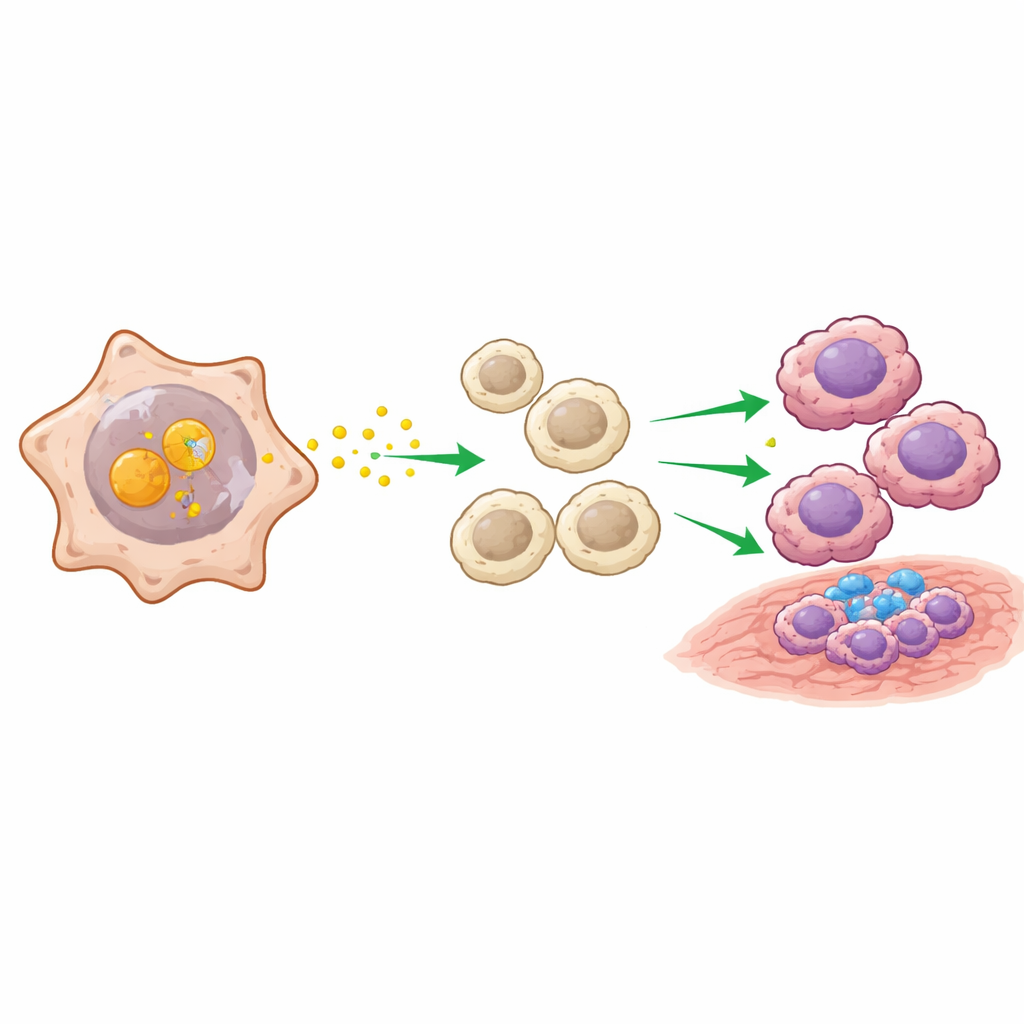
ממנגנון לתרופה פוטנציאלית
מצוידים בתובנה המנגנונית הזו, הקבוצה חיפשה תרופה שיכולה לשבור את שותפות ENO2–MIF. באמצעות סינון ממוחשב של יותר מ‑6,000 מולקולות קטנות, ולאחר בדיקות מעבדה, זוהה הפריתיוקסין (pyrithioxin) כחומר החודר לאתר המגע בין ENO2 ל‑MIF. בתוך תאי הסרטן, הפריתיוקסין הפריע לאינטראקציה ביניהם, החזיר את פירוקו של MIF והחליש אותות גדילה מטה־זרם. במודלים עכבריים שבהם הוזרקו תאי סרטן מעי כדי לגרום לגרורות כבדיות, טיפול אוראלי בפריתיוקסין הקטין באופן דרמטי את מספר וגודל הגרעומים הכבדיים והוריד סמני מאקרופאגים בדמיון M2 באתרים המטסטטיים.
מה משמעות הדבר עבור מטופלים
בקצרה, המחקר מראה כי אנזים יחיד — ENO2 — מסייע לתאי סרטן מעי "לשכתב" תאי חיסון סמוכים לתפקיד מטפח ותומך בגידול בכבד על‑ידי הגנה על חלבון האות MIF מפני פירוק. זה יוצר לופ מחזק של דיכוי חיסוני וגדילה מטסטטית. בכך שהראו שחסימה של האינטראקציה בין ENO2 ל‑MIF יכולה להקטין גרורות כבדיות בעכברים, העבודה מציגה אסטרטגיית טיפולית מבטיחה חדשה: במקום לתקוף רק את תאי הסרטן ישירות, לשבש את השיחות הסמויות שמאפשרות להם להפוך את מערכת החיסון לשותפה לפשע.
ציטוט: Tang, J., Chen, Z., Zhang, D. et al. ENO2 drives tumor cell-induced M2 macrophage polarization to promote colorectal cancer liver metastasis. Sig Transduct Target Ther 11, 166 (2026). https://doi.org/10.1038/s41392-026-02732-2
מילות מפתח: גרורות כבדיות של סרטן המעי הגס, מיקרו־סביבת הגידול, קוטביות מאקרופאגים, ציר ENO2–MIF, אימונותרפיה של סרטן