Clear Sky Science · zh
用于探索星形胶质细胞驱动的神经病理学、具突触隔离神经网络的微流控共培养系统
大脑支持细胞如何悄然扩散问题
当大脑细胞生病时,损伤很少局限在单一位置。本研究揭示了星形胶质细胞——大脑中呈星形的支持细胞——如何在不声张的情况下将有害信号从一组神经元传到另一组。研究者用一个微型的实验室芯片重建了一个简化的脑回路,以观察某一角落的压力如何波及到从未直接遭受原始伤害的邻近区域。
模拟大脑社区的微小迷宫
团队构建了一个掌心大小的微流控装置,像一座供脑细胞活动的微型城市。两个独立腔室容纳不同的神经元群体,中间通道则用于星形胶质细胞。区域间有一组狭窄通道,允许星形胶质细胞穿过,但阻挡神经元的长轴突。通过精确控制相连储液池的液位,研究者能在设定时间内保持每个室的化学环境隔离,从而确保神经元群体间的任何交流必须通过星形胶质细胞层进行,而非通过直接突触接触或共享液体。
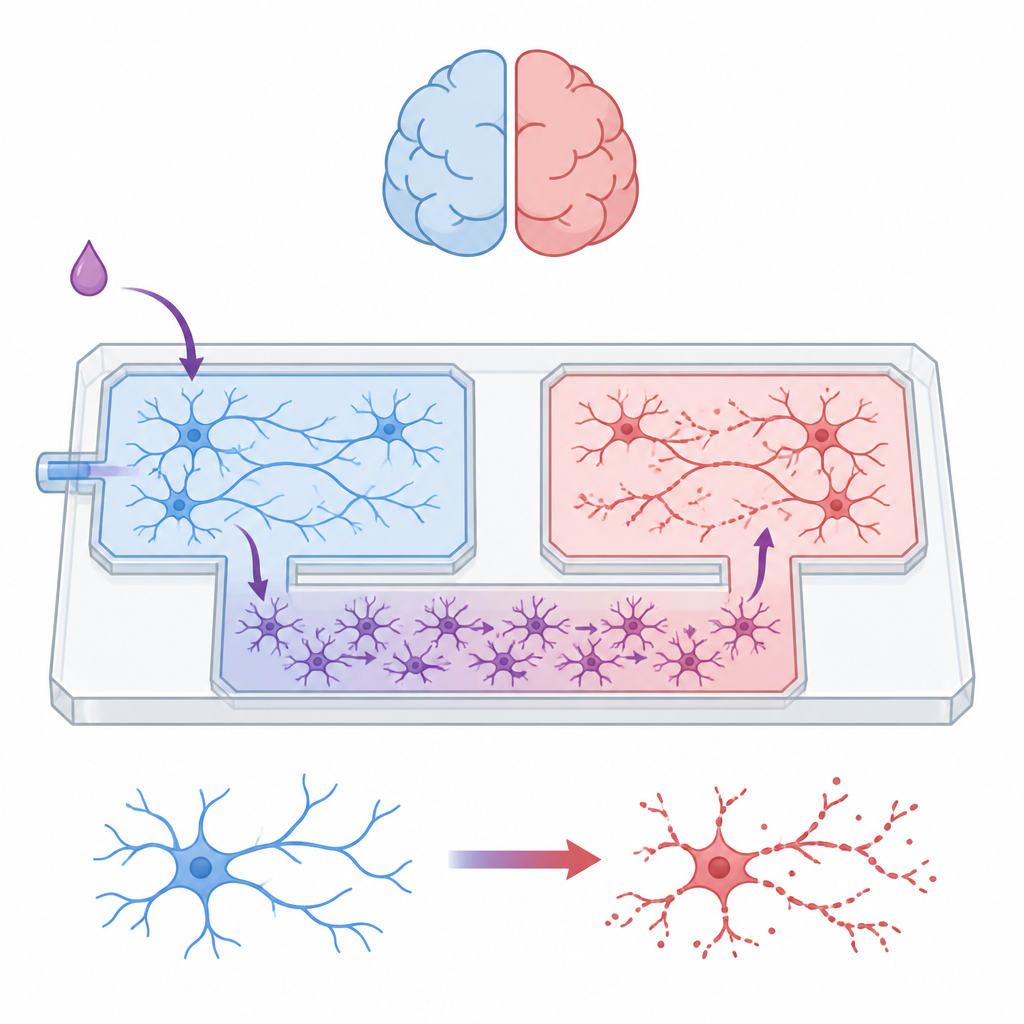
让“帮手”游走同时围拦神经元
星形胶质细胞在装置中快乐生长,形成了一层连续的细胞毯,横跨迷宫并延伸进各个腔室。相比之下,神经元被限制在各自区域。测试显示,当神经元的树突尝试穿越迷宫时,其数量在每个障碍处显著下降,且没有任何神经元达到仅含星形胶质细胞的通道。对不同区域的蛋白质谱分析证实了这种物理分离:混合的神经元—星形胶质细胞腔室中富含与神经生长、突触和电活动相关的蛋白,而仅含星形胶质细胞的区域显示出代谢和类免疫功能的特征,这些是胶质细胞的典型标志。综上结果表明,该装置既能容纳复杂的混合网络,又能将细胞类型和信号清晰分隔。
观察有毒信号跨越空隙
在建立该平台后,研究者探究星形胶质细胞是否能在隔离的神经元群体间传播“兴奋性毒性”压力。他们仅在一侧的神经元—星形胶质细胞腔室施加诱发癫痫的毒素卡因酸,同时维持流体隔离。15分钟内,受处理一侧的神经树突出现串珠状肿胀,这是损伤的标志。令人惊讶的是,未受触及的一侧神经元群体中也很快出现了类似的串珠,即使两腔室之间没有直接的神经元对神经元连接或共享液体。当相同毒素施加到没有星形胶质细胞共培养的神经元时,损伤保持局部,表明星形胶质细胞在传播病理过程中是关键的。
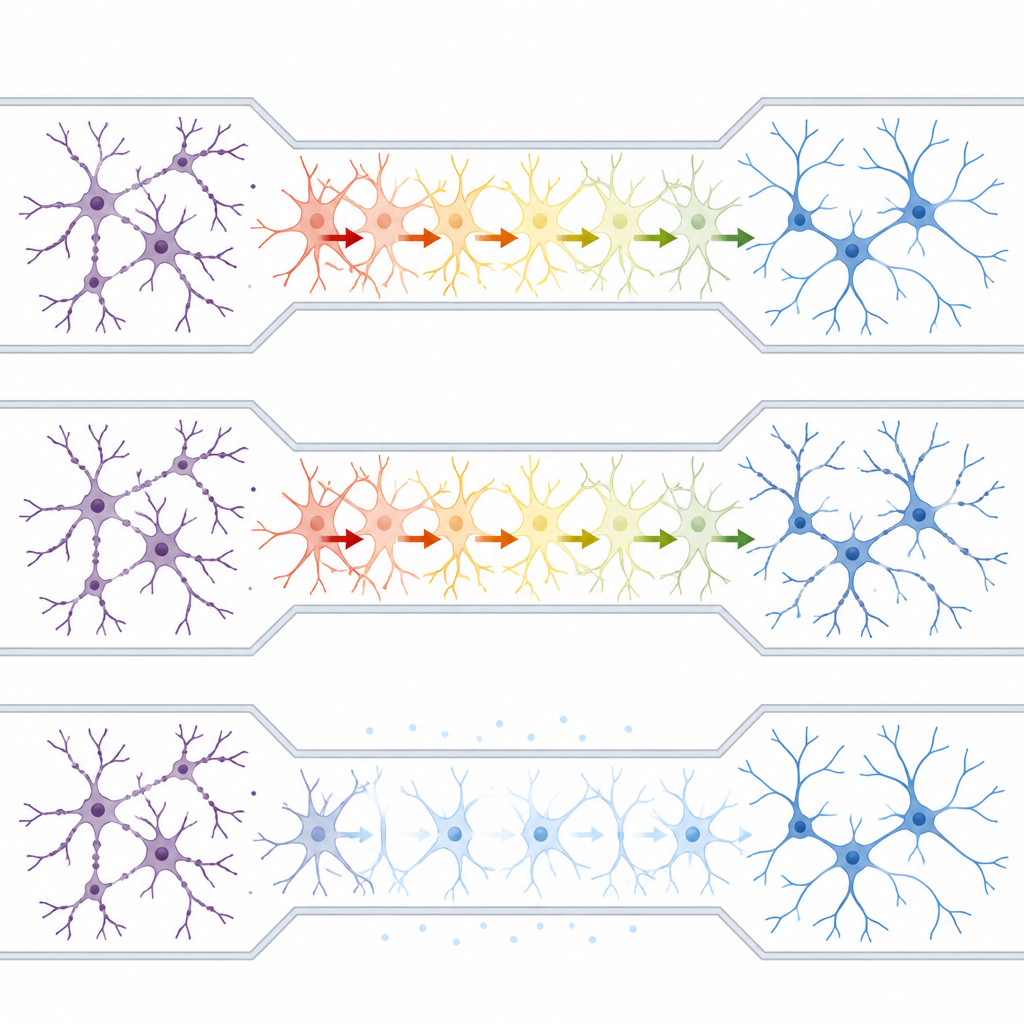
星形胶质细胞中的钙波作为隐秘使者
星形胶质细胞通过细胞内的钙波进行交流。团队使用荧光钙指示剂追踪这些变化,发现一侧受毒素刺激会在中央通道的星形胶质细胞中触发升高的钙信号。用一种可穿膜的螯合剂阻断星形胶质细胞内的钙后,这些钙波减弱,直接暴露的神经元损伤减少,并且重要的是,远端神经元群体的损伤传播被阻止。有趣的是,单独完全抑制星形胶质细胞的钙活动本身也会损害神经元,这表明这些细胞的正常钙活动有助于维持健康的网络功能,而过度的钙则可能推动类似疾病的过程。
这对脑疾病和疗法测试意味着什么
这项工作引入了一个多用途的大脑芯片系统,能够在保持神经元与星形胶质细胞现实接触的同时,分隔、连接并独立处理不同的脑细胞群体。研究显示,星形胶质细胞能通过依赖钙的机制在被切断的神经元群体之间传递兴奋性毒性压力。对非专业读者而言,关键信息是:大脑的支持细胞并非被动旁观者——它们能放大和传播损伤,同时也是潜在的保护性干预目标。该平台为探究这些角色并测试旨在平抑有害星形胶质细胞信号的未来疗法提供了一个可控的方法,适用于癫痫、中风和神经退行性疾病等病症的研究。
引用: Yap, Y.C., Musgrove, R.E., Breadmore, M.C. et al. Microfluidic co-culture system for synaptically segregated neural networks to explore astrocyte-driven neural pathology. Microsyst Nanoeng 12, 181 (2026). https://doi.org/10.1038/s41378-026-01187-3
关键词: 星形胶质细胞, 微流控大脑芯片, 兴奋性毒性, 神经元-胶质细胞相互作用, 钙信号