Clear Sky Science · de
Mikrofluidisches Ko-Kultursystem für synaptisch getrennte neuronale Netzwerke zur Erforschung astrozytär getriebener neuronaler Pathologie
Wie Unterstützerzellen im Gehirn stillschweigend Probleme verbreiten können
Wenn Gehirnzellen erkranken, bleibt der Schaden selten auf einen Ort beschränkt. Diese Studie zeigt, wie Astrozyten, die sternförmigen Stützzellen des Gehirns, schädliche Signale von einer Gruppe von Nervenzellen zur nächsten tragen können. Mithilfe eines winzigen Lab-on-a-Chip rekonstruierten die Forschenden einen vereinfachten Hirnkreis, um zu beobachten, wie Stress in einer Ecke wellenartig auf benachbarte Regionen überspringt, die nie der ursprünglichen Schädigung ausgesetzt waren.
Ein winziges Labyrinth, das Hirnnachbarschaften nachbildet
Das Team baute ein handtellergroßes mikrofluidisches Gerät, das wie eine Miniaturstadt für Gehirnzellen funktioniert. Zwei getrennte Kammern beherbergen unterschiedliche Neuronpopulationen, während eine zentrale Spur für Astrozyten reserviert ist. Dazwischen liegt ein Labyrinth aus engen Kanälen, das Astrozyten durchschlüpfen lässt, aber die langen Nervenfasern der Neuronen blockiert. Durch sorgfältige Kontrolle der Flüssigkeitsstände in verbundenen Reservoiren konnten die Forschenden die chemische Umgebung in jedem Bereich für definierte Zeiträume isoliert halten, sodass jede Kommunikation zwischen den Neuronengruppen über die Astrozytenschicht und nicht durch direkte synaptische Kontakte oder gemeinsames Medium erfolgen musste.
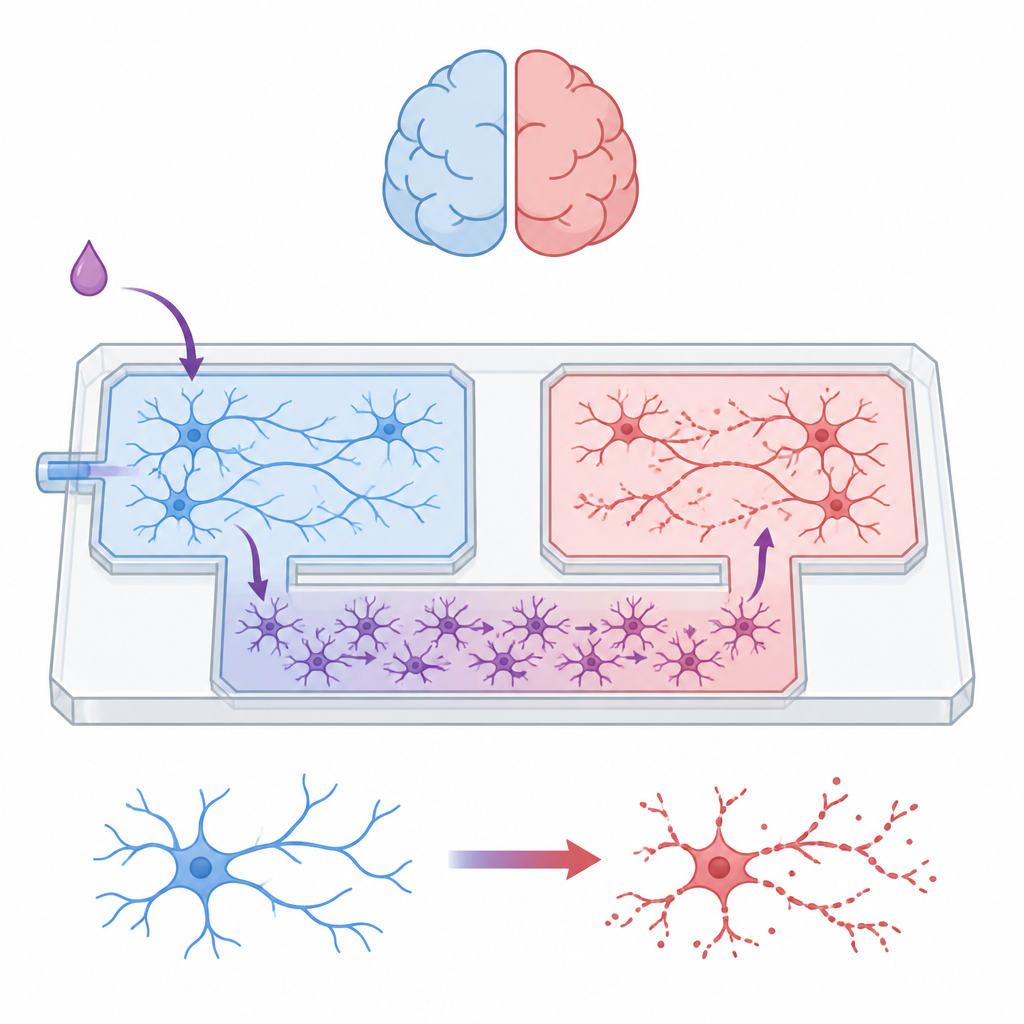
Helfer frei herumlaufen lassen, Neuronen einzäunen
Astrozyten wuchsen gut im gesamten Gerät und bildeten einen durchgehenden Teppich, der sich durchs Labyrinth bis in alle Kammern erstreckte. Neuronen blieben dagegen eingeschränkt. Tests zeigten, dass die Zahl der Neuriten beim Versuch, das Labyrinth zu überqueren, an jeder Barriere stark abnahm und keine in die astrozyten-exklusive Spur vordrang. Proteinprofilierungen der verschiedenen Bereiche bestätigten diese physische Trennung: Die gemischten Neuron–Astrozyten-Kammern waren angereichert mit Proteinen, die mit Nervenwachstum, Synapsen und elektrischer Signalgebung assoziiert sind, während der astrozyten-only Bereich Signaturen von Stoffwechsel- und immunähnlichen Funktionen zeigte, wie sie für Gliazellen typisch sind. Zusammen zeigten diese Ergebnisse, dass das Gerät komplexe, gemischte Netzwerke beherbergen kann und gleichzeitig Zelltypen und Signale sauber getrennt hält.
Beobachtung, wie toxische Signale die Lücke überspringen
Mit dieser Plattform untersuchten die Forschenden, ob Astrozyten „exzitotoxischen“ Stress zwischen isolierten Neuronengruppen übertragen können. Sie applizierten Kainsäure, eine anfallsinduzierende Verbindung, nur in einer Neuron–Astrozyten-Kammer, während die fluidische Isolation erhalten blieb. Innerhalb von 15 Minuten zeigten die Nervenäste auf der behandelten Seite perlenartige Schwellungen, ein Kennzeichen von Schaden. Überraschenderweise traten ähnliche Perlenbildungen bald auch in der unbehandelten Neuronengruppe auf der anderen Seite des Labyrinths auf, obwohl keine direkten Neuron-zu-Neuron-Verbindungen oder gemeinsames Medium zwischen den Kammern bestanden. Wurde dasselbe Toxin an Neuronen ohne Astrozyten angewendet, blieb der Schaden lokal, was darauf hindeutet, dass Astrozyten für die Ausbreitung der Pathologie erforderlich sind.
Calciumwellen in Astrozyten als versteckter Bote
Astrozyten kommunizieren über Calciumwellen innerhalb ihrer Zellen. Das Team nutzte einen fluoreszenten Calciumindikator, um diese Veränderungen zu verfolgen, und fand heraus, dass die Toxinexposition auf einer Seite des Geräts erhöhte Calciumsignale in Astrozyten der zentralen Spur auslöste. Das Blockieren von Astrozyten-Calcium mit einem membrangängigen Chelator dämpfte diese Wellen, verringerte den Schaden an den direkt exponierten Neuronen und verhinderte wichtig: die Ausbreitung der Verletzung zur entfernten Neuronengruppe. Interessanterweise schadete das vollständige Stilllegen des Astrozyten-Calciums allein den Neuronen, was darauf hindeutet, dass normale Calciumaktivität in diesen Zellen gesunde Netzwerkfunktionen unterstützt, während übermäßiges Calcium krankheitsähnliche Prozesse fördert.
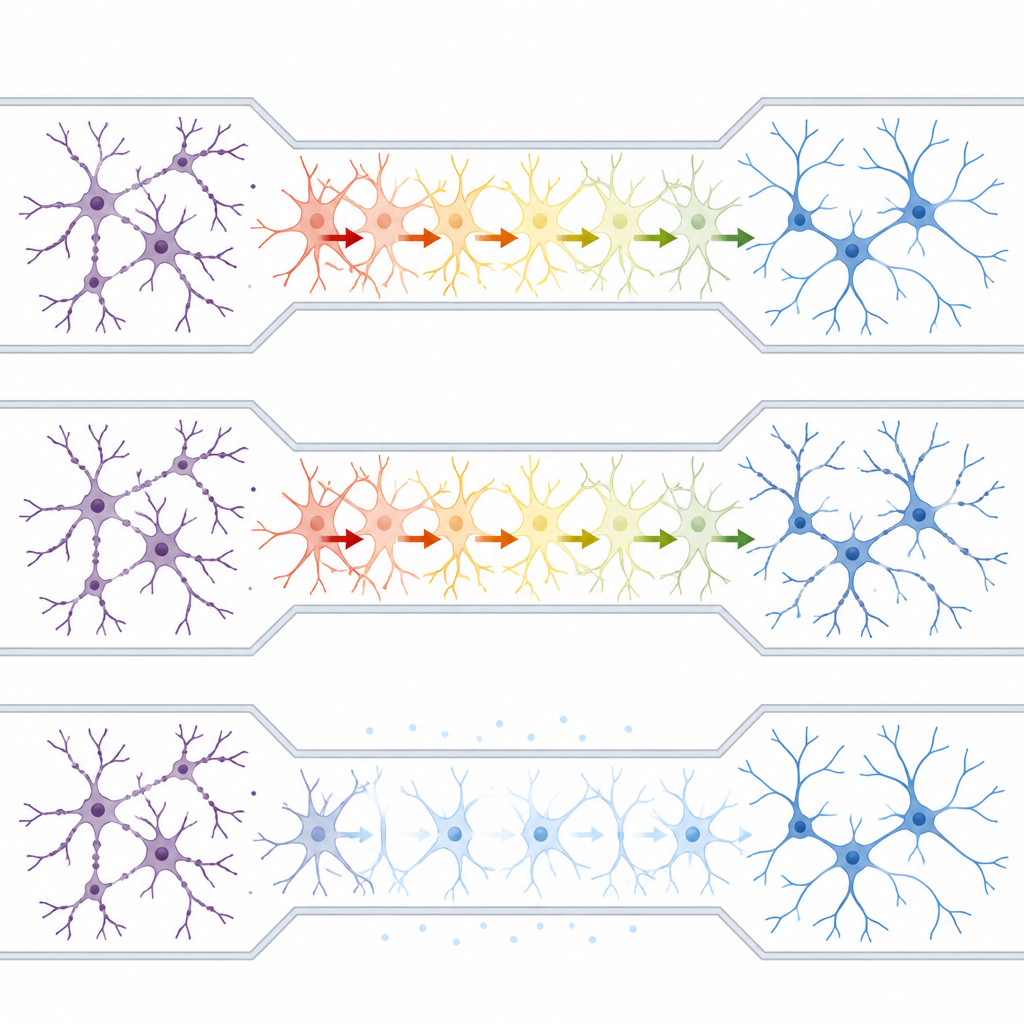
Warum das für Hirnerkrankungen und Therapie-Tests wichtig ist
Diese Arbeit stellt ein vielseitiges Brain-on-a-Chip-System vor, das verschiedene Gehirnzellpopulationen trennen, verbinden und unabhängig behandeln kann, während es dennoch realistische Kontakte zwischen Neuronen und Astrozyten erlaubt. Sie zeigt, dass Astrozyten excitotoxischen Stress zwischen Neuronengruppen über einen calciumabhängigen Mechanismus weiterleiten können, selbst wenn die Neuronen selbst voneinander abgeschnitten sind. Für Nicht-Spezialisten lautet die Kernbotschaft: Unterstützerzellen im Gehirn sind keine passiven Beobachter – sie können Schäden verstärken und verbreiten, bieten aber zugleich ein Ziel für schützende Behandlungen. Diese Plattform liefert einen kontrollierten Weg, diese Rollen zu untersuchen und künftige Therapien zu testen, die darauf abzielen, schädliche Astrozyten-Signale bei Erkrankungen wie Epilepsie, Schlaganfall und neurodegenerativen Erkrankungen zu dämpfen.
Zitation: Yap, Y.C., Musgrove, R.E., Breadmore, M.C. et al. Microfluidic co-culture system for synaptically segregated neural networks to explore astrocyte-driven neural pathology. Microsyst Nanoeng 12, 181 (2026). https://doi.org/10.1038/s41378-026-01187-3
Schlüsselwörter: Astrozyten, mikrofluidischer Gehirnchip, Exzitotoxizität, Neuron-Glia-Interaktionen, Calcium-Signalgebung