Clear Sky Science · fr
Système de co-culture microfluidique pour réseaux neuronaux synaptiquement séparés afin d’explorer la pathologie neuronale conduite par les astrocytes
Comment les cellules de soutien du cerveau peuvent discrètement propager des problèmes
Quand des cellules cérébrales tombent malades, les dégâts restent rarement localisés. Cette étude révèle comment les astrocytes, ces cellules de soutien en forme d’étoile du cerveau, peuvent silencieusement transporter des signaux nocifs d’un groupe de neurones à un autre. À l’aide d’un petit lab-on-a-chip, les chercheurs ont recréé un circuit cérébral simplifié pour observer comment le stress dans un coin peut se répercuter sur des régions voisines qui n’ont jamais subi l’agression initiale.
Un micro-labyrinthe qui mime les quartiers du cerveau
L’équipe a construit un dispositif microfluidique de la taille de la paume qui agit comme une mini-cité pour cellules cérébrales. Deux chambres séparées hébergent des populations neuronales distinctes, tandis qu’une voie centrale est réservée aux astrocytes. Entre ces zones, un réseau de canaux étroits permet aux astrocytes de se faufiler mais bloque les longues fibres nerveuses des neurones. En contrôlant soigneusement les niveaux de liquide dans des réservoirs connectés, les chercheurs ont pu maintenir l’isolement chimique de chaque compartiment pendant des périodes définies, garantissant que toute communication entre les groupes de neurones devait passer par la couche d’astrocytes plutôt que par un contact synaptique direct ou un liquide partagé.
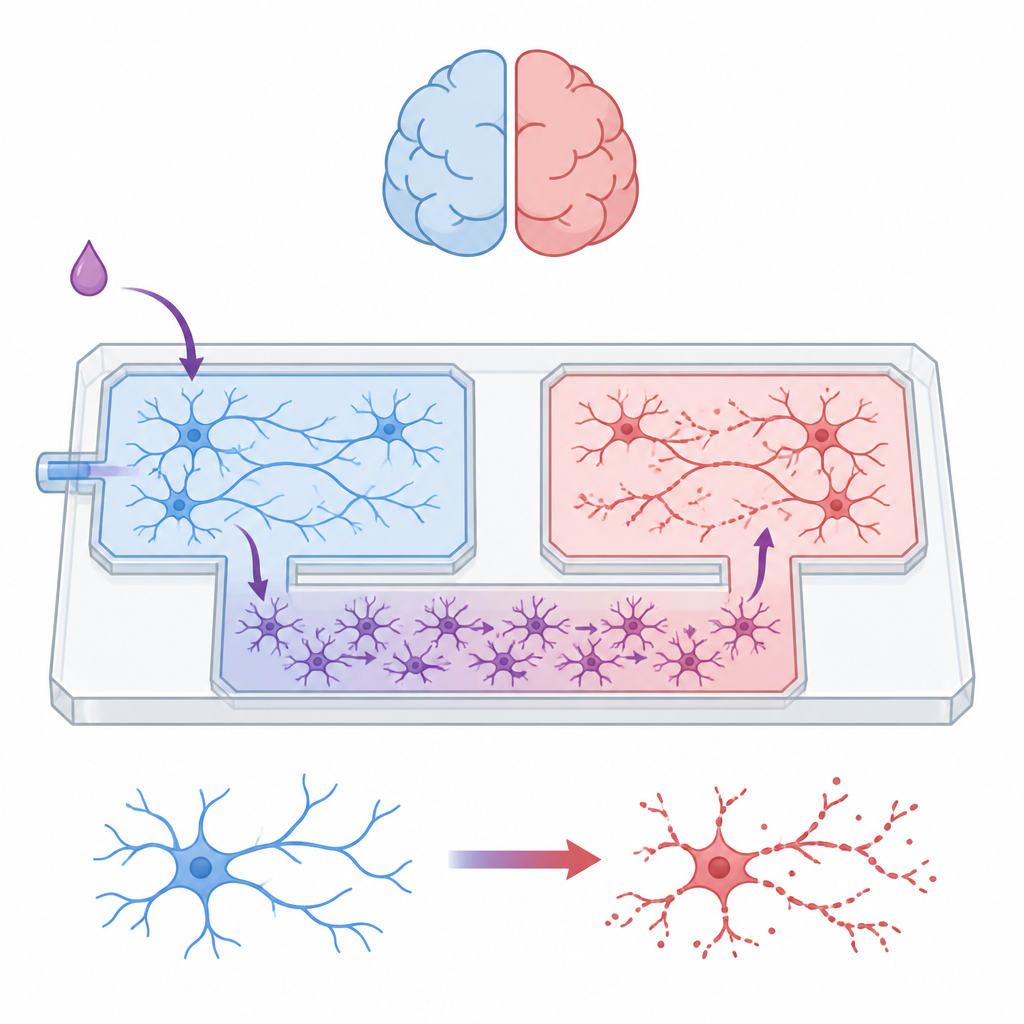
Laisser les auxiliaires se déplacer tout en confinant les neurones
Les astrocytes se sont développés harmonieusement dans tout le dispositif, formant un tapis continu qui s’étendait à travers le labyrinthe et dans toutes les chambres. Les neurones, en revanche, sont restés confinés. Des tests ont montré que, lorsque leurs prolongements tentaient de traverser le labyrinthe, leur nombre chutait fortement à chaque obstacle, et aucun n’atteignait la voie réservée aux astrocytes. Le profilage protéique des différentes régions a confirmé cette séparation physique : les chambres mixtes neurone–astrocyte étaient enrichies en protéines liées à la croissance nerveuse, aux synapses et à la signalisation électrique, tandis que la zone réservée aux astrocytes présentait des signatures métaboliques et des fonctions de type immunitaire typiques des cellules gliales. Ensemble, ces résultats montrent que le dispositif peut héberger des réseaux mixtes complexes tout en maintenant une séparation nette des types cellulaires et des signaux.
Observer les signaux toxiques franchir l’écart
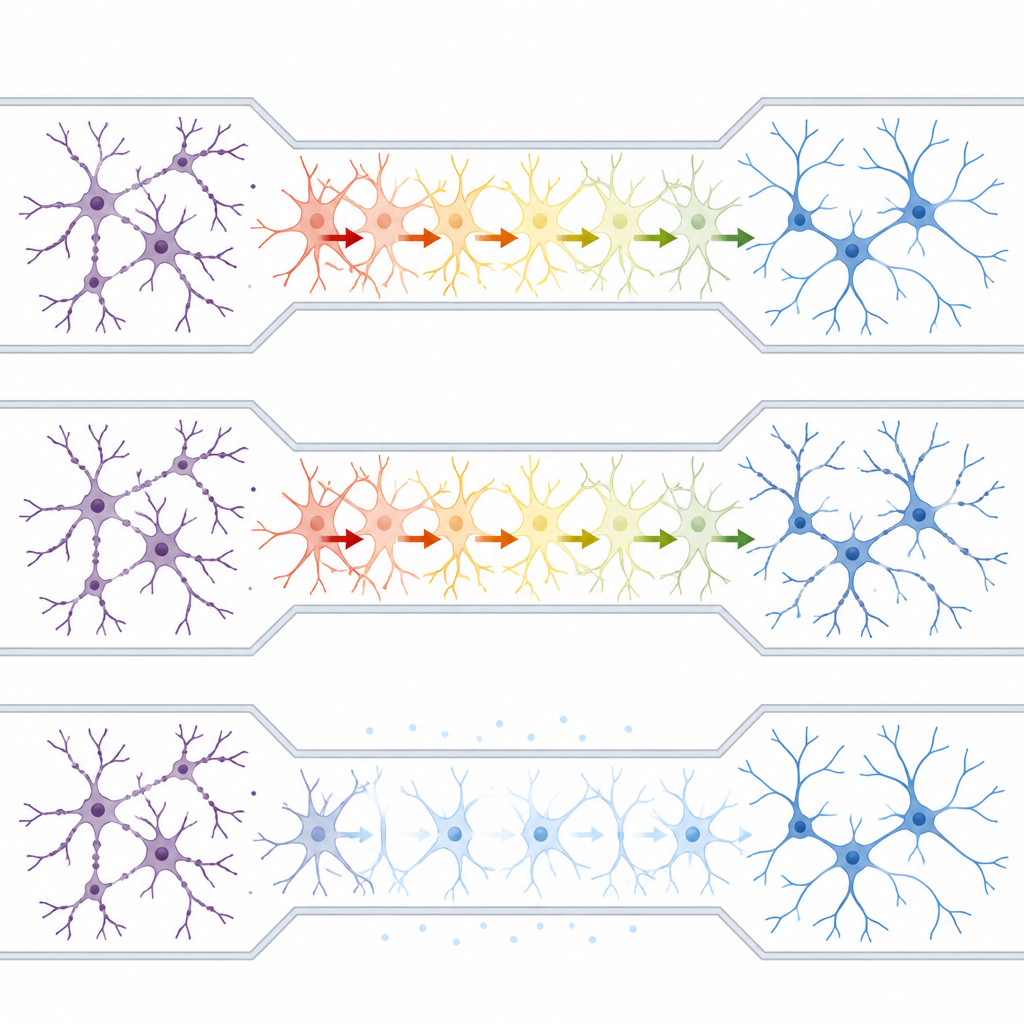
Avec cette plateforme en place, les chercheurs se sont demandé si les astrocytes pouvaient transporter un stress « excitotoxique » entre des groupes de neurones isolés. Ils ont appliqué de l’acide kainique, un composé provoquant des crises, à une seule chambre neurone–astrocyte tout en maintenant l’isolation fluidique. En moins de 15 minutes, les branches nerveuses du côté traité ont développé des renflements en perles, marqueur caractéristique de dommage. De façon surprenante, un phénomène de perlage similaire est rapidement apparu dans le groupe de neurones intact de l’autre côté du labyrinthe, bien qu’il n’existât aucune connexion directe neurone–neurone ni liquide partagé entre les chambres. Lorsque le même toxique a été appliqué à des neurones cultivés sans astrocytes, les dommages sont restés locaux, indiquant que les astrocytes étaient essentiels à la propagation de la pathologie.
Les ondes de calcium dans les astrocytes comme messager caché
Les astrocytes communiquent via des ondes de calcium intracellulaires. L’équipe a utilisé un indicateur fluorescent du calcium pour suivre ces changements et a constaté que l’exposition au toxique d’un côté du dispositif déclenchait des signaux calciques élevés chez les astrocytes de la voie centrale. Le blocage du calcium astrocytaire avec un chélateur membrane-perméable a atténué ces ondes, réduit les dommages chez les neurones directement exposés et, surtout, empêché la propagation de la lésion vers le groupe neuronal distant. Fait intéressant, l’inhibition complète du calcium astrocytaire à elle seule nuisait aux neurones, ce qui suggère que l’activité calcique normale de ces cellules soutient le fonctionnement sain du réseau, tandis qu’un excès de calcium contribue aux processus pathologiques.
Pourquoi cela compte pour les maladies du cerveau et le test des traitements
Ce travail présente un système polyvalent de cerveau sur puce qui peut séparer, connecter et traiter indépendamment différentes populations cellulaires cérébrales tout en permettant un contact réaliste entre neurones et astrocytes. Il montre que les astrocytes peuvent relayer un stress excitotoxique entre groupes de neurones via un mécanisme dépendant du calcium, même lorsque les neurones eux-mêmes sont isolés les uns des autres. Pour le grand public, le message clé est que les cellules de soutien du cerveau ne sont pas de simples spectatrices : elles peuvent amplifier et propager les dommages, mais aussi constituer une cible pour des traitements protecteurs. Cette plateforme offre un moyen contrôlé d’étudier ces rôles et de tester de futures thérapies visant à calmer les signaux astrocytaires nocifs dans des affections telles que l’épilepsie, l’accident vasculaire cérébral et les maladies neurodégénératives.
Citation: Yap, Y.C., Musgrove, R.E., Breadmore, M.C. et al. Microfluidic co-culture system for synaptically segregated neural networks to explore astrocyte-driven neural pathology. Microsyst Nanoeng 12, 181 (2026). https://doi.org/10.1038/s41378-026-01187-3
Mots-clés: astrocytes, puce cérébrale microfluidique, excitotoxicité, interactions neurone-glie, signalisation calcique