Clear Sky Science · nl
Microfluidisch co-cultuursysteem voor synaptisch gesegregeerde netwerken om astrocyt-gedreven neurale pathologie te onderzoeken
Hoe ondersteunende hersencellen ongemerkt problemen kunnen verspreiden
Wanneer hersencellen ziek worden, blijft de schade zelden op één plek. Deze studie laat zien hoe astrocyten, de stervormige ondersteunende cellen van de hersenen, schadelijke signalen stilletjes van de ene groep zenuwcellen naar de andere kunnen dragen. Met een kleine lab-on-a-chip recreëerden de onderzoekers een vereenvoudigd hersencircuit om te observeren hoe stress in één hoek kan doorwerken naar naburige regio’s die de oorspronkelijke aantasting nooit direct ondergaan.
Een klein doolhof dat hersenbuurten nabootst
Het team bouwde een palmgroot microfluidisch apparaat dat fungeert als een miniatuurstad voor hersencellen. Twee afzonderlijke kamers herbergen verschillende neuronpopulaties, terwijl een centrale baan is gereserveerd voor astrocyten. Tussen deze gebieden ligt een netwerk van smalle kanaaltjes dat astrocyten doorlaat maar de lange zenuwvezels van neuronen blokkeert. Door de vloeistofniveaus in verbonden reservoirs nauwkeurig te regelen, konden de onderzoekers de chemische omgeving in elk compartiment gedurende bepaalde perioden geïsoleerd houden, wat ervoor zorgde dat elke communicatie tussen neurongroepen via de astrocytlaag moest verlopen en niet via directe synaptische verbindingen of gedeelde vloeistof.
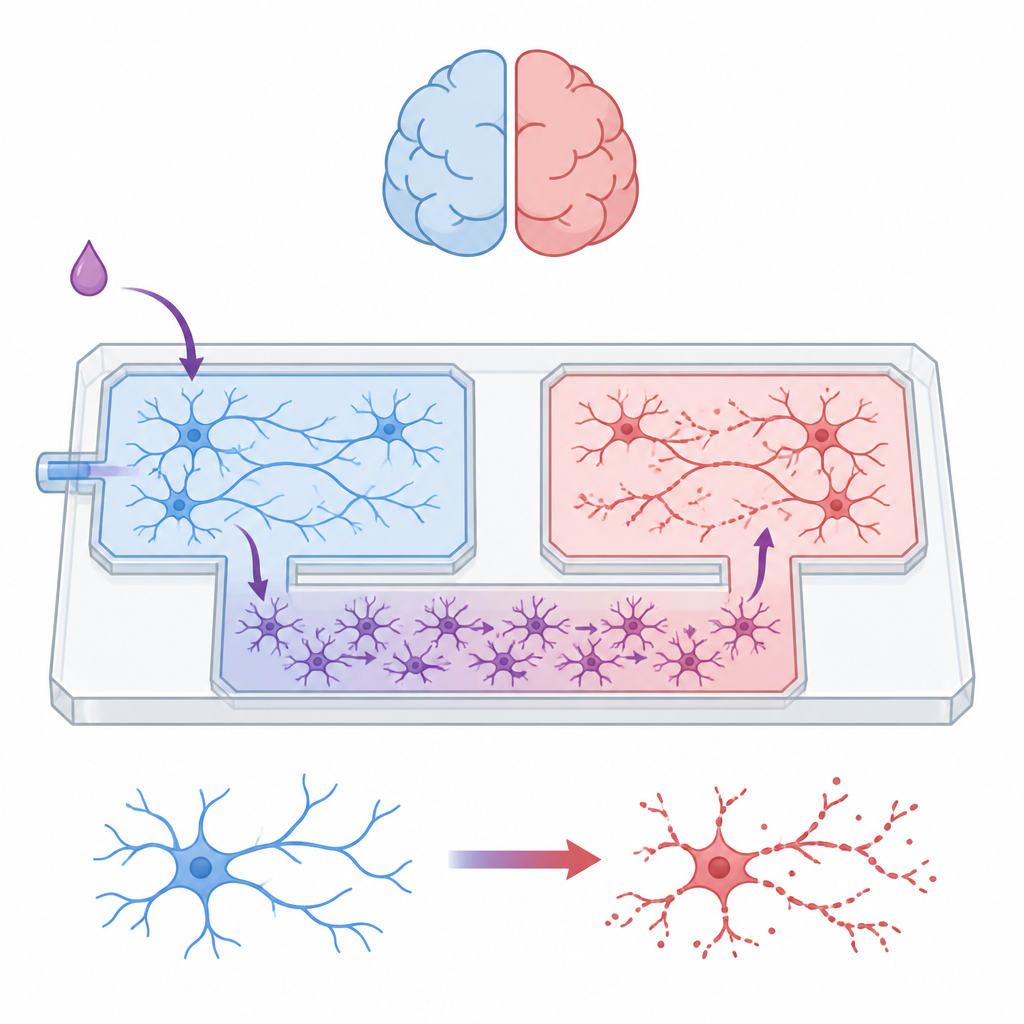
De helpers laten rondlopen terwijl neuronen worden ingesloten
Astrocyten groeiden goed door het hele apparaat en vormden een doorlopend tapijt dat zich over het doolhof en in alle kamers uitstrekte. Neuronen daarentegen bleven geconcentreerd in hun eigen compartimenten. Tests lieten zien dat wanneer hun uitlopers probeerden het doolhof over te steken, hun aantallen scherp daalden bij elke barrière en dat geen enkele uitloper de astrocyt-only baan bereikte. Eiwitprofilering van de verschillende regio’s bevestigde deze fysieke scheiding: de gemengde neuron–astrocyt kamers waren verrijkt met eiwitten geassocieerd met neurale groei, synapsen en elektrische signalering, terwijl het astrocyt-only gebied signaturen toonde van metabolisme en immuunachtige functies typisch voor gliacellen. Samen tonen deze resultaten aan dat het apparaat complexe, gemengde netwerken kan herbergen terwijl celtypen en signalen keurig gescheiden blijven.
Toeschouwen hoe toxische signalen de kloof oversteken
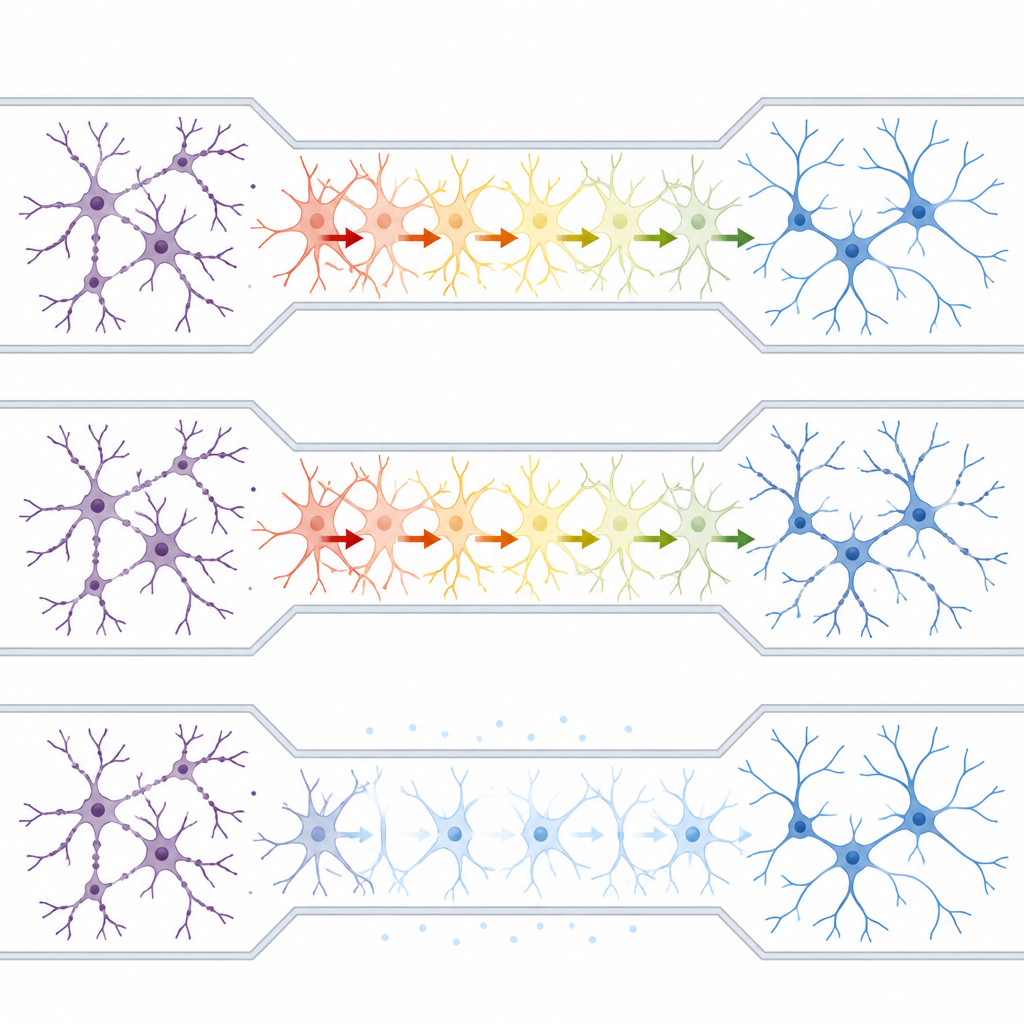
Met dit platform vroegen de onderzoekers zich af of astrocyten ‘‘excitotoxische’’ stress tussen geïsoleerde neurongroepen konden overbrengen. Ze brachten kaininezuur, een toevallig aanvalveroorzakende verbinding, aan op slechts één neuron–astrocyt kamer terwijl de vloeistofisolatie werd gehandhaafd. Binnen 15 minuten ontwikkelden de zenuwtakken aan de behandelde zijde kraalachtige zwellingen, een kenmerk van schade. Verrassend genoeg verschenen vergelijkbare kralenvormige zwellingen spoedig in de onaangeraakte neurongroep aan de andere kant van het doolhof, ondanks het ontbreken van directe neuron–neuron verbindingen of gedeelde vloeistof tussen de kamers. Toen hetzelfde toxine werd toegepast op neuronen gekweekt zonder astrocyten, bleef de schade lokaal, wat aangeeft dat astrocyten essentieel waren voor het verspreiden van de pathologie.
Calciumgolven in astrocyten als de verborgen boodschapper
Astrocyten communiceren met behulp van calciumgolven binnen hun cellen. Het team gebruikte een fluorescerende calciumindicator om deze veranderingen te volgen en vond dat blootstelling aan het toxine aan één kant van het apparaat verhoogde calciumsignalen in astrocyten in de centrale baan triggerde. Het blokkeren van astrocytcalcium met een membraanpermeabele chelator dempte deze golven, verminderde schade in de direct blootgestelde neuronen en voorkwam, belangrijker nog, de verspreiding van letsel naar de verre neurongroep. Interessant genoeg schaadde het volledig stilleggen van astrocytcalcium op zich neuronen, wat suggereert dat normale calciumactiviteit in deze cellen de gezonde netwerkfunctie ondersteunt, terwijl excessief calcium helpt ziektelike processen aan te jagen.
Waarom dit ertoe doet voor hersenziekten en behandeltests
Dit werk introduceert een veelzijdig brain-on-a-chip systeem dat verschillende hersencelpopulaties kan scheiden, verbinden en onafhankelijk behandelen terwijl het toch realistische interactie tussen neuronen en astrocyten toestaat. Het toont aan dat astrocyten excitotoxische stress tussen neurongroepen kunnen overbrengen via een calciumafhankelijk mechanisme, zelfs wanneer neuronen zelf van elkaar zijn afgesneden. Voor niet-specialisten is de kernboodschap dat ondersteunende hersencellen geen passieve toeschouwers zijn: ze kunnen schade versterken en verspreiden, maar vormen ook een doelwit voor beschermende behandelingen. Dit platform biedt een gecontroleerde manier om die rollen te onderzoeken en toekomstige therapieën te testen die schadelijke astrocytsignalen willen kalmeren bij aandoeningen zoals epilepsie, beroerte en neurodegeneratieve ziekten.
Bronvermelding: Yap, Y.C., Musgrove, R.E., Breadmore, M.C. et al. Microfluidic co-culture system for synaptically segregated neural networks to explore astrocyte-driven neural pathology. Microsyst Nanoeng 12, 181 (2026). https://doi.org/10.1038/s41378-026-01187-3
Trefwoorden: astrocyten, microfluidische brain chip, excitotoxiciteit, interacties tussen neuron en glia, calciumsignalering