Clear Sky Science · es
Sistema de co-cultivo microfluídico para redes neuronales sinápticamente segregadas para explorar la patología neural mediada por astrocitos
Cómo las células de soporte cerebral pueden propagar problemas en silencio
Cuando las células cerebrales enferman, el daño rara vez se queda en un solo lugar. Este estudio revela cómo los astrocitos, las células de apoyo en forma de estrella del cerebro, pueden transportar en silencio señales perjudiciales de un grupo de neuronas a otro. Usando un diminuto laboratorio en un chip, los investigadores recrearon un circuito cerebral simplificado para observar cómo el estrés en una esquina puede extenderse a regiones cercanas que nunca experimentaron la lesión original.
Un pequeño laberinto que imita barrios cerebrales
El equipo construyó un dispositivo microfluídico del tamaño de la palma que funciona como una ciudad en miniatura para células cerebrales. Dos cámaras separadas albergan poblaciones neuronales distintas, mientras que una vía central está reservada para los astrocitos. Entre estas áreas hay un entramado de canales estrechos que permite a los astrocitos deslizarse pero bloquea las largas fibras nerviosas de las neuronas. Al controlar cuidadosamente los niveles de líquido en los depósitos conectados, los investigadores pudieron mantener el entorno químico de cada compartimento aislado durante periodos determinados, garantizando que cualquier comunicación entre grupos neuronales tuviera que viajar a través de la capa de astrocitos en lugar de por contacto sináptico directo o líquido compartido.
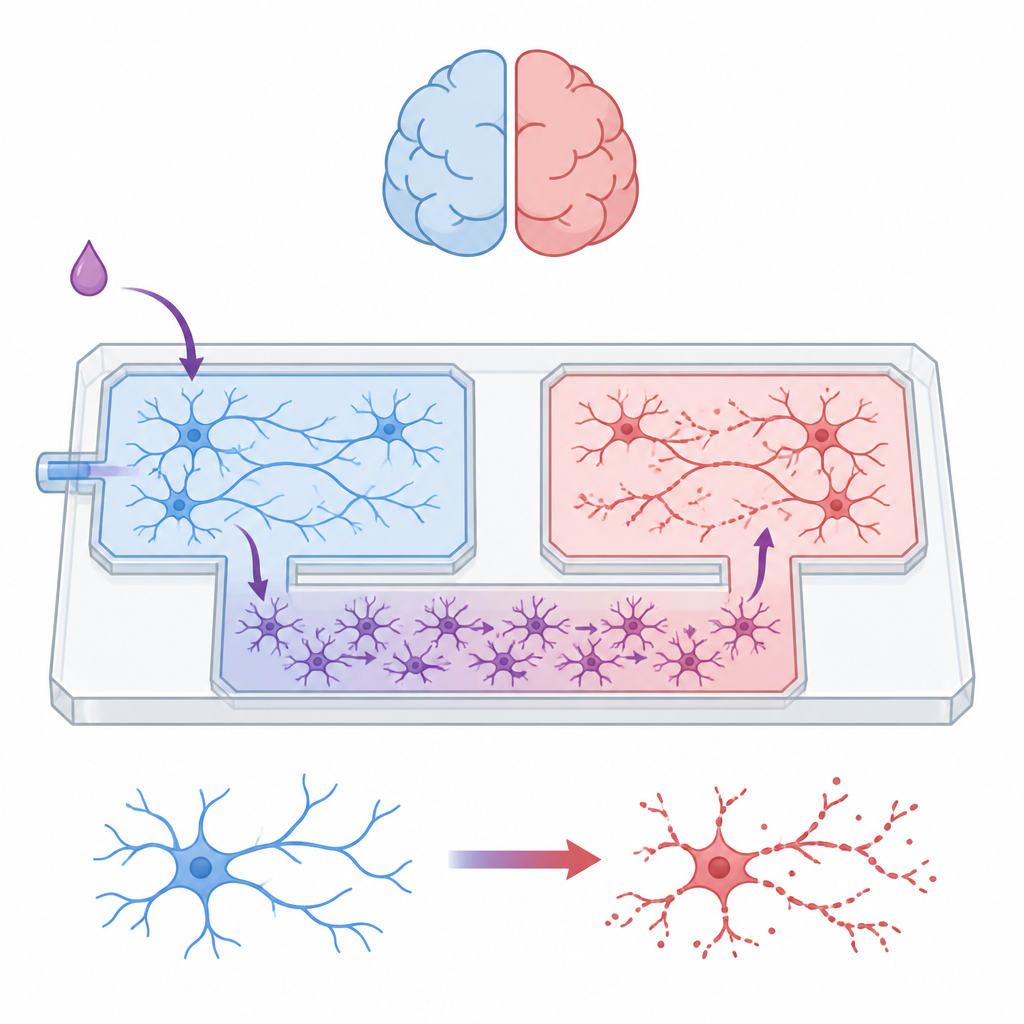
Dejar que los ayudantes vaguen mientras se encierran las neuronas
Los astrocitos crecieron con normalidad por todo el dispositivo, formando una alfombra continua que se extendió por el laberinto y hacia todas las cámaras. Las neuronas, en cambio, permanecieron confinadas. Las pruebas mostraron que cuando sus ramas intentaban cruzar el laberinto, su número caía drásticamente en cada barrera, y ninguna alcanzó la vía exclusiva de astrocitos. El perfil proteico de las distintas regiones confirmó esta separación física: las cámaras mixtas de neuronas y astrocitos estaban enriquecidas en proteínas asociadas al crecimiento neuronal, las sinapsis y la señalización eléctrica, mientras que el área de solo astrocitos mostraba firmas relacionadas con el metabolismo y funciones de tipo inmunitario propias de las células gliales. En conjunto, estos resultados demostraron que el dispositivo podía albergar redes complejas y heterogéneas manteniendo los tipos celulares y las señales claramente separados.
Observando cómo las señales tóxicas saltan la brecha
Con esta plataforma lista, los investigadores se preguntaron si los astrocitos podrían transportar estrés «excitotóxico» entre grupos neuronales aislados. Aplicaron ácido kainico, un compuesto que induce convulsiones, a únicamente una de las cámaras mixtas de neuronas y astrocitos manteniendo la separación fluidica. En 15 minutos, las ramas neuronales del lado tratado desarrollaron hinchazones en forma de cuentas, un sello característico de daño. Sorprendentemente, un beading similar apareció pronto en el grupo neuronal intacto al otro lado del laberinto, aunque no existían conexiones neurona a neurona directas ni líquido compartido entre las cámaras. Cuando la misma toxina se aplicó a neuronas cultivadas sin astrocitos, el daño se mantuvo local, lo que indica que los astrocitos eran esenciales para la propagación de la patología.
Ondas de calcio en astrocitos como mensajero oculto
Los astrocitos se comunican mediante ondas de calcio dentro de sus células. El equipo usó un indicador fluorescente de calcio para seguir estos cambios y encontró que la exposición a la toxina en un lado del dispositivo desencadenó señales elevadas de calcio en los astrocitos de la vía central. Bloquear el calcio de los astrocitos con un quelante permeable a membrana atenuó estas ondas, redujo el daño en las neuronas expuestas directamente y, lo que es importante, evitó la difusión de la lesión al grupo neuronal distante. Curiosamente, silenciar por completo el calcio astrocitario por sí solo perjudicó a las neuronas, lo que sugiere que la actividad normal del calcio en estas células sostiene la función saludable de la red, mientras que su exceso contribuye a procesos semejantes a la enfermedad.
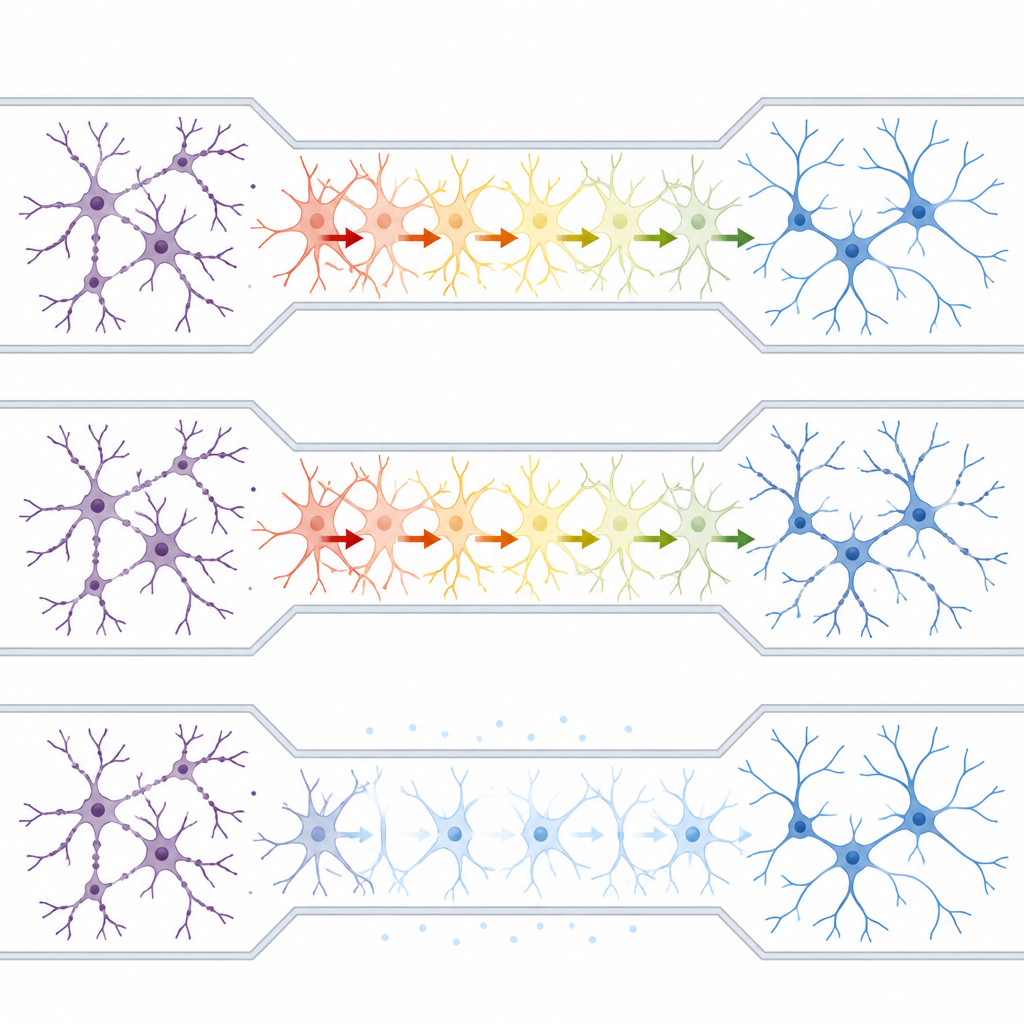
Por qué esto importa para las enfermedades cerebrales y las pruebas de tratamientos
Este trabajo presenta un sistema versátil de «cerebro-en-un-chip» que puede separar, conectar y tratar de forma independiente diferentes poblaciones celulares cerebrales al tiempo que permite un contacto realista entre neuronas y astrocitos. Muestra que los astrocitos pueden retransmitir estrés excitotóxico entre grupos de neuronas mediante un mecanismo dependiente de calcio, incluso cuando las neuronas están desconectadas entre sí. Para los no especialistas, el mensaje clave es que las células de soporte del cerebro no son meras espectadoras: pueden amplificar y propagar el daño, pero también constituyen un objetivo para tratamientos protectores. Esta plataforma proporciona una forma controlada de investigar esos papeles y probar futuras terapias destinadas a calmar las señales astrocitarias nocivas en afecciones como la epilepsia, el ictus y las enfermedades neurodegenerativas.
Cita: Yap, Y.C., Musgrove, R.E., Breadmore, M.C. et al. Microfluidic co-culture system for synaptically segregated neural networks to explore astrocyte-driven neural pathology. Microsyst Nanoeng 12, 181 (2026). https://doi.org/10.1038/s41378-026-01187-3
Palabras clave: astrocitos, chip cerebral microfluídico, excitotoxicidad, interacciones neurona-glía, señalización por calcio