Clear Sky Science · zh
基于DNA框架的纳米药物平台:通过抗菌、抗炎和促进成骨三重功能治疗牙周炎的策略
你的牙龈为何关系到全身健康
出血的牙龈和松动的牙齿常被视为小毛病,但晚期牙龈疾病——牙周炎——与心脏病、糖尿病甚至脑部疾病有密切关联。本研究探索了一种由DNA构建的新型“智能药物”,它能渗入受损的牙龈组织,清除有害细菌、平息失控的炎症,并帮助颌骨自我重建。通过同时解决三大问题——病菌、肿胀和骨质流失——这项工作指向了更短、更有效的治疗方案,针对目前影响数亿人的疾病具有重要意义。
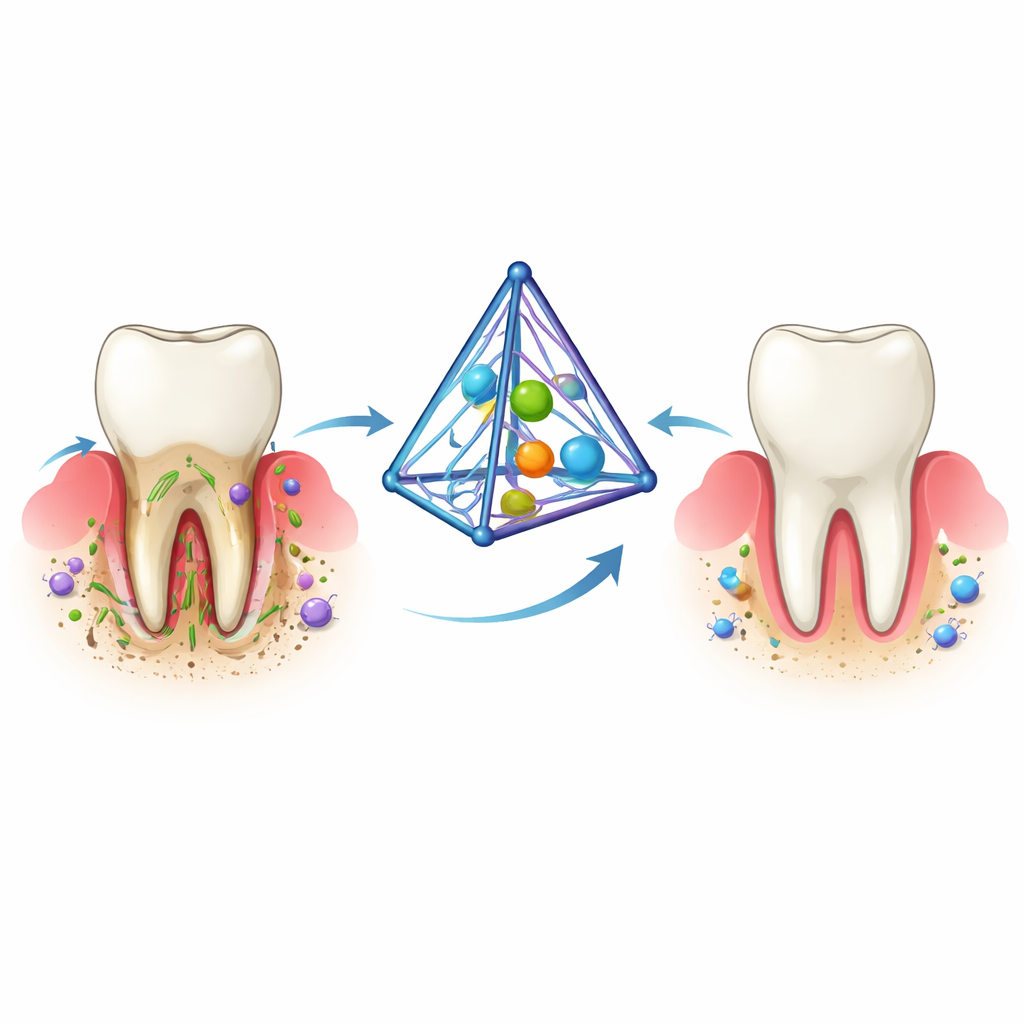
顽固牙龈病的问题所在
牙周炎始于黏性细菌斑块在牙龈缘下的堆积。机体以炎症反应来抵御感染,但随着时间推移,这种防御反而产生副作用。化学信号和活性氧分子累积,固定牙齿的胶原纤维被破坏,牙齿周围的骨骼逐渐溶解。现有的治疗——深度洁治和反复的局部用药——可以减少细菌和炎症,但很少能一次性解决全部三方面的问题:感染、持续性炎症和骨丧失。因此,许多患者需要长期护理,仍可能失去牙齿。
构建微小的DNA递送载体
研究人员采用了一种特殊的金字塔状DNA结构,称为四面体框架核酸。这种微小框架仅有数十纳米尺度,可以由DNA链精确组装并装载功能性货物。在本研究中,团队将一种名为防御素的抗菌肽连接到DNA的角部,并将姜黄素——一种具有抗炎和促进骨骼作用的姜黄提取物——嵌入DNA的槽位中。所得复合体被命名为Cur-de-tFNA,体积小、在类体液中稳定、易被细胞乃至细菌摄取,并能降解为天然DNA成分而不留下有害残留物。
抗菌与抑制炎症双重作用
在针对若干关键牙周致病菌的体外实验中,这一新型复合体比单独使用防御素或姜黄素显示出更强的效力。在显微镜下,暴露于Cur-de-tFNA的细菌显示出细胞壁破裂和内部受损,且其生长几乎完全被抑制。在暴露于细菌毒素的人类牙周膜干细胞中,该复合体显著降低了活性氧水平并减少了促炎信号的产生。同时,它下调了细胞内通常会放大炎症反应的关键报警通路,并上调已知有助于维持骨组织并引导干细胞修复的保护性信号。
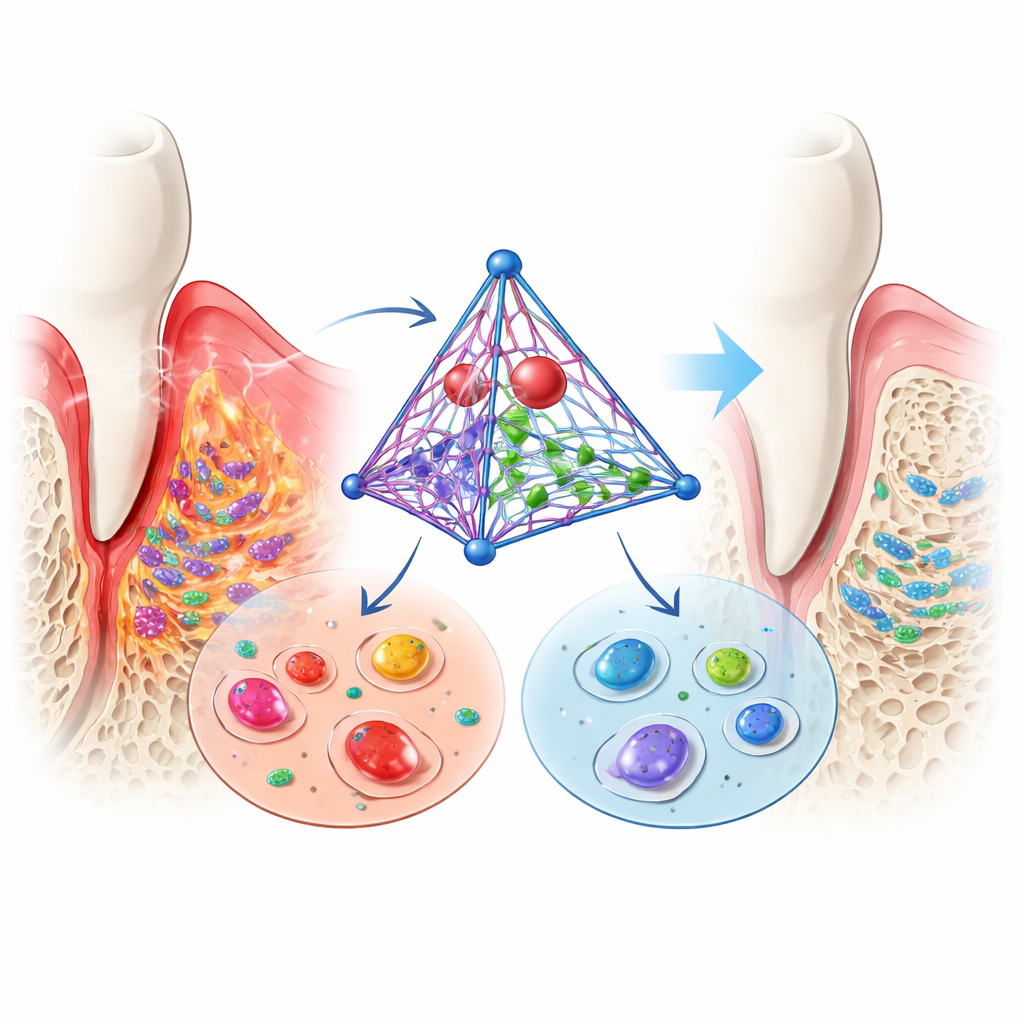
帮助干细胞重建流失的骨质
在适当条件下,锚定牙齿的韧带细胞可以成熟为成骨细胞。在模仿牙周炎的炎性环境中,这种能力通常受到抑制:成骨相关基因表达降低,矿化沉积稀少。当研究者加入其DNA复合体后,情况发生逆转。早期和晚期成骨标志物恢复乃至超过健康对照细胞的水平,培养物产生了更多矿化结节。这些发现表明,该平台不仅保护细胞免受损伤,还促使它们朝重建支持牙齿的骨和结缔组织方向发展。
在疾病牙龈中的概念验证
为评估该策略在生物体内的效果,团队在结扎诱导的牙周炎大鼠模型中测试了该复合体,这是评估严重牙龈疾病的标准模型。接受局部注射Cur-de-tFNA的动物,其支持骨丧失明显减少——约为未治疗动物骨吸收的一半——且在三维成像下显示出更致密、更厚的骨质。组织切片显示破骨细胞减少、胶原纤维更有序、炎性细胞浸润减少。全身炎症相关的血液标志物也下降,且治疗组大鼠的体重恢复更接近健康对照,暗示咀嚼舒适度和整体健康有所改善。
这对未来牙科护理意味着什么
总体而言,该研究引入了一种基于DNA的纳米药物平台,能够在单一系统中杀灭致病细菌、抑制有害炎症并促进牙周周围的新骨形成。尽管仍需进一步研究以确认长期安全性并将该方法适配于人类使用,这一三重功能策略展示了未来更具针对性、更持久且更少依赖广谱抗生素的牙龈治疗前景——这不仅可能保护我们的笑容,也有助于维护全身健康。
引用: Zhang, G., Cui, W., Wu, H. et al. DNA framework-based nanomedicine platform: a triple-function strategy for treating periodontitis via antibacterial, anti-inflammatory, and osteogenesis-promoting activities. Int J Oral Sci 18, 39 (2026). https://doi.org/10.1038/s41368-026-00439-2
关键词: 牙周炎, 纳米药物, DNA纳米结构, 姜黄素, 骨再生