Clear Sky Science · de
Nanomedizinplattform auf DNA-Rahmenbasis: Eine Dreifachfunktion-Strategie zur Behandlung von Parodontitis durch antibakterielle, entzündungshemmende und osteogenese-fördernde Aktivitäten
Warum Ihr Zahnfleisch für Ihren ganzen Körper wichtig ist
Blutendes Zahnfleisch und lockere Zähne werden oft als kleine Ärgernisse abgetan, doch fortgeschrittene Zahnfleischerkrankungen, also Parodontitis, stehen in engem Zusammenhang mit Herzkrankheiten, Diabetes und sogar Erkrankungen des Gehirns. Diese Studie untersucht eine neue Art von „intelligenter Medizin“ aus DNA, die in geschädigtes Zahnfleisch eindringen kann, schädliche Bakterien beseitigt, übermäßige Entzündungen dämpft und dem Kieferknochen beim Wiederaufbau hilft. Indem alle drei Probleme gleichzeitig angegangen werden — Erreger, Schwellung und Knochenverlust — deutet die Arbeit auf kürzere, wirksamere Behandlungen für eine Erkrankung hin, die derzeit Hunderte Millionen Menschen weltweit betrifft.
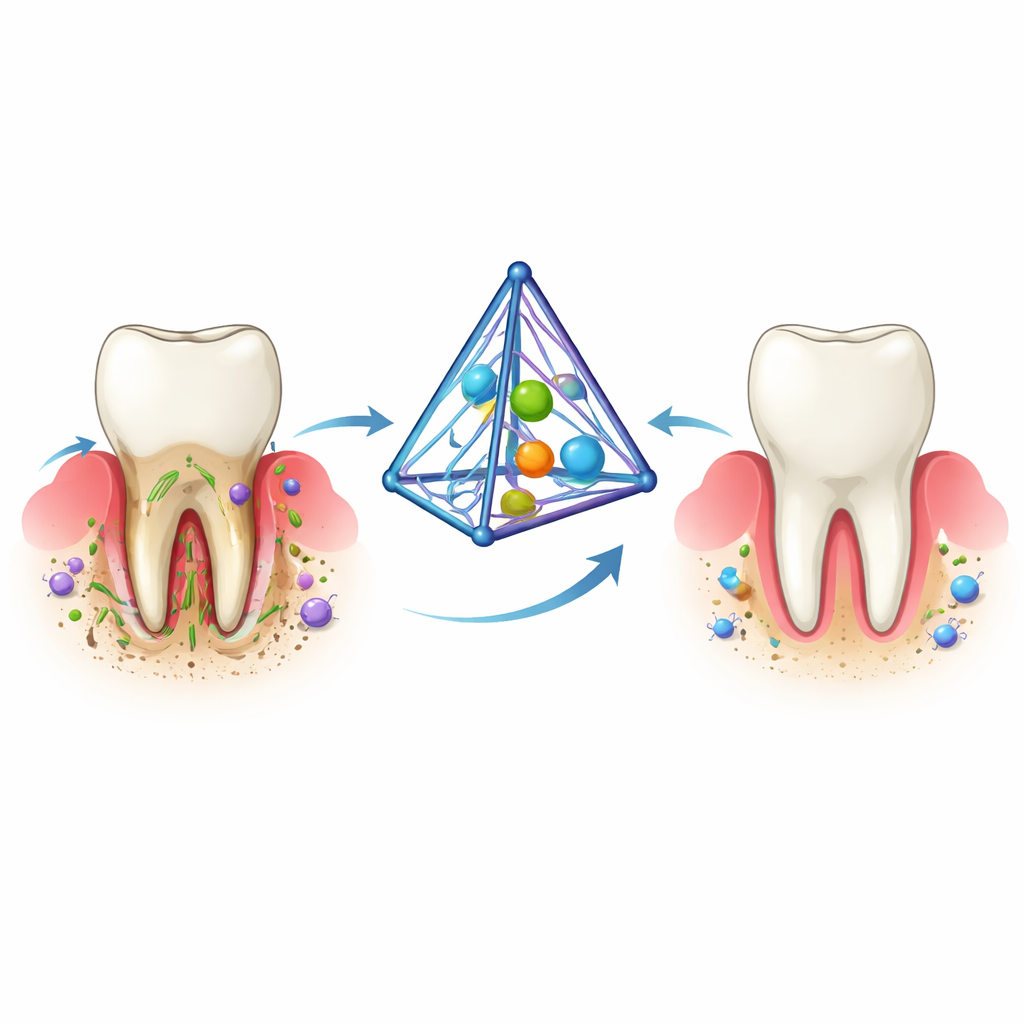
Das Problem hartnäckiger Zahnfleischerkrankungen
Parodontitis beginnt, wenn sich klebriger bakterieller Belag unter dem Zahnfleischrand ansammelt. Der Körper reagiert mit einer Entzündung, die der Abwehr von Infektionen dienen soll, doch mit der Zeit schlägt diese Verteidigung fehl. Chemische Signalstoffe und reaktive Sauerstoffmoleküle häufen sich, die Kollagenfasern, die den Zahn halten, bauen sich ab, und der Knochen um die Zähne löst sich langsam auf. Die heutigen Behandlungen — gründliche Reinigung unter dem Zahnfleisch und wiederholte lokale Medikamentenanwendungen — können Bakterien und Entzündung reduzieren, beheben aber selten alle drei Probleme auf einmal: Infektion, andauernde Entzündung und Knochenverlust. Daher benötigen viele Patienten langfristige Betreuung und verlieren dennoch möglicherweise Zähne.
Ein winziges DNA-Lieferfahrzeug bauen
Die Forschenden nutzten eine spezielle, pyramidenförmige DNA-Struktur, das tetraedrische Rahmen-Nukleinsäuregerüst. Dieses winzige Gerüst, nur wenige Milliardstel Meter groß, lässt sich präzise aus DNA-Strängen zusammensetzen und mit nützlicher Fracht versehen. In dieser Arbeit befestigte das Team ein antimikrobielles Peptid namens Defensin an den Ecken der DNA und platzierte Curcumin — eine entzündungshemmende und knochenunterstützende Verbindung aus Kurkuma — in den Rillen der DNA. Der resultierende Komplex, Cur-de-tFNA genannt, ist klein, stabil in körperähnlichen Flüssigkeiten, leicht von Zellen und sogar Bakterien aufzunehmen und baut sich in natürliche DNA-Bausteine ab, ohne schädliche Rückstände zu hinterlassen.
Gegen Erreger kämpfen und das Feuer beruhigen
In Labortests gegen mehrere wichtige Parodontitis-Erreger erwies sich der neue Komplex als deutlich wirksamer als Defensin oder Curcumin allein. Unter dem Mikroskop zeigten Bakterien, die Cur-de-tFNA ausgesetzt waren, aufgerissene Wände und beschädigte Innenstrukturen, und ihr Wachstum wurde fast vollständig gestoppt. In menschlichen Stammzellen des parodontalen Ligaments, die bakteriellen Toxinen ausgesetzt wurden, reduzierte der Komplex die Menge reaktiver Sauerstoffspezies stark und senkte die Produktion aggressiver Entzündungsmediatoren. Er dämpfte zugleich einen zentralen Alarmsignalweg in den Zellen, der normalerweise Entzündungen verstärkt. Gleichzeitig verstärkte er schützende Signale, die bekanntermaßen den Knochen erhalten und Stammzellen zur Reparatur leiten.
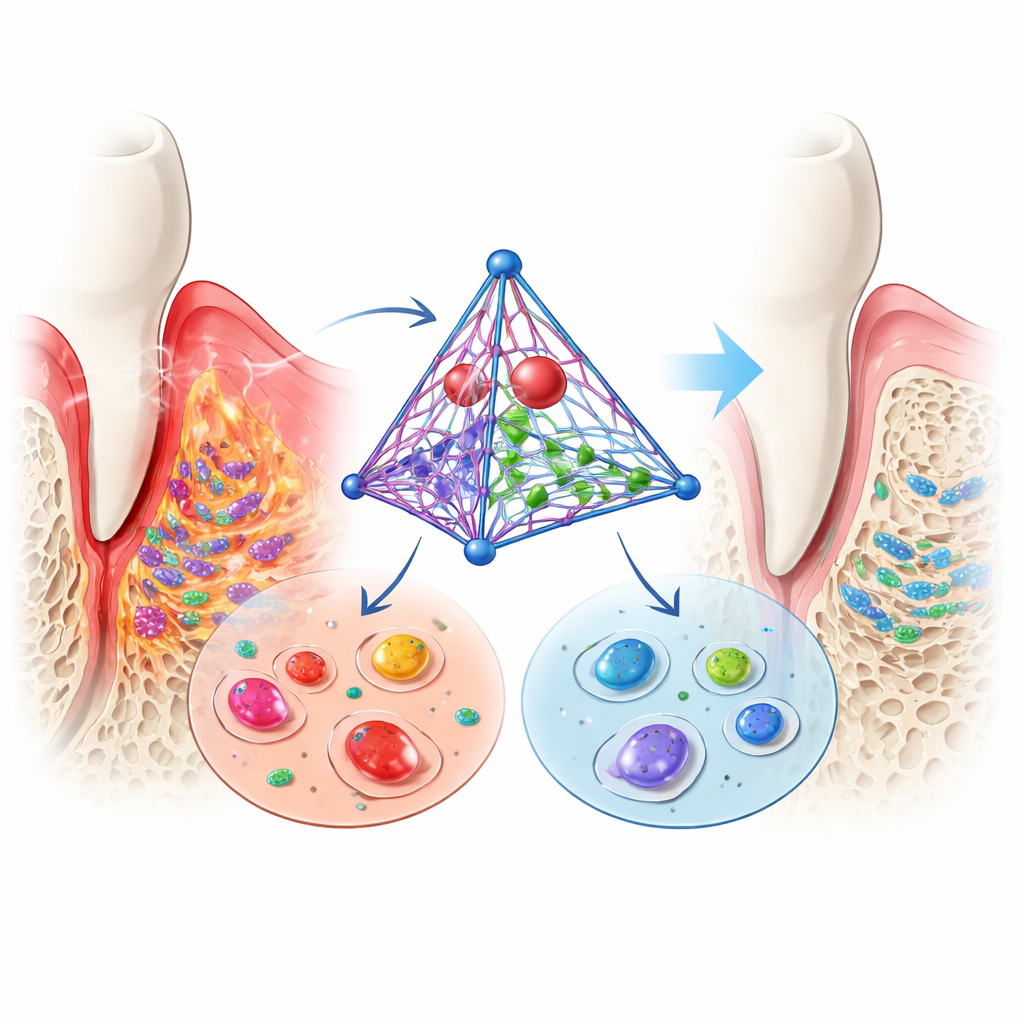
Stammzellen beim Wiederaufbau verlorenen Knochens unterstützen
Die Ligamentzellen, die die Zähne verankern, können unter den richtigen Bedingungen zu knochenbildenden Zellen heranreifen. In einer entzündeten Umgebung, die Parodontitis nachahmt, ist diese Fähigkeit normalerweise unterdrückt: knochenbildende Gene werden stiller, und Mineraleinlagerungen sind selten. Als die Forschenden ihren DNA-Komplex hinzugaben, kehrte sich die Lage um. Marker früher und später Knochenbildung erholten sich oder übertrafen sogar die Werte gesunder Kontrollzellen, und die Kulturen bildeten mehr mineralisierte Knötchen. Diese Befunde deuten darauf hin, dass die Plattform nicht nur Zellen vor Schäden schützt, sondern sie auch in Richtung Wiederaufbau von Knochen und Bindegewebe, die die Zähne stützen, lenkt.
Machbarkeitsnachweis in erkranktem Zahnfleisch
Um zu prüfen, ob die Strategie in lebenden Organismen wirkt, testete das Team den Komplex an Ratten mit ligaturinduzierter Parodontitis, einem Standardmodell schwerer Zahnfleischerkrankung. Tiere, die lokale Injektionen von Cur-de-tFNA rund um die betroffenen Zähne erhielten, verloren deutlich weniger Stütz-Knochen — etwa halb so viel Resorption wie unbehandelte Tiere — und zeigten unter 3D-Bildgebung dichteren, dickeren Knochen. Gewebeschnitte zeigten weniger knochensetzende Zellen, organisiertere Kollagenfasern und reduzierte Infiltration entzündlicher Zellen. Blutmarker systemischer Entzündung sanken ebenfalls, und die behandelten Ratten nahmen mehr wie gesunde Kontrollen zu, was auf besseren Kaukomfort und allgemein bessere Gesundheit hindeutet.
Was das für die künftige Zahnmedizin bedeuten könnte
Insgesamt stellt die Studie eine DNA-basierte Nanomedizin vor, die in einer einzigen Plattform krankheitsverursachende Bakterien abtöten, schädliche Entzündungen beruhigen und die Neubildung von Knochen um Zähne fördern kann. Obwohl weitere Arbeiten nötig sind, um Langzeitsicherheit zu bestätigen und den Ansatz für den Menschen anzupassen, bietet diese Dreifachfunktion-Strategie einen Ausblick auf zukünftige Zahnfleischbehandlungen, die gezielter, länger anhaltend und weniger abhängig von Breitbandantibiotika sind — und damit möglicherweise nicht nur unser Lächeln, sondern die Gesundheit des ganzen Körpers schützen.
Zitation: Zhang, G., Cui, W., Wu, H. et al. DNA framework-based nanomedicine platform: a triple-function strategy for treating periodontitis via antibacterial, anti-inflammatory, and osteogenesis-promoting activities. Int J Oral Sci 18, 39 (2026). https://doi.org/10.1038/s41368-026-00439-2
Schlüsselwörter: Parodontitis, Nanomedizin, DNA-Nanostruktur, Curcumin, Knochenregeneration