Clear Sky Science · fr
Plate-forme de nanomédecine à base d’ossature d’ADN : une stratégie à triple fonction pour traiter la parodontite via des activités antibactériennes, anti-inflammatoires et pro-ostéogenèse
Pourquoi vos gencives comptent pour tout votre corps
Les gencives qui saignent et les dents qui se déchaussent sont souvent perçues comme de petits désagréments, mais la maladie avancée des gencives, la parodontite, est étroitement liée aux maladies cardiaques, au diabète et même à des troubles cérébraux. Cette étude explore un nouveau type de « médicament intelligent » construit à partir d’ADN capable de pénétrer les tissus gingivaux endommagés, d’éliminer les bactéries nocives, d’apaiser l’inflammation incontrôlée et d’aider l’os de la mâchoire à se reconstruire. En traitant simultanément les trois problèmes — germes, gonflement et perte osseuse — ce travail ouvre la voie à des traitements plus courts et plus efficaces pour une maladie qui touche actuellement des centaines de millions de personnes dans le monde.
Le problème de la parodontite tenace
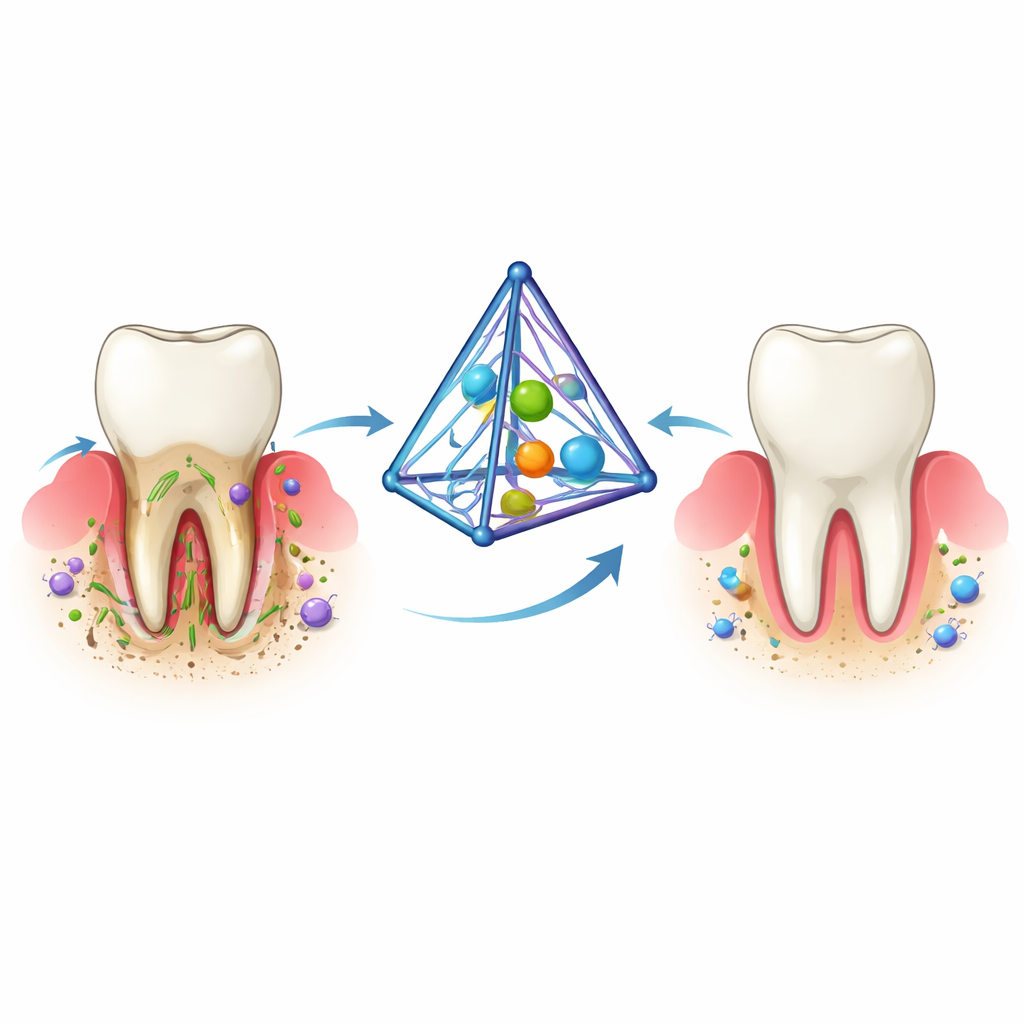
La parodontite commence lorsque la plaque bactérienne adhésive s’accumule sous la ligne gingivale. L’organisme réagit par une inflammation destinée à lutter contre l’infection, mais au fil du temps cette défense se retourne contre l’hôte. Des signaux chimiques et des molécules réactives de l’oxygène s’accumulent, les fibres de collagène qui maintiennent la dent se dégradent et l’os autour des dents se dissout progressivement. Les traitements actuels — détartrage et surfaçage radiculaire profonds et applications locales répétées de médicaments — peuvent réduire les bactéries et l’inflammation mais corrigent rarement les trois problèmes en une seule intervention : infection, inflammation persistante et perte osseuse. En conséquence, de nombreux patients nécessitent des soins à long terme et peuvent quand même perdre des dents.
Construire un minuscule vecteur d’ADN
Les chercheurs se sont tournés vers une structure d’ADN pyramidale spéciale appelée acide nucléique à ossature tétraédrique. Ce minuscule échafaudage, de l’ordre de quelques nanomètres, peut être construit avec précision à partir de brins d’ADN puis paré de charges utiles. Dans ce travail, l’équipe a fixé un peptide antimicrobien appelé défensine aux sommets de l’ADN puis a logé la curcumine — un composé anti-inflammatoire et favorable à l’os provenant du curcuma — dans les sillons de l’ADN. Le complexe résultant, nommé Cur-de-tFNA, est petit, stable dans des fluides de type corporel, facilement capté par les cellules et même les bactéries, et se dégrade en composants d’ADN naturels sans laisser de résidus nocifs.
Combattre les germes et calmer l’inflammation
Dans des essais en laboratoire contre plusieurs bactéries clés de la maladie parodontale, le nouveau complexe s’est avéré bien plus puissant que la défensine ou la curcumine prises séparément. Au microscope, les bactéries exposées au Cur-de-tFNA présentaient des parois rompues et des intérieurs endommagés, et leur croissance était presque complètement arrêtée. Dans des cellules souches du ligament parodontal humain exposées à des toxines bactériennes, le complexe a fortement réduit les niveaux d’espèces réactives de l’oxygène et diminué la production de signaux inflammatoires agressifs. Il a également atténué une voie d’alarme centrale à l’intérieur des cellules qui amplifie normalement l’inflammation. Parallèlement, il a renforcé des signaux protecteurs connus pour aider à maintenir l’os et orienter les cellules souches vers la réparation.
Aider les cellules souches à reconstruire l’os perdu
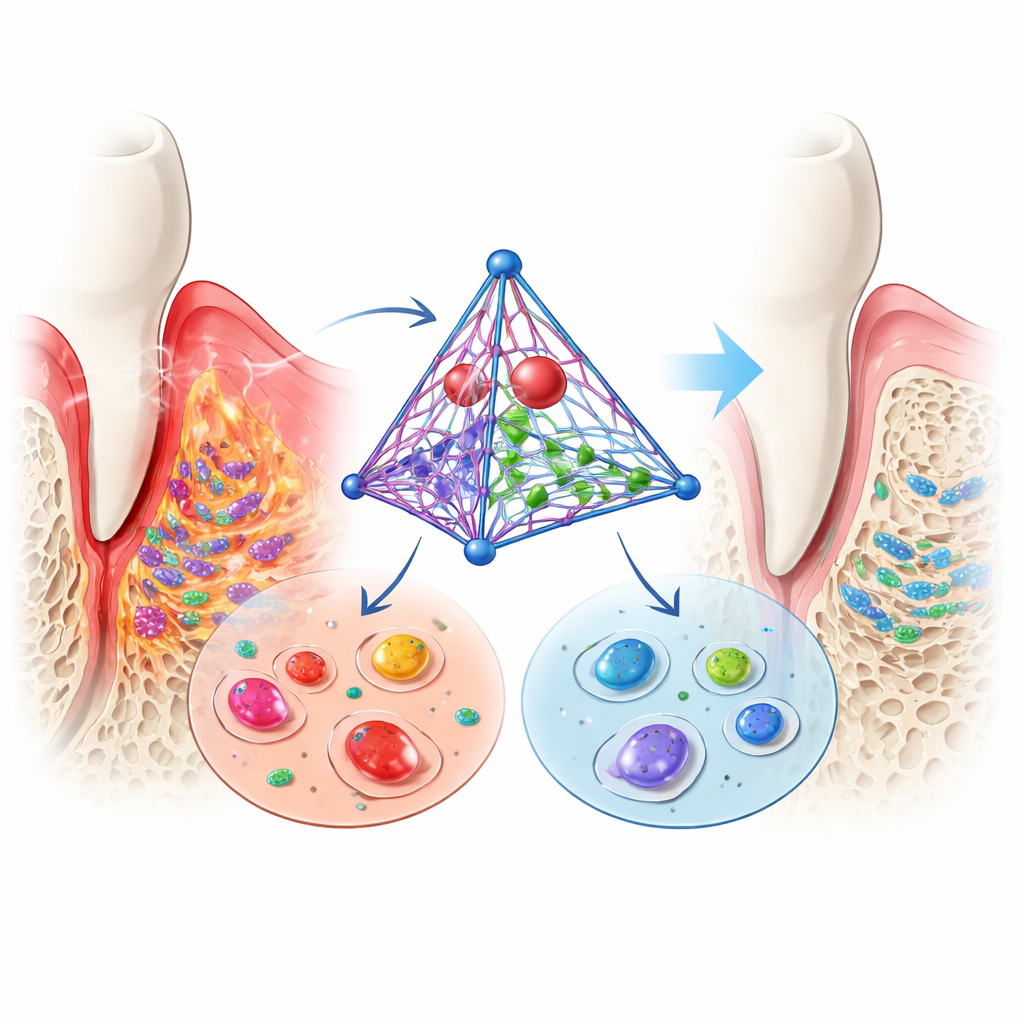
Les cellules ligamentaires qui ancrent les dents peuvent, dans de bonnes conditions, mûrir en cellules productrices d’os. Dans un environnement inflammé qui imite la parodontite, cette capacité est généralement supprimée : les gènes de formation osseuse se taisent et les dépôts minéraux sont rares. Lorsque les chercheurs ont ajouté leur complexe d’ADN, la situation s’est inversée. Les marqueurs de la formation osseuse précoce et tardive ont rebondi ou ont même dépassé les niveaux observés dans les cellules témoins saines, et les cultures ont produit davantage de nodules minéralisés. Ces observations suggèrent que la plate-forme ne se contente pas de protéger les cellules des dommages, elle les incite aussi à reconstruire l’os et le tissu conjonctif qui soutiennent les dents.
Preuve de concept dans des gencives malades
Pour vérifier si la stratégie fonctionne chez des organismes vivants, l’équipe a testé le complexe chez des rats présentant une parodontite induite par ligature, un modèle standard de maladie gingivale sévère. Les animaux ayant reçu des injections locales de Cur-de-tFNA autour des dents affectées ont perdu beaucoup moins d’os de soutien — environ la moitié de la résorption observée chez les animaux non traités — et ont montré un os plus dense et plus épais en imagerie 3D. Les coupes tissulaires ont révélé moins de cellules résorbant l’os, des fibres de collagène mieux organisées et une infiltration réduite de cellules inflammatoires. Les marqueurs sanguins d’inflammation systémique ont également diminué, et les rats traités ont pris du poids de façon plus similaire aux témoins sains, suggérant un meilleur confort masticatoire et un état de santé général amélioré.
Ce que cela pourrait signifier pour les soins dentaires futurs
Dans l’ensemble, l’étude présente une nanomédecine à base d’ADN qui peut, sur une seule plate-forme, éliminer les bactéries pathogènes, calmer l’inflammation nuisible et favoriser la formation d’un nouvel os autour des dents. Bien que des travaux supplémentaires soient nécessaires pour confirmer la sécurité à long terme et adapter l’approche à l’usage humain, cette stratégie à triple fonction offre un aperçu de traitements gingivaux futurs plus ciblés, plus durables et moins dépendants des antibiotiques à large spectre — protégeant potentiellement non seulement notre sourire mais aussi la santé de tout le corps.
Citation: Zhang, G., Cui, W., Wu, H. et al. DNA framework-based nanomedicine platform: a triple-function strategy for treating periodontitis via antibacterial, anti-inflammatory, and osteogenesis-promoting activities. Int J Oral Sci 18, 39 (2026). https://doi.org/10.1038/s41368-026-00439-2
Mots-clés: parodontite, nanomédecine, nanostructure d’ADN, curcumine, régénération osseuse