Clear Sky Science · nl
Nanomedicineplatform op DNA-raamwerkbasis: een drievoudige strategie voor de behandeling van parodontitis via antibacteriële, ontstekingsremmende en botregeneratiebevorderende activiteiten
Waarom je tandvlees ertoe doet voor je hele lichaam
Bloedend tandvlees en losse tanden worden vaak gezien als kleine ergernissen, maar gevorderde tandvleesontsteking, oftewel parodontitis, hangt sterk samen met hartaandoeningen, diabetes en zelfs hersenstoornissen. Deze studie onderzoekt een nieuw soort ‘slimme therapie’ opgebouwd uit DNA die beschadigd tandvlees kan binnendringen, schadelijke bacteriën kan verwijderen, buitensporige ontsteking kan kalmeren en het kaakbot kan helpen herstellen. Door alle drie de problemen tegelijk aan te pakken — microben, zwelling en botverlies — wijst het werk op kortere, effectievere behandelingen voor een aandoening die momenteel honderden miljoenen mensen wereldwijd treft.
Het probleem van hardnekkige tandvleesontsteking
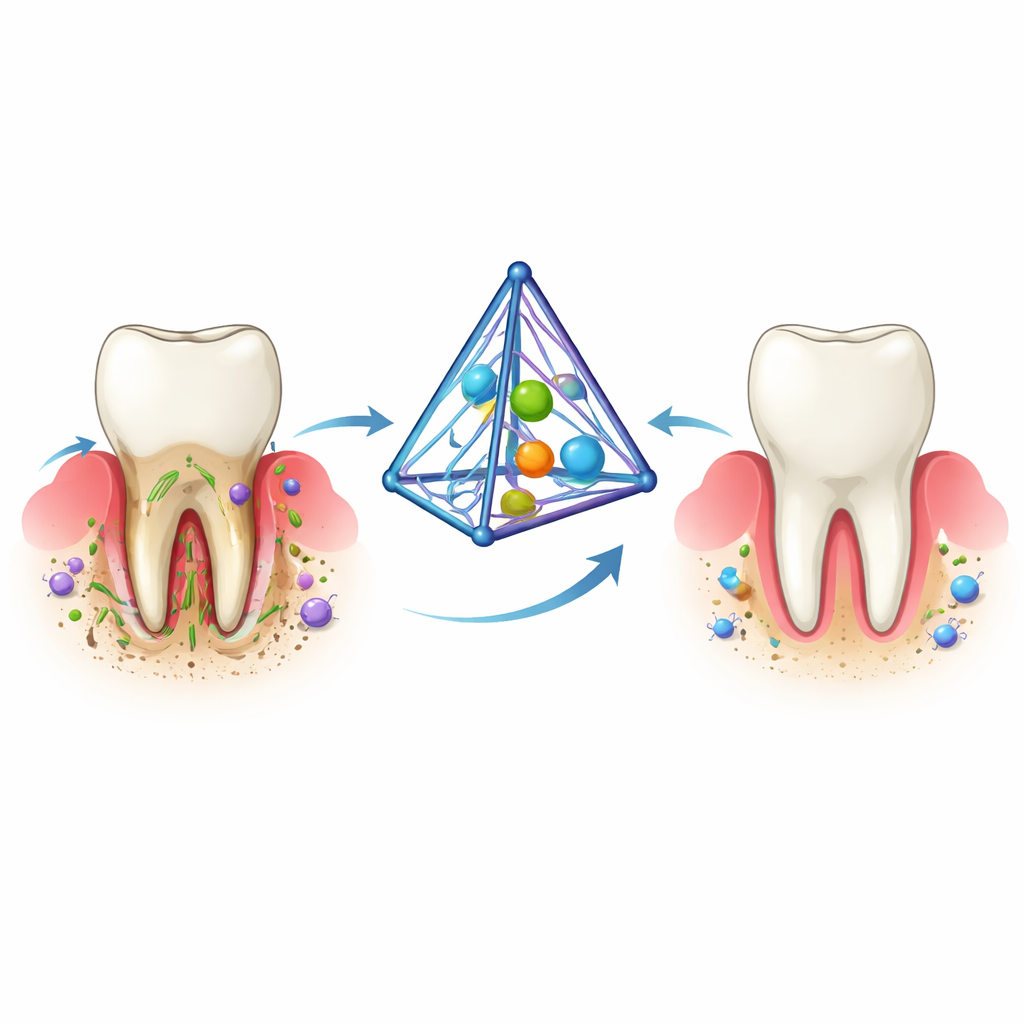
Parodontitis begint wanneer plakkerig bacterieel tandplak zich onder de tandvleesrand ophoopt. Het lichaam reageert met ontsteking die bedoeld is om tegen infectie te verdedigen, maar na verloop van tijd slaat die verdediging om. Chemische signalen en reactieve zuurstofmoleculen hopen zich op, collageenvezels die de tand op zijn plaats houden breken af en het bot rond de tanden lost langzaam op. De huidige behandelingen — grondige reiniging onder het tandvlees en herhaalde lokale toediening van geneesmiddelen — kunnen bacteriën en ontsteking verminderen maar lossen zelden alle drie de problemen in één keer op: infectie, aanhoudende ontsteking en verloren bot. Daardoor hebben veel patiënten langdurige zorg nodig en kunnen ze toch tanden verliezen.
Het bouwen van een klein DNA-bezorgvoertuig
De onderzoekers schakelden een speciale piramidevormige DNA-structuur in, een tetraëdrisch raamwerk van nucleïnezuren. Dit piepkleine raamwerk, slechts enkele miljardsten van een meter groot, kan nauwkeurig worden opgebouwd uit DNA-strengen en vervolgens worden versierd met nuttige lading. In dit werk bevestigde het team een antimicrobieel peptide genaamd defensine aan de DNA-hoeken en stopte curcumine — een ontstekingsremmende en botondersteunende verbinding uit kurkuma — in de groeven van het DNA. Het resulterende complex, genoemd Cur-de-tFNA, is klein, stabiel in lichaamsachtige vloeistoffen, gemakkelijk op te nemen door cellen en zelfs bacteriën, en breekt af tot natuurlijke DNA-componenten zonder schadelijke residuen achter te laten.
Microben bestrijden en het vuur blussen
In laboratoriumtests tegen meerdere belangrijke tandvleesziektebacteriën bleek het nieuwe complex veel krachtiger dan alleen defensine of curcumine. Onder de microscoop vertoonden bacteriën die aan Cur-de-tFNA werden blootgesteld gescheurde wanden en beschadigde binnenstructuren, en hun groei werd vrijwel volledig stilgelegd. In menselijke periodontale ligament-stamcellen die aan bacteriële toxines werden blootgesteld, verminderde het complex sterk de niveaus van reactieve zuurstofsoorten en verlaagde het de productie van agressieve ontstekingssignalen. Het dempte ook een centraal alarmsignaalpad in cellen dat normaal gesproken ontsteking versterkt. Tegelijkertijd versterkte het beschermende signalen die bekend zijn om bot te behouden en stamcellen naar herstel te sturen.
Stamcellen helpen verloren bot te herbouwen
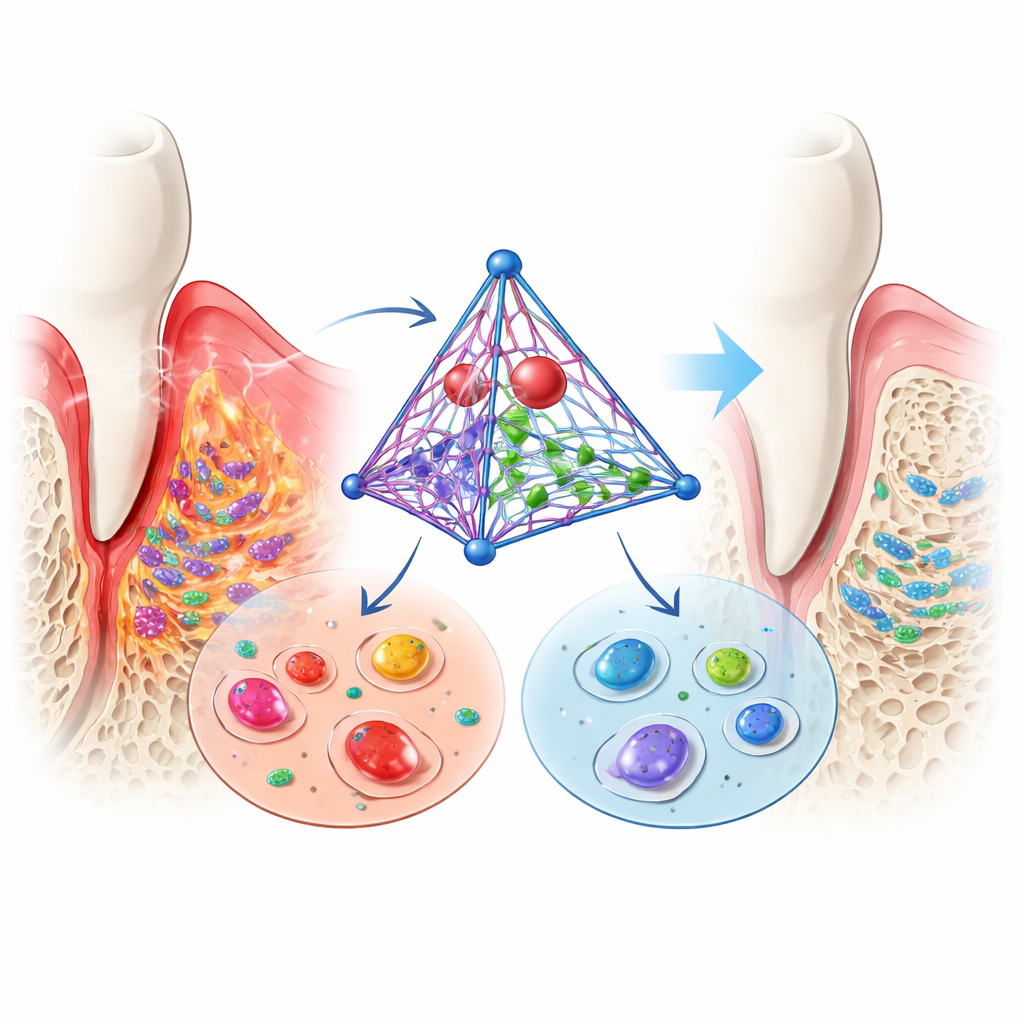
De ligamentcellen die tanden verankeren kunnen, onder de juiste omstandigheden, uitrijpen tot botvormende cellen. In een ontstoken omgeving die parodontitis nabootst, is dit vermogen meestal onderdrukt: botopbouwende genen zwakken af en minerale afzettingen zijn schaars. Toen de onderzoekers hun DNA-complex toevoegden, keerde de situatie om. Merkers van vroege en late botvorming herstelden of overschreden zelfs de niveaus gezien in gezonde controlecellen, en de culturen produceerden meer gemineraliseerde knobbeltjes. Deze bevindingen suggereren dat het platform niet alleen cellen tegen schade beschermt, maar ze ook aanspoort om het bot en bindweefsel dat tanden ondersteunt, te herbouwen.
Proof of concept in aangetast tandvlees
Om te zien of de strategie in levende organismen werkt, testte het team het complex in ratten met ligatuur-geïnduceerde parodontitis, een standaardmodel van ernstige tandvleesontsteking. Dieren die lokale injecties van Cur-de-tFNA rond de aangetaste tanden kregen, verloren veel minder ondersteunend bot — ongeveer de helft van de resorptie gezien bij onbehandelde dieren — en toonden dichtere, dikkere botstructuur op 3D-beelden. Weefseldoorsneden toonden minder botresorberende cellen, meer geordende collageenvezels en verminderde infiltratie van ontstekingscellen. Bloedmarkers van systemische ontsteking daalden ook, en de behandelde ratten kwamen aan in gewicht meer vergelijkbaar met gezonde controles, wat wijst op beter kauwcomfort en algemene gezondheid.
Wat dit kan betekenen voor toekomstige tandheelkundige zorg
Al met al introduceert de studie een op DNA gebaseerde nanomedicine die in één platform ziekteverwekkende bacteriën kan doden, schadelijke ontsteking kan dempen en de vorming van nieuw bot rond tanden kan stimuleren. Hoewel er meer werk nodig is om de veiligheid op lange termijn te bevestigen en de aanpak voor menselijk gebruik aan te passen, biedt deze drievoudige strategie een vooruitblik op toekomstige tandvleesbehandelingen die gerichter, duurzamer en minder afhankelijk van breedspectrumantibiotica zijn — mogelijk ter bescherming van niet alleen ons gebit maar onze algehele gezondheid.
Bronvermelding: Zhang, G., Cui, W., Wu, H. et al. DNA framework-based nanomedicine platform: a triple-function strategy for treating periodontitis via antibacterial, anti-inflammatory, and osteogenesis-promoting activities. Int J Oral Sci 18, 39 (2026). https://doi.org/10.1038/s41368-026-00439-2
Trefwoorden: parodontitis, nanomedicine, DNA-nanostructuur, curcumine, botregeneratie