Clear Sky Science · ar
منصة نانوادوية مبنية على هيكل DNA: استراتيجية ثلاثية الوظائف لعلاج التهاب اللثة من خلال نشاطات مضادة للبكتيريا، مضادة للالتهاب، ومحفزة لتكوّن العظم
لماذا لثتك تهم جسدك كله
نزيف اللثة وارتخاء الأسنان قد يُنظر إليهما غالبًا كمشاكل بسيطة، لكن مرض اللثة المتقدم، أو التهاب اللثة (periodontitis)، مرتبط ارتباطًا وثيقًا بأمراض القلب والسكري وحتى اضطرابات الدماغ. تستعرض هذه الدراسة نوعًا جديدًا من «الدواء الذكي» المبني من الـDNA الذي يمكنه التسلل إلى نسيج اللثة المتضرر، والقضاء على البكتيريا الضارة، وتهدئة الالتهاب المفرط، ومساعدة عظم الفك على إعادة بناء نفسه. من خلال التصدي للمشكلات الثلاثة معًا — الجراثيم، التورّم، وفقدان العظم — يشير العمل إلى علاجات أقصر وأكثر فعالية لمرض يصيب مئات الملايين من الناس حول العالم.
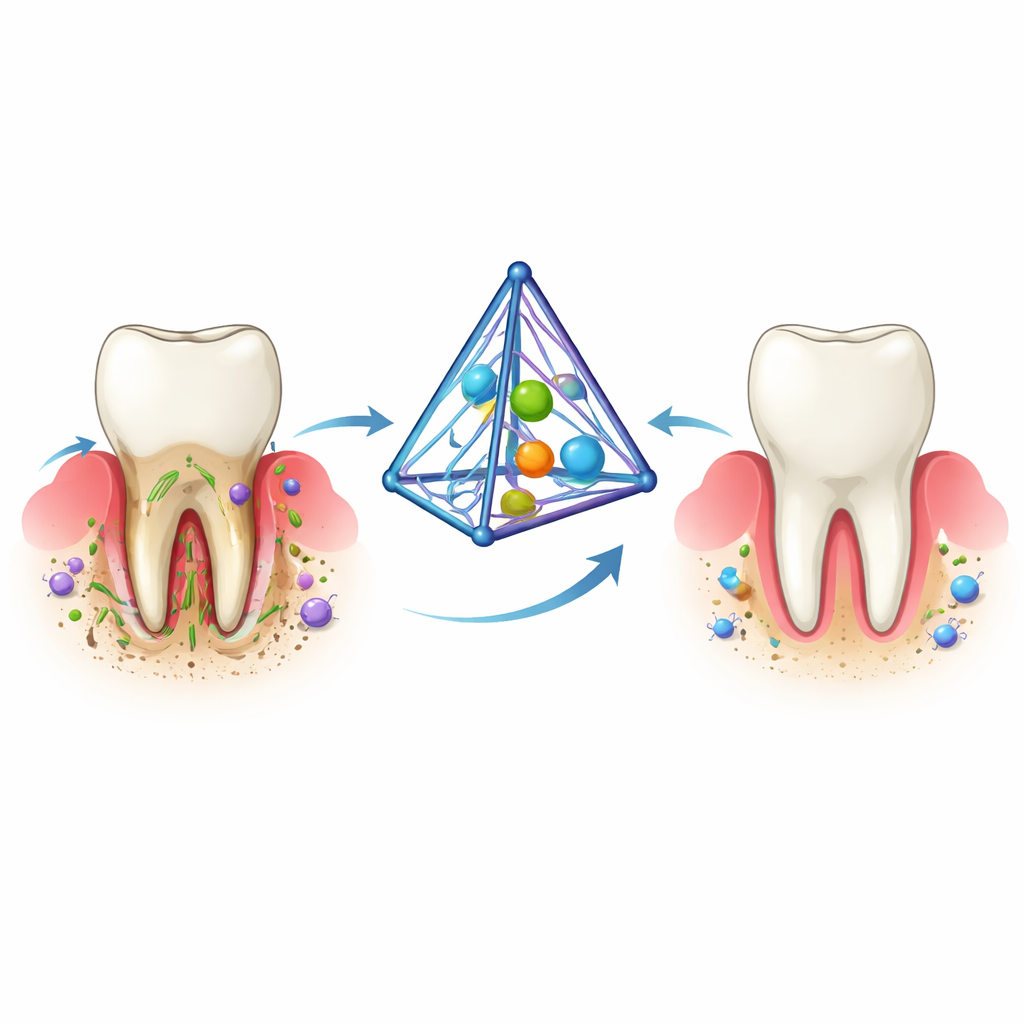
المشكلة مع مرض اللثة العنيد
يبدأ التهاب اللثة عندما تتراكم طبقة لزجة من البلاك البكتيري تحت خط اللثة. يستجيب الجسم بالالتهاب الذي يقصد به الدفاع عن العدوى، لكن مع مرور الوقت تنقلب هذه الدفاعات ضد النسيج. تتراكم الإشارات الكيميائية وجزيئات الأكسدة التفاعلية، وتتكسّر ألياف الكولاجين التي تُثبت السن في مكانه، ويذوب العظم المحيط بالأسنان تدريجيًا. العلاجات الحالية — تنظيف عميق تحت اللثة وتطبيقات دوائية محلية متكررة — يمكن أن تقلل البكتيريا والالتهاب لكنها نادرًا ما تعالج القضايا الثلاث في آن واحد: العدوى، الالتهاب المستمر، وفقدان العظم. ونتيجة لذلك، يحتاج العديد من المرضى إلى رعاية طويلة الأمد وقد يفقدون أسنانهم رغم العلاج.
بناء ناقل مواد صغير من الـDNA
اتجه الباحثون إلى بنية DNA هرمية خاصة تُسمى هيكل نُوكلييك حمضي رباعي السطوح. هذا الإطار الصغير، الذي لا يتجاوز بضعة مليارات من المتر عرضًا، يمكن بناؤه بدقة من خيوط الـDNA ثم تزيينه بحمولات مفيدة. في هذا العمل، ركّب الفريق ببتيدًا مضادًا للميكروبات يسمى ديفنسين على زوايا الـDNA ثم وضع الكركمين — مركب مضاد للالتهاب ويدعم العظم مستخرج من الكركم — في أخاديد الـDNA. المُركّب الناتج، المُسمى Cur-de-tFNA، صغير ومستقر في سوائل تحاكي سوائل الجسم، وسهل الامتصاص للخلايا وحتى للبكتيريا، ويتحلّل إلى مكونات DNA طبيعية دون ترك رواسب ضارة.
مكافحة الجراثيم وتهدئة الالتهاب
في اختبارات مختبرية ضد عدة بكتيريا رئيسية لمرض اللثة، أثبت المُركّب الجديد فعالية أكبر بكثير من الديفنسين أو الكركمين بمفردهما. تحت الميكروسكوب، أظهرت البكتيريا المعرضة لـCur-de-tFNA جدرانًا منقرضة وداخليات متضررة، وتوقّف نموها تقريبًا تمامًا. في خلايا جذع رباط الأسنان البشري المعرضة لسموم بكتيرية، خفّض المُركّب بشكل حاد مستويات أنواع الأكسجين التفاعلية وقلّل إنتاج إشارات التهابية عدوانية. كما خفّض مسار إنذار مركزي داخل الخلايا كان يضخم الالتهاب عادة. وفي الوقت نفسه، عزّز إشارات حماية معروفة بمساهمتها في الحفاظ على العظم وتوجيه الخلايا الجذعية نحو الإصلاح.
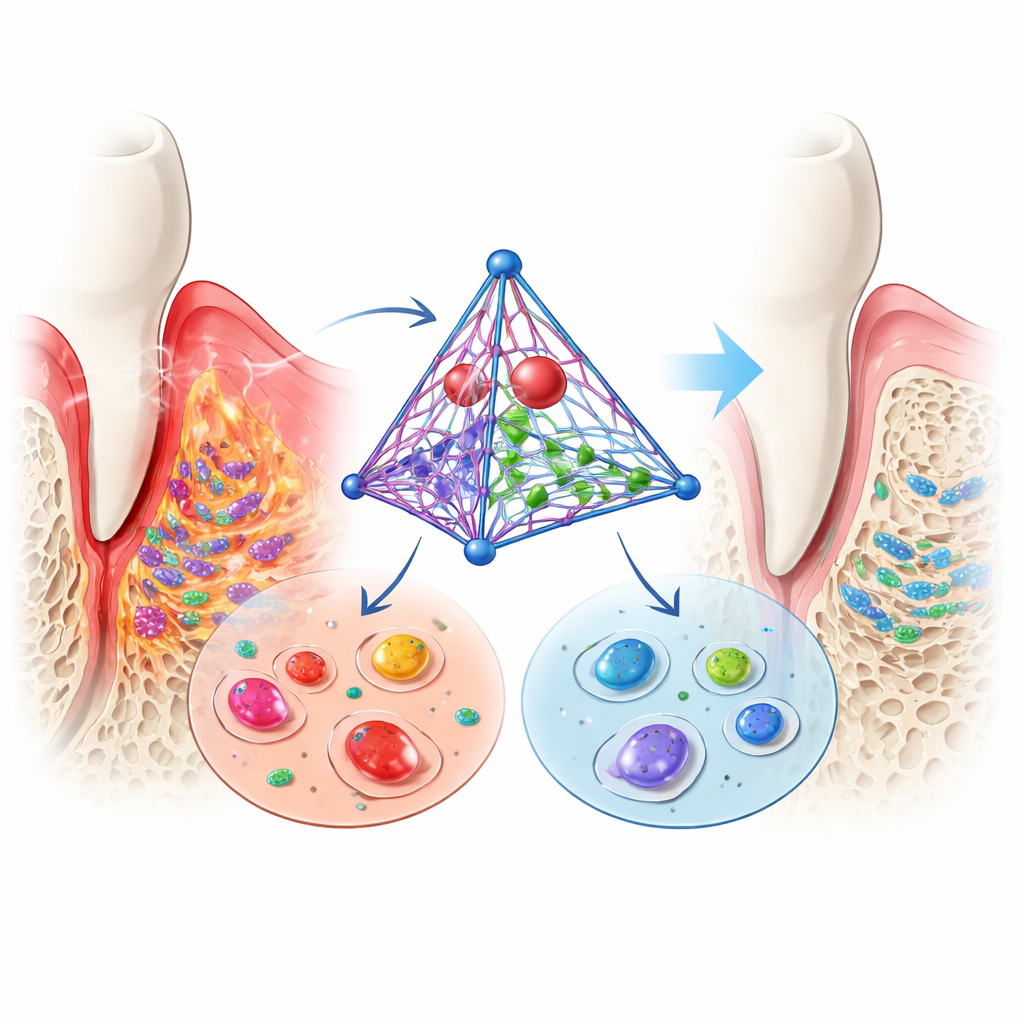
مساعدة الخلايا الجذعية على إعادة بناء العظم المفقود
الخلايا الرباطية التي تُثبت الأسنان يمكن أن تتمايز، في ظروف مناسبة، إلى خلايا مُشكّلة للعظم. في بيئة ملتهبة تحاكي التهاب اللثة، تُكبَح هذه القدرة عادة: تهدأ جينات بناء العظم وتندر الترسبات المعدنية. عندما أضاف الباحثون مُركّب الـDNA، انعكست الحالة. عادت مؤشرات التكوّن العظمي المبكرة والمتأخرة أو تجاوزت المستويات المرصودة في الخلايا الضابطة السليمة، وأنتجت الزرعات المزيد من العقد المعدنية. تشير هذه النتائج إلى أن المنصة لا تحمي الخلايا من الضرر فحسب، بل تدفعها أيضًا نحو إعادة بناء العظم والأنسجة الضامة التي تدعم الأسنان.
برهان المفهوم في لثَة مريضة
لاختبار ما إذا كانت الاستراتيجية تعمل في كائنات حية، اختبر الفريق المركّب في فئران مصابة بالتهاب لثة مستحث بحلقة (ligature-induced periodontitis)، وهو نموذج شائع لمرض اللثة الشديد. الحيوانات التي تلقت حقنًا موضعية من Cur-de-tFNA حول الأسنان المتأثرة فقدت عظمًا داعمًا أقل بكثير — نحو نصف الارتشاف الذي لوحظ في الحيوانات غير المعالجة — وأظهرت عظمًا أكثف وأكثر سماكة في تصوير ثلاثي الأبعاد. كشفت مقاطع الأنسجة عن خلايا مُتبقية مُقللة مسؤولة عن ارتشاف العظم، وألياف كولاجين أكثر انتظامًا، وتقلصًا في تسلل الخلايا الالتهابية. كما انخفضت مؤشرات الدم للالتهاب الجهازي، واكتسبت الجرذان المعالجة وزنًا يشبه الحيوانات الضابطة السليمة، مما يوحي براحة مضغ أفضل وصحة عامة أحسن.
ما الذي قد يعنيه هذا لرعاية الأسنان في المستقبل
بصفة عامة، تقدم الدراسة دواءً نانويًا قائمًا على الـDNA يمكنه، عبر منصة واحدة، قتل البكتيريا الممرضة، وتهدئة الالتهاب الضار، وتشجيع تكوّن عظم جديد حول الأسنان. رغم أن مزيدًا من العمل مطلوب لتأكيد السلامة على المدى الطويل وتكييف النهج للاستخدام البشري، تقدم هذه الاستراتيجية الثلاثية الوظائف لمحة عن علاجات مستقبلية للثة أكثر استهدافًا، أطول أمدًا، وأقل اعتمادًا على المضادات الحيوية واسعة الطيف — وربما تحمي ليس ابتساماتنا فحسب بل صحتنا الجسدية بأكملها.
الاستشهاد: Zhang, G., Cui, W., Wu, H. et al. DNA framework-based nanomedicine platform: a triple-function strategy for treating periodontitis via antibacterial, anti-inflammatory, and osteogenesis-promoting activities. Int J Oral Sci 18, 39 (2026). https://doi.org/10.1038/s41368-026-00439-2
الكلمات المفتاحية: التهاب اللثة, النانو دواء, بنية نانوية من الـDNA, الكركمين, تجديد العظم