Clear Sky Science · zh
COL1A1 诱导的 LOXL2 通过在抑制 EGFR 溶酶体降解时形成反馈回路促进卵巢癌转移
为什么肿瘤“邻里”很重要
卵巢癌之所以常致命,往往不是因为原发肿瘤本身,而是癌细胞在腹腔内广泛播散。本研究考察了肿瘤周围的“邻里”——尤其是一种结构蛋白胶原——如何悄然促使卵巢癌细胞变得更具侵袭性。通过追踪肿瘤细胞与其微环境之间这种隐秘的交流,研究人员发现了一个自我增强的环路,有助于癌症扩散,并提出了可能打破该环路的新策略。
一种会招来麻烦的粘性蛋白
团队关注了名为 LOXL2 的蛋白,它有助于交联胶原和弹性蛋白,使组织具有强度。先前的研究表明,邻近成纤维细胞产生的另一种胶原成分 COL1A1 能增强卵巢癌细胞的迁移性。在本项研究中,科学家发现,当卵巢癌细胞暴露于 COL1A1 时,会显著增加 LOXL2 的产生和分泌。在患者样本中,卵巢癌组织中的 LOXL2 水平明显高于正常卵巢,在转移灶中甚至高于原发肿瘤。肿瘤中 LOXL2 含量更高的女性往往病程更晚期、腹腔积液更多、肿瘤标志物水平更高且生存期更短。
帮助癌细胞移动与侵入
为探明 LOXL2 的实际作用,研究人员在卵巢癌细胞系和小鼠模型中对基因进行开关调控。当他们降低癌细胞中的 LOXL2 时,这些细胞通过人工膜的迁移和侵袭能力减少,细胞用于移动的肌动蛋白“足”结构——即微小突起——也减弱。增强 LOXL2 则产生相反效果:细胞变得更具迁移和侵袭性。在将癌细胞引入腹腔的小鼠模型中,过度产生 LOXL2 的肿瘤形成了更多且更重的转移结节,并缩短了动物的生存期。关键是,当 LOXL2 被沉默时,COL1A1 促进转移的效应在很大程度上消失,表明 LOXL2 是胶原丰富环境与癌细胞扩散之间的重要中介。
隐匿反馈回路如何形成
进一步深入研究时,科学家们探问 COL1A1 如何将 LOXL2 推上高位。他们发现 COL1A1 激活了癌细胞内一条称为 EGFR–MEK–ERK 的信号链。该通路促使转录因子 SP1 从细胞质迁移到含有 DNA 的细胞核内。一旦进入细胞核,SP1 就会结合 LOXL2 基因的特定位点并增强其转录,提升 LOXL2 的产生。用化学抑制剂阻断 MEK–ERK 步骤可以阻止 SP1 进入细胞核,降低 LOXL2 水平,并在小鼠中削减转移,即便存在 COL1A1。归根结底,细胞外的胶原触发了细胞核内的开关,使细胞产生更多 LOXL2。
保护一个强大的生长信号
事情并未就此结束。研究人员发现 LOXL2 还与细胞表面的著名生长受体 EGFR 有物理相互作用,EGFR 能启动 MEK–ERK 通路。LOXL2 并没有改变 EGFR 的基因表达,而是保护 EGFR 蛋白免于被送往细胞的“回收站”——溶酶体。当 LOXL2 水平低时,更多的 EGFR 被标记并送往溶酶体降解;而 LOXL2 水平高时,EGFR 存留更久,下游信号(MEK 和 ERK 的激活)持续存在。LOXL2 的一个特定区域——其 SRC3 结构域——对于结合 EGFR 和促进转移是必需的。这意味着 LOXL2 不仅响应 EGFR 信号,也帮助维持该信号的持续性。
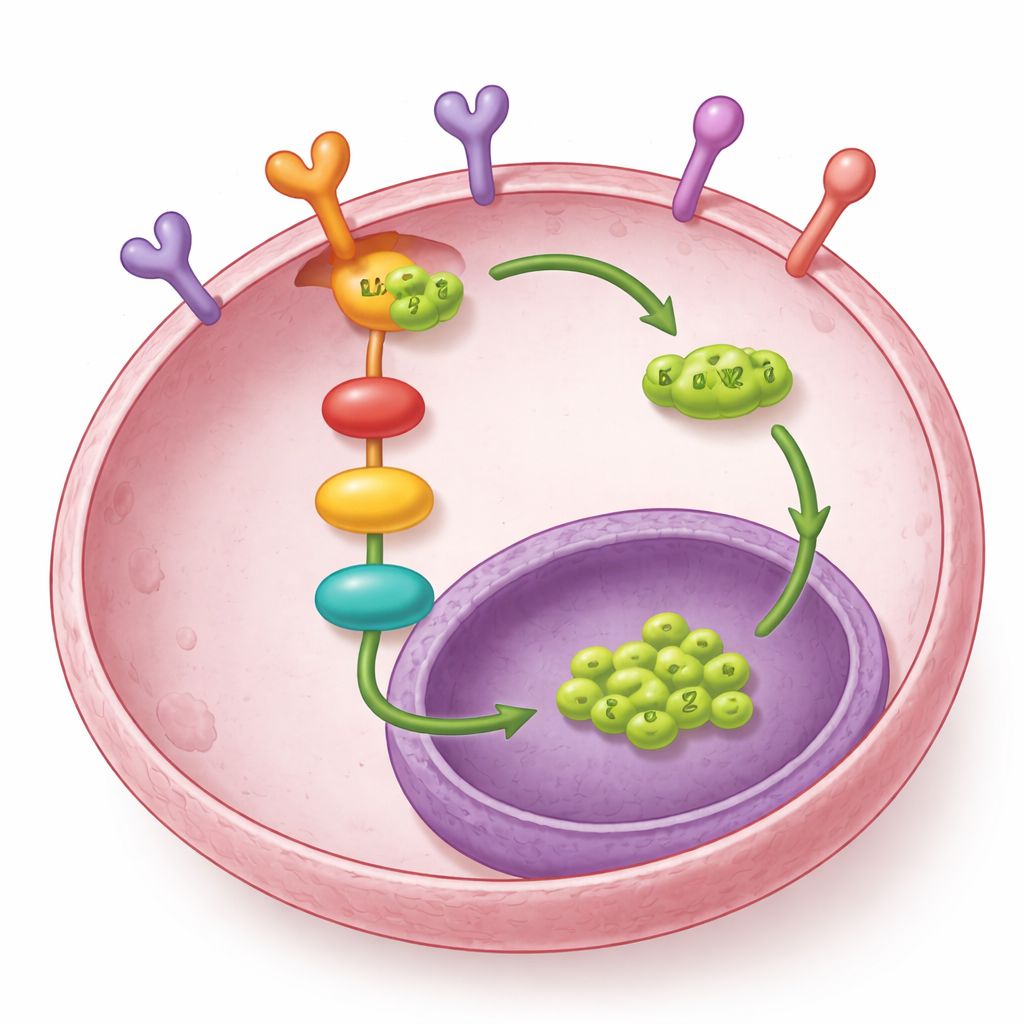
这对未来治疗意味着什么
综合起来,研究结果揭示了一个恶性循环:肿瘤微环境中的 COL1A1 激活卵巢癌细胞中的 EGFR,进而开启 MEK–ERK,使 SP1 进入细胞核并上调 LOXL2 产生。LOXL2 又通过保护 EGFR 免于降解来稳定该受体,反向促进相同通路的持续活跃。该环路帮助癌细胞在腹腔中迁移并播种新瘤灶。对患者而言,这项研究表明靶向 LOXL2——特别是其细胞内功能,而不仅仅是细胞外部分——既可削弱 EGFR 信号,也能抑制转移。与现有的 EGFR 抑制药联合应用,这类策略未来可能为减缓或阻止卵巢癌扩散提供更有效的途径。
引用: Shen, Z., Gu, L., Zheng, M. et al. COL1A1-induced LOXL2 promotes ovarian cancer metastasis via a feedback loop upon inhibiting EGFR lysosomal degradation. Exp Mol Med 58, 864–878 (2026). https://doi.org/10.1038/s12276-026-01675-6
关键词: 卵巢癌转移, 肿瘤微环境, LOXL2, EGFR 信号, 胶原 COL1A1