Clear Sky Science · fr
LOXL2 induit par COL1A1 favorise les métastases de l’ovaire via une boucle de rétroaction en inhibant la dégradation lysosomale d’EGFR
Pourquoi le « quartier » tumoral compte
Le cancer de l’ovaire est souvent mortel non pas à cause de la tumeur initiale, mais parce que les cellules cancéreuses se propagent largement dans l’abdomen. Cette étude examine comment le « quartier » autour d’une tumeur — en particulier une protéine structurale appelée collagène — peut en catimini pousser les cellules ovariennes à devenir plus agressives. En retraçant cette conversation cachée entre les cellules tumorales et leur environnement, les chercheurs mettent au jour une boucle autorenforçante qui facilite la dissémination du cancer et suggèrent de nouvelles approches pour interrompre cette boucle.
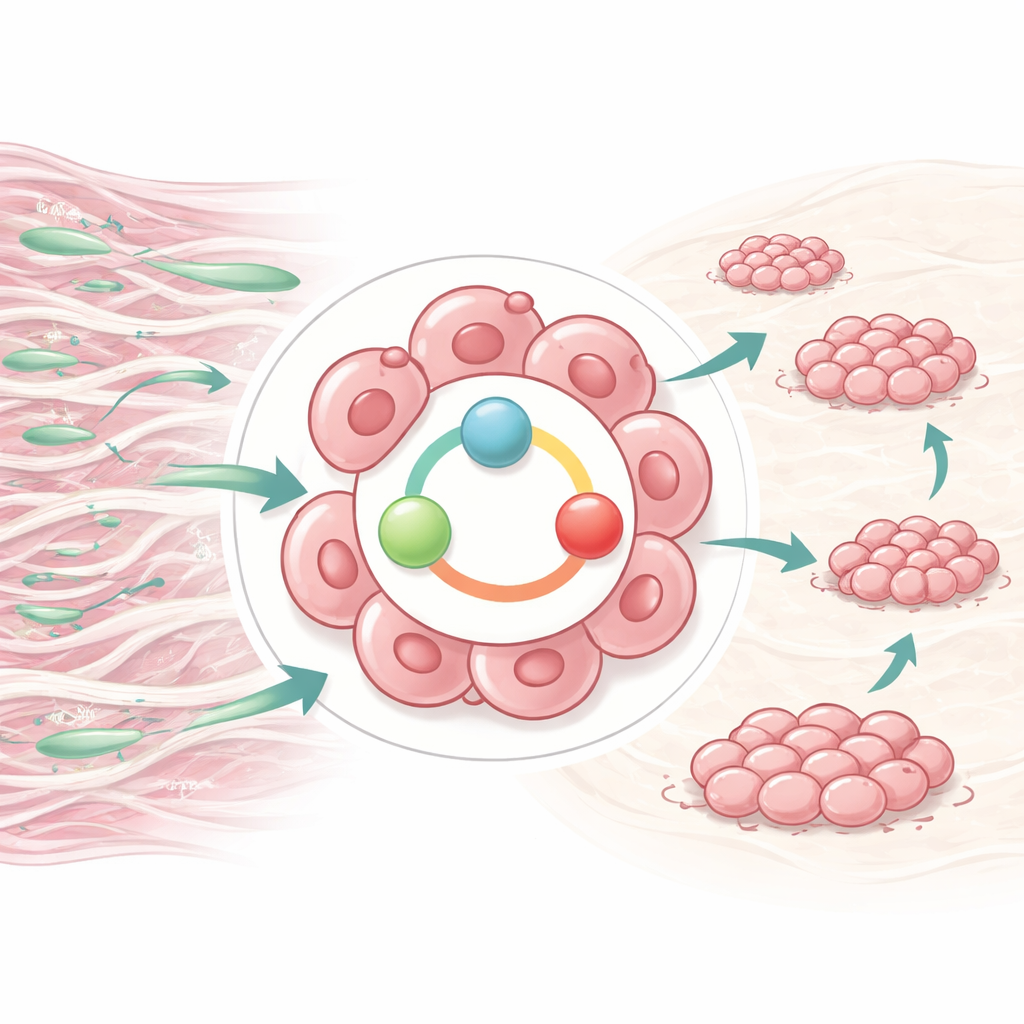
Une protéine collante qui signale des ennuis
L’équipe s’est concentrée sur une protéine appelée LOXL2, qui favorise le réticulage du collagène et de l’élastine, conférant ainsi de la résistance aux tissus. Des travaux antérieurs montraient qu’un autre composant du collagène, COL1A1, produit par des fibroblastes voisins, pouvait augmenter la mobilité des cellules du cancer ovarien. Ici, les scientifiques ont découvert que lorsque les cellules cancéreuses sont exposées à COL1A1, elles augmentent de façon marquée leur production et leur sécrétion de LOXL2. Dans des échantillons de patientes, les niveaux de LOXL2 étaient beaucoup plus élevés dans les tissus cancéreux ovariens que dans les ovaires normaux, et encore plus élevés dans les foyers métastatiques que dans les tumeurs primaires. Les femmes dont les tumeurs présentaient plus de LOXL2 avaient tendance à présenter une maladie plus avancée, un plus grand épanchement abdominal, des taux plus élevés de marqueurs tumoraux et une survie plus courte.
Faciliter le mouvement et l’invasion des cellules cancéreuses
Pour déterminer ce que fait réellement LOXL2, les chercheurs ont modulé des gènes dans des lignées cellulaires du cancer ovarien et chez la souris. Lorsque LOXL2 était réduit dans les cellules cancéreuses, ces cellules migraient et envahissaient moins à travers des membranes artificielles, et leurs structures d’« pieds » actine — de petites protrusions utilisées pour le mouvement — étaient diminuées. À l’inverse, l’augmentation de LOXL2 rendait les cellules plus mobiles et invasives. Dans des modèles murins où des cellules cancéreuses étaient introduites dans la cavité abdominale, les tumeurs surexprimant LOXL2 formaient davantage de nodules métastatiques, plus lourds, et raccourcissaient la survie des animaux. De façon cruciale, lorsque LOXL2 était inhibé, l’effet pro-métastatique de COL1A1 disparaissait en grande partie, montrant que LOXL2 est un médiateur clé entre l’environnement riche en collagène et la propagation tumorale.
Comment se forme une boucle de rétroaction cachée
En approfondissant, les scientifiques se sont demandé comment COL1A1 augmentait autant les niveaux de LOXL2. Ils ont découvert que COL1A1 active une cascade de signaux à l’intérieur des cellules cancéreuses connue sous le nom de voie EGFR–MEK–ERK. Cette voie déplace un facteur de transcription nommé SP1 du cytoplasme vers le noyau, où se trouve l’ADN. Une fois dans le noyau, SP1 se lie à une région spécifique du gène LOXL2 et l’active plus fortement, augmentant ainsi la production de LOXL2. Le blocage de l’étape MEK–ERK avec un inhibiteur chimique empêchait SP1 d’entrer dans le noyau, réduisait les niveaux de LOXL2 et diminuait les métastases chez la souris, même en présence de COL1A1. En substance, le collagène extracellulaire active un interrupteur nucléaire qui incite la cellule à produire davantage de LOXL2.
Protection d’un signal de croissance puissant
L’histoire ne s’arrête pas là. Les chercheurs ont constaté que LOXL2 interagit également physiquement avec EGFR, un récepteur de croissance bien connu à la surface cellulaire qui initie la voie MEK–ERK. Plutôt que d’altérer l’expression du gène EGFR, LOXL2 protège la protéine EGFR d’être envoyée vers la « benne » cellulaire, le lysosome. Lorsque LOXL2 était bas, davantage d’EGFR était étiqueté pour la destruction et finissait dans les lysosomes ; lorsque LOXL2 était élevé, EGFR persistait plus longtemps et la signalisation en aval (activation de MEK et ERK) restait continue. Une région spécifique de LOXL2 — son domaine SRC3 — était essentielle pour se lier à EGFR et promouvoir les métastases. Cela signifie que LOXL2 non seulement répond à la signalisation EGFR, mais contribue aussi à maintenir cette signalisation active.
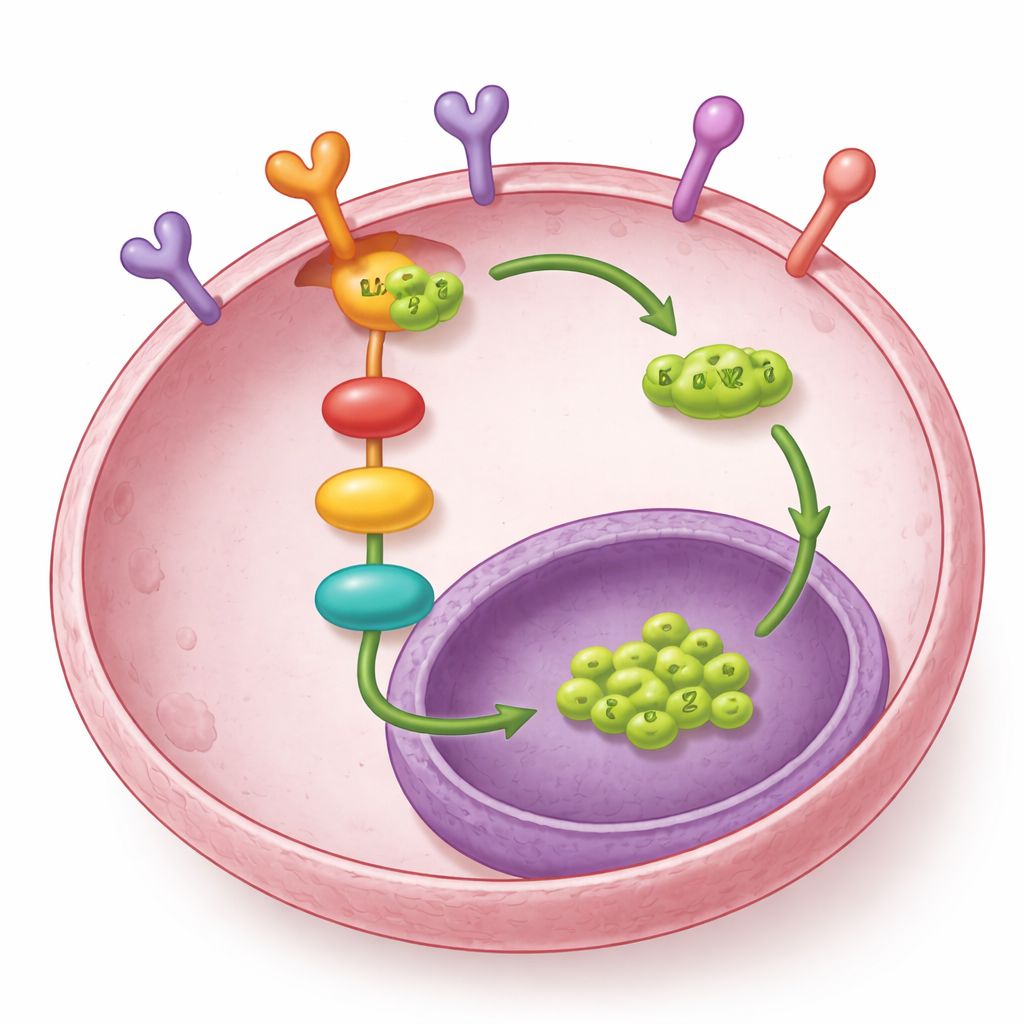
Ce que cela implique pour les traitements futurs
En synthèse, les résultats révèlent un cercle vicieux : COL1A1 dans l’environnement tumoral active EGFR dans les cellules du cancer ovarien, ce qui déclenche MEK–ERK, déplace SP1 vers le noyau et augmente la production de LOXL2. LOXL2, à son tour, stabilise EGFR en le protégeant de la dégradation, bouclant ainsi le circuit pour maintenir la voie active. Cette boucle aide les cellules cancéreuses à migrer et à coloniser de nouveaux foyers dans l’abdomen. Pour les patientes, ces travaux suggèrent que cibler LOXL2 — en particulier ses actions intracellulaires, et pas seulement sa portion extracellulaire — pourrait affaiblir la signalisation EGFR et réduire les métastases. Combinées aux traitements existants bloquant EGFR, de telles stratégies pourraient, un jour, offrir des moyens plus efficaces de ralentir ou d’arrêter la propagation du cancer de l’ovaire.
Citation: Shen, Z., Gu, L., Zheng, M. et al. COL1A1-induced LOXL2 promotes ovarian cancer metastasis via a feedback loop upon inhibiting EGFR lysosomal degradation. Exp Mol Med 58, 864–878 (2026). https://doi.org/10.1038/s12276-026-01675-6
Mots-clés: métastases du cancer de l’ovaire, microenvironnement tumoral, LOXL2, signalisation EGFR, collagène COL1A1