Clear Sky Science · pt
COL1A1 induzido por LOXL2 promove a metástase do câncer de ovário por meio de um circuito de retroalimentação ao impedir a degradação lisossomal do EGFR
Por que o bairro do tumor importa
O câncer de ovário costuma ser fatal não por causa do tumor primário, mas porque as células cancerosas se espalham amplamente pela cavidade abdominal. Este estudo investiga como a “vizinhança” ao redor de um tumor — em especial uma proteína estrutural chamada colágeno — pode, de forma silenciosa, orientar as células do câncer de ovário a se tornarem mais agressivas. Ao traçar essa conversa oculta entre as células tumorais e seu entorno, os pesquisadores revelam um circuito autorreforçador que facilita a disseminação do câncer e sugerem novas maneiras de interromper esse ciclo.
Uma proteína pegajosa que sinaliza perigo
A equipe concentrou-se em uma proteína chamada LOXL2, que ajuda a entrecruzar colágeno e elastina, conferindo resistência aos tecidos. Trabalhos anteriores mostraram que um outro componente do colágeno, COL1A1, produzido por fibroblastos próximos, pode aumentar a mobilidade das células de câncer de ovário. Aqui, os cientistas descobriram que, quando as células do câncer de ovário são expostas ao COL1A1, elas aumentam dramaticamente sua produção e secreção de LOXL2. Em amostras de pacientes, os níveis de LOXL2 eram muito maiores no tecido de câncer de ovário do que em ovários normais, e ainda mais elevados nos depósitos metastáticos em comparação com os tumores primários. Mulheres cujos tumores apresentavam mais LOXL2 tendiam a ter doença mais avançada, maior acúmulo de líquido abdominal, níveis mais altos de marcadores tumorais e sobrevivência mais curta.
Auxiliando a movimentação e invasão das células cancerosas
Para entender o que o LOXL2 realmente faz, os pesquisadores ativaram e silenciaram genes em linhagens de células de câncer de ovário e em camundongos. Quando reduziram o LOXL2 nas células cancerosas, essas células migraram e invadiram menos através de membranas artificiais, e suas estruturas de actina — pequenos prolongamentos usados para locomoção — estavam diminuídas. Aumentar o LOXL2 teve o efeito oposto: as células tornaram-se mais móveis e invasivas. Em modelos murinos nos quais as células cancerosas foram introduzidas na cavidade abdominal, tumores que superproduziam LOXL2 formaram mais nódulos metastáticos e mais pesados, encurtando a sobrevivência dos animais. Crucialmente, quando o LOXL2 foi silenciado, o efeito de promoção de metástase induzido pelo COL1A1 desapareceu em grande parte, mostrando que o LOXL2 é um mediador-chave entre o ambiente rico em colágeno e a disseminação do câncer.
Como se forma um circuito de retroalimentação oculto
Aprofundando-se, os cientistas investigaram como o COL1A1 eleva tanto os níveis de LOXL2. Descobriram que o COL1A1 ativa uma cascata de sinais dentro das células cancerosas conhecida como via EGFR–MEK–ERK. Essa via desloca um fator de transcrição chamado SP1 do citoplasma para o núcleo da célula, onde o DNA é armazenado. Uma vez no núcleo, o SP1 se liga a uma região específica do gene LOXL2 e o ativa mais fortemente, aumentando a produção de LOXL2. Bloquear a etapa MEK–ERK com um inibidor químico impediu a entrada do SP1 no núcleo, reduziu os níveis de LOXL2 e diminuiu a metástase em camundongos, mesmo na presença de COL1A1. Em essência, o colágeno fora da célula aciona um interruptor dentro do núcleo que diz à célula para produzir mais LOXL2.
Protegendo um sinal poderoso de crescimento
A história não termina aí. Os pesquisadores descobriram que o LOXL2 também interage fisicamente com o EGFR, um receptor de crescimento bem conhecido na superfície celular que inicia a via MEK–ERK. Em vez de alterar a atividade gênica do EGFR, o LOXL2 protege a proteína EGFR de ser enviada para a “lixeira” da célula, o lisossomo. Quando o LOXL2 estava baixo, mais EGFR era marcado para degradação e acabava nos lisossomos; quando o LOXL2 estava alto, o EGFR persistia por mais tempo e a sinalização a jusante (ativação de MEK e ERK) permanecia ativa. Uma região específica do LOXL2 — seu domínio SRC3 — foi essencial para ligar-se ao EGFR e promover a metástase. Isso significa que o LOXL2 não apenas responde à sinalização do EGFR, mas também ajuda a manter essa sinalização ativa.
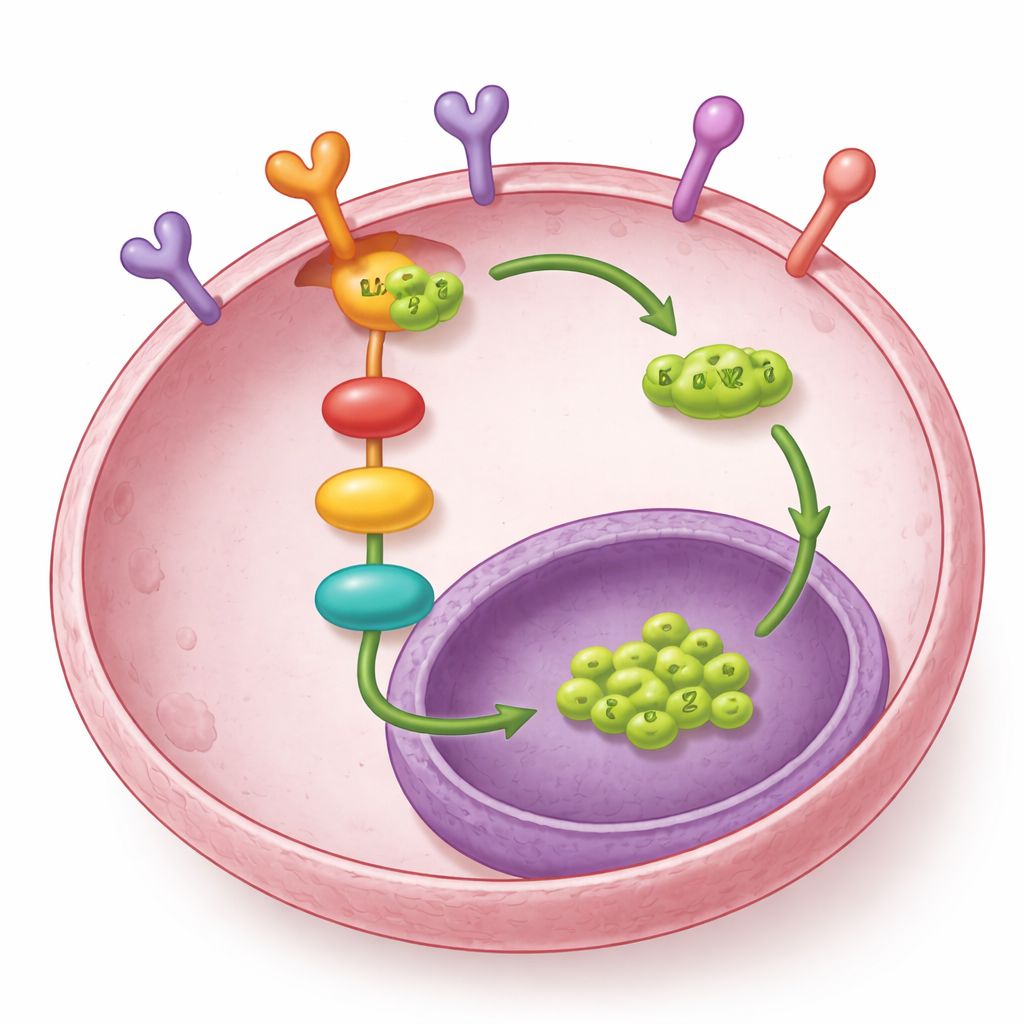
O que isso significa para tratamentos futuros
Juntos, os achados revelam um círculo vicioso: o COL1A1 no entorno do tumor ativa o EGFR nas células de câncer de ovário, que liga MEK–ERK, desloca o SP1 para o núcleo e aumenta a produção de LOXL2. O LOXL2, por sua vez, estabiliza o EGFR ao protegê-lo da degradação, retroalimentando para manter a mesma via ativa. Esse circuito ajuda as células cancerosas a se locomoverem e semearem novos tumores por toda a cavidade abdominal. Para os pacientes, essa pesquisa sugere que direcionar o LOXL2 — especialmente suas ações internas, não apenas a porção extracelular — poderia enfraquecer a sinalização do EGFR e diminuir a metástase. Em combinação com medicamentos existentes que bloqueiam o EGFR, tais estratégias podem um dia oferecer formas mais eficazes de retardar ou interromper a disseminação do câncer de ovário.
Citação: Shen, Z., Gu, L., Zheng, M. et al. COL1A1-induced LOXL2 promotes ovarian cancer metastasis via a feedback loop upon inhibiting EGFR lysosomal degradation. Exp Mol Med 58, 864–878 (2026). https://doi.org/10.1038/s12276-026-01675-6
Palavras-chave: metástase do câncer de ovário, microambiente tumoral, LOXL2, sinalização do EGFR, colágeno COL1A1