Clear Sky Science · de
COL1A1-induziertes LOXL2 fördert die Metastasierung von Ovarialkarzinomen über eine Rückkopplungsschleife durch Hemmung des lysosomalen Abbaus von EGFR
Warum die Nachbarschaft des Tumors wichtig ist
Ovarialkarzinome sind oft tödlich, nicht wegen des Primärtumors an sich, sondern weil sich Krebszellen weit im Bauchraum ausbreiten. Diese Studie untersucht, wie die „Nachbarschaft“ um einen Tumor – insbesondere ein Strukturprotein namens Kollagen – ovarianen Krebszellen heimlich dazu bringen kann, aggressiver zu werden. Indem die Forschenden dieses versteckte Gespräch zwischen Tumorzellen und ihrer Umgebung nachzeichnen, decken sie eine sich selbst verstärkende Schleife auf, die das Fortschreiten begünstigt, und zeigen mögliche Ansätze auf, wie man diese Schleife durchbrechen könnte.
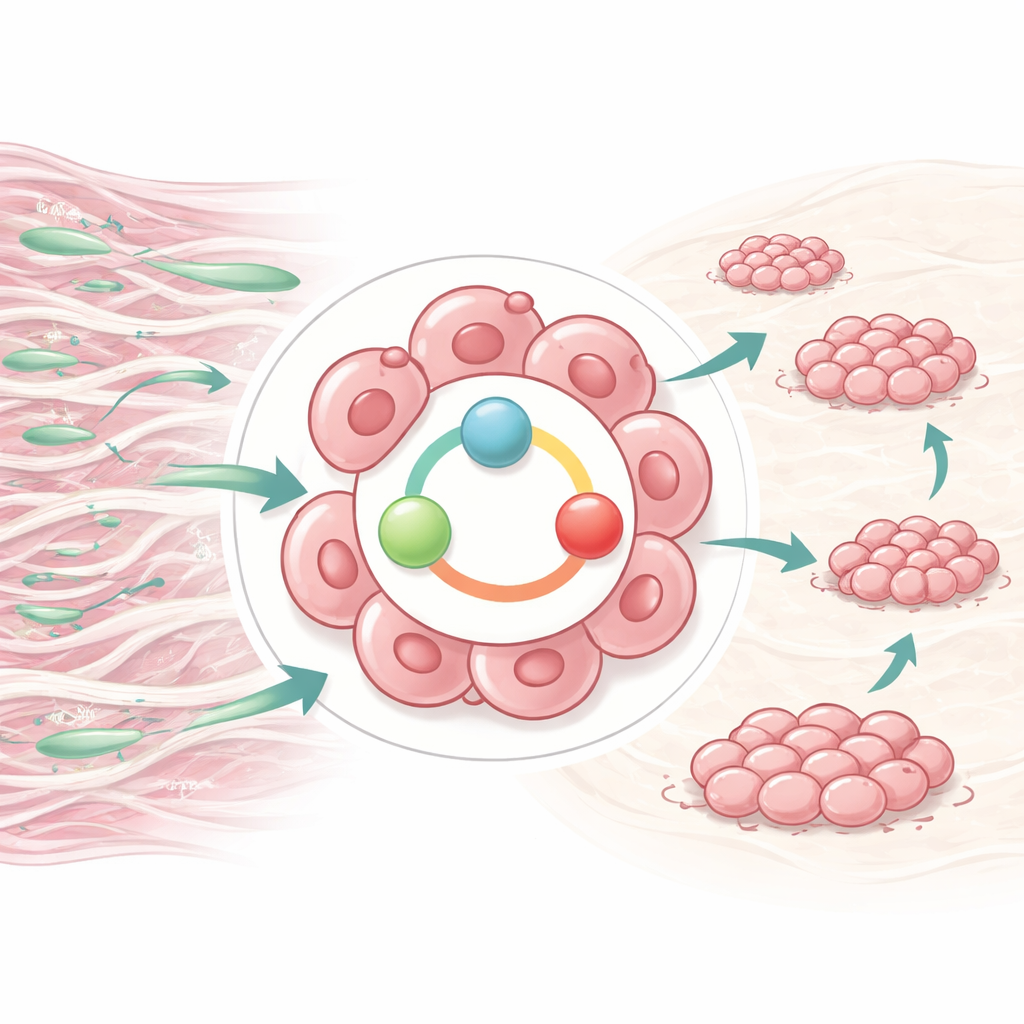
Ein klebriges Protein, das Ärger ankündigt
Das Team konzentrierte sich auf ein Protein namens LOXL2, das Kollagen und Elastin vernetzt und Gewebe Festigkeit verleiht. Frühere Arbeiten zeigten, dass ein anderes Kollagenprotein, COL1A1, das von benachbarten Fibroblasten produziert wird, die Beweglichkeit von Ovarialkarzinomzellen erhöhen kann. Hier fanden die Forschenden heraus, dass Ovarialkarzinomzellen nach Exposition gegenüber COL1A1 ihre Produktion und Sekretion von LOXL2 dramatisch steigern. In Patientenproben waren die LOXL2-Spiegel im Krebsgewebe deutlich höher als in normalen Ovarien und in metastatischen Ablagerungen noch höher als im Primärtumor. Frauen, deren Tumoren höhere LOXL2-Werte aufwiesen, hatten tendenziell fortgeschrittenere Erkrankungen, stärkere Aszitesbildung, höhere Tumormarkerwerte und eine kürzere Überlebenszeit.
Wie LOXL2 Krebszellen beim Wandern und Eindringen hilft
Um zu prüfen, was LOXL2 tatsächlich bewirkt, schalteten die Forschenden Gene in Ovarialkarzinomzelllinien und in Mäusen an und aus. Reduzierten sie LOXL2 in Krebszellen, bewegten sich diese Zellen weniger und zeigten geringere Invasivität durch künstliche Membranen; auch ihre actinbasierten „Füße“ – winzige Ausstülpungen für die Bewegung – waren reduziert. Eine Erhöhung von LOXL2 führte zum Gegenteil: Zellen wurden beweglicher und invasiver. In Mausmodellen, in denen Krebszellen in die Bauchhöhle eingebracht wurden, bildeten Tumoren mit LOXL2-Überproduktion mehr und schwerere metastatische Herde und verkürzten das Überleben der Tiere. Entscheidend war, dass bei Stummschaltung von LOXL2 der metastasierende Effekt von COL1A1 größtenteils verschwand, was zeigt, dass LOXL2 ein wichtiger Vermittler zwischen der kollagenreichen Umgebung und der Tumorausbreitung ist.
Wie eine versteckte Rückkopplungsschleife entsteht
Bei genauerer Untersuchung fragten die Forschenden, wie COL1A1 die LOXL2-Spiegel derart hoch treibt. Sie entdeckten, dass COL1A1 eine Signalkaskade in Krebszellen aktiviert, bekannt als EGFR–MEK–ERK-Weg. Dieser Weg veranlasst den Transkriptionsfaktor SP1, vom Zytoplasma in den Zellkern zu wandern, wo die DNA liegt. Dort bindet SP1 an eine spezifische Region des LOXL2-Gens und erhöht dessen Aktivität, wodurch mehr LOXL2 produziert wird. Das Blockieren des MEK–ERK-Schritts mit einem chemischen Inhibitor verhinderte das Eintreten von SP1 in den Kern, reduzierte LOXL2-Spiegel und verringerte die Metastasierung in Mäusen, selbst bei Vorhandensein von COL1A1. Im Kern bedeutet das: Kollagen außerhalb der Zelle schaltet einen Schalter im Zellkern, der die Zelle anweist, mehr LOXL2 zu produzieren.
Schutz eines starken Wachstumsignals
Die Geschichte endet nicht dort. Die Forschenden fanden, dass LOXL2 auch physisch mit EGFR interagiert, einem bekannten Wachstumsrezeptor an der Zelloberfläche, der den MEK–ERK-Weg initiiert. Anstatt die Genaktivität von EGFR zu verändern, schützt LOXL2 das EGFR-Protein davor, in das lysosomale „Recycling“-System der Zelle geschickt zu werden. Bei niedrigen LOXL2-Werten wurde mehr EGFR für den Abbau markiert und gelangte in Lysosomen; bei hohen LOXL2-Werten blieb EGFR länger erhalten und die nachgeschaltete Signalgebung (MEK- und ERK-Aktivierung) blieb aktiv. Eine spezifische Region von LOXL2 – die SRC3-Domäne – war essentiell für die Bindung an EGFR und für die Förderung der Metastasierung. Das bedeutet, LOXL2 reagiert nicht nur auf EGFR-Signale, sondern trägt auch dazu bei, diese Signale aufrechtzuerhalten.
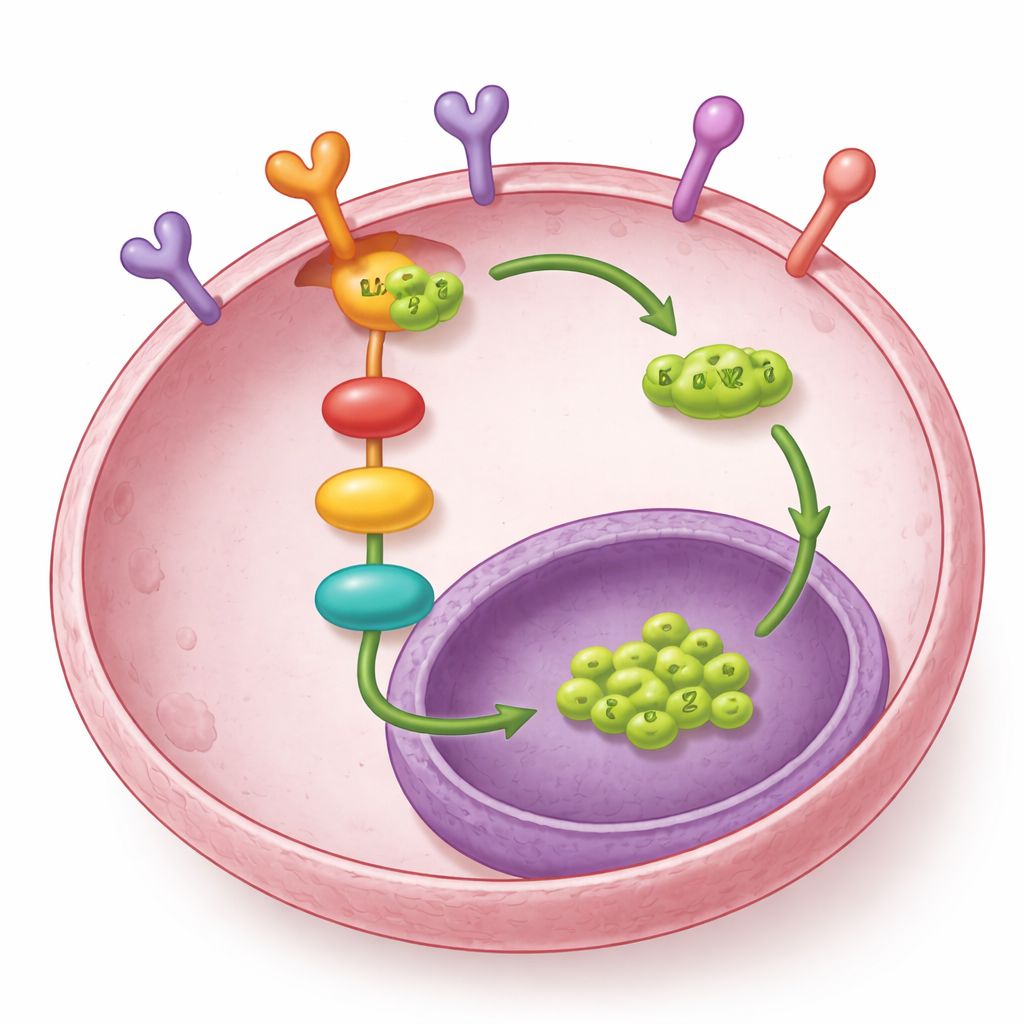
Was das für zukünftige Therapien bedeutet
In der Zusammenfassung zeigen die Befunde einen Teufelskreis: COL1A1 in der Tumornachbarschaft aktiviert EGFR in Ovarialkarzinomzellen, was MEK–ERK einschaltet, SP1 in den Kern verschiebt und die LOXL2-Produktion hochfährt. LOXL2 stabilisiert wiederum EGFR, indem es diesen vor dem Abbau schützt, und hält so den gleichen Signalweg aktiv. Diese Schleife erleichtert es Krebszellen, sich zu verbreiten und neue Tumoren im Bauchraum anzusiedeln. Für Patientinnen legt diese Forschung nahe, dass das gezielte Blockieren von LOXL2 – insbesondere seiner intrazellulären Funktionen und nicht nur der extrazellulären Anteile – sowohl die EGFR-Signalgebung schwächen als auch die Metastasierung abschwächen könnte. In Kombination mit bestehenden EGFR-blockierenden Medikamenten könnten solche Strategien eines Tages wirksamere Möglichkeiten bieten, die Ausbreitung von Ovarialkarzinomen zu verlangsamen oder zu stoppen.
Zitation: Shen, Z., Gu, L., Zheng, M. et al. COL1A1-induced LOXL2 promotes ovarian cancer metastasis via a feedback loop upon inhibiting EGFR lysosomal degradation. Exp Mol Med 58, 864–878 (2026). https://doi.org/10.1038/s12276-026-01675-6
Schlüsselwörter: Metastasierung von Ovarialkarzinomen, tumorales Mikroenvironment, LOXL2, EGFR-Signalgebung, Kollagen COL1A1