Clear Sky Science · es
LOXL2 inducido por COL1A1 promueve la metástasis del cáncer de ovario mediante un circuito de retroalimentación al inhibir la degradación lisosomal de EGFR
Por qué importa el vecindario del tumor
El cáncer de ovario suele ser mortal no tanto por el tumor primario, sino porque las células cancerosas se diseminan ampliamente por la cavidad abdominal. Este estudio examina cómo el “vecindario” alrededor del tumor —especialmente una proteína estructural llamada colágeno— puede, de forma silenciosa, incitar a las células de cáncer de ovario a volverse más agresivas. Al trazar esta conversación oculta entre las células tumorales y su entorno, los investigadores desvelan un circuito autorreforzante que facilita la diseminación y sugieren nuevas vías para que los médicos puedan interrumpir ese circuito.
Una proteína pegajosa que anuncia problemas
El equipo se centró en una proteína llamada LOXL2, que ayuda a entrecruzar colágeno y elastina, confiriendo resistencia a los tejidos. Trabajos anteriores mostraron que otro componente del colágeno, COL1A1, producido por fibroblastos cercanos, podía aumentar la movilidad de las células de cáncer de ovario. Aquí, los científicos hallaron que cuando las células tumorales de ovario se exponen a COL1A1, aumentan de forma notable su producción y secreción de LOXL2. En muestras de pacientes, los niveles de LOXL2 eran mucho más altos en tejido de cáncer de ovario que en ovarios normales, y aún más elevados en depósitos metastásicos en comparación con los tumores primarios. Las mujeres cuyos tumores presentaban más LOXL2 tendían a tener enfermedad más avanzada, mayor acumulación de líquido abdominal, niveles más altos de marcadores tumorales y supervivencia más corta.
Facilitando el movimiento y la invasión de las células cancerosas
Para determinar qué hace realmente LOXL2, los investigadores activaron y silenciaron genes en líneas celulares de cáncer de ovario y en ratones. Cuando redujeron LOXL2 en las células cancerosas, esas células se movieron e invadieron menos a través de membranas artificiales, y sus estructuras de actina —pequeñas protrusiones usadas para el movimiento— se veían disminuidas. Aumentar LOXL2 produjo el efecto contrario: las células se volvieron más móviles e invasivas. En modelos murinos donde se introdujeron células cancerosas en la cavidad abdominal, los tumores que sobreproducían LOXL2 formaron más nódulos metastásicos y de mayor peso, acortando la supervivencia de los animales. De forma crucial, cuando LOXL2 fue silenciado, el efecto pro-metastásico de COL1A1 desapareció en gran medida, mostrando que LOXL2 es un intermediario clave entre el entorno rico en colágeno y la diseminación tumoral.
Cómo se forma un bucle de retroalimentación oculto
Profundizando más, los científicos investigaron cómo COL1A1 eleva tanto los niveles de LOXL2. Descubrieron que COL1A1 activa una cadena de señales dentro de las células tumorales conocida como vía EGFR–MEK–ERK. Esta vía moviliza un factor de transcripción llamado SP1 desde el citoplasma hacia el núcleo, donde se aloja el ADN. Una vez dentro, SP1 se une a una región específica del gen LOXL2 y lo activa con más intensidad, aumentando la producción de LOXL2. Bloquear el paso MEK–ERK con un inhibidor químico impidió que SP1 entrara en el núcleo, redujo los niveles de LOXL2 y disminuyó la metástasis en ratones, incluso en presencia de COL1A1. En esencia, el colágeno fuera de la célula enciende un interruptor dentro del núcleo que ordena a la célula producir más LOXL2.
Protegiendo una señal de crecimiento poderosa
La historia no termina ahí. Los investigadores hallaron que LOXL2 también interactúa físicamente con EGFR, un receptor de crecimiento bien conocido en la superficie celular que inicia la vía MEK–ERK. En lugar de alterar la actividad génica de EGFR, LOXL2 protege la proteína EGFR de ser enviada al “cubo de reciclaje” de la célula, el lisosoma. Cuando LOXL2 era bajo, más EGFR quedaba marcado para destrucción y acababa en lisosomas; cuando LOXL2 era alto, EGFR persistía más tiempo y la señalización aguas abajo (activación de MEK y ERK) permanecía activa. Una región específica de LOXL2 —su dominio SRC3— fue esencial para unirse a EGFR y promover la metástasis. Esto significa que LOXL2 no solo responde a la señalización de EGFR, sino que también contribuye a mantener esa señal activa.
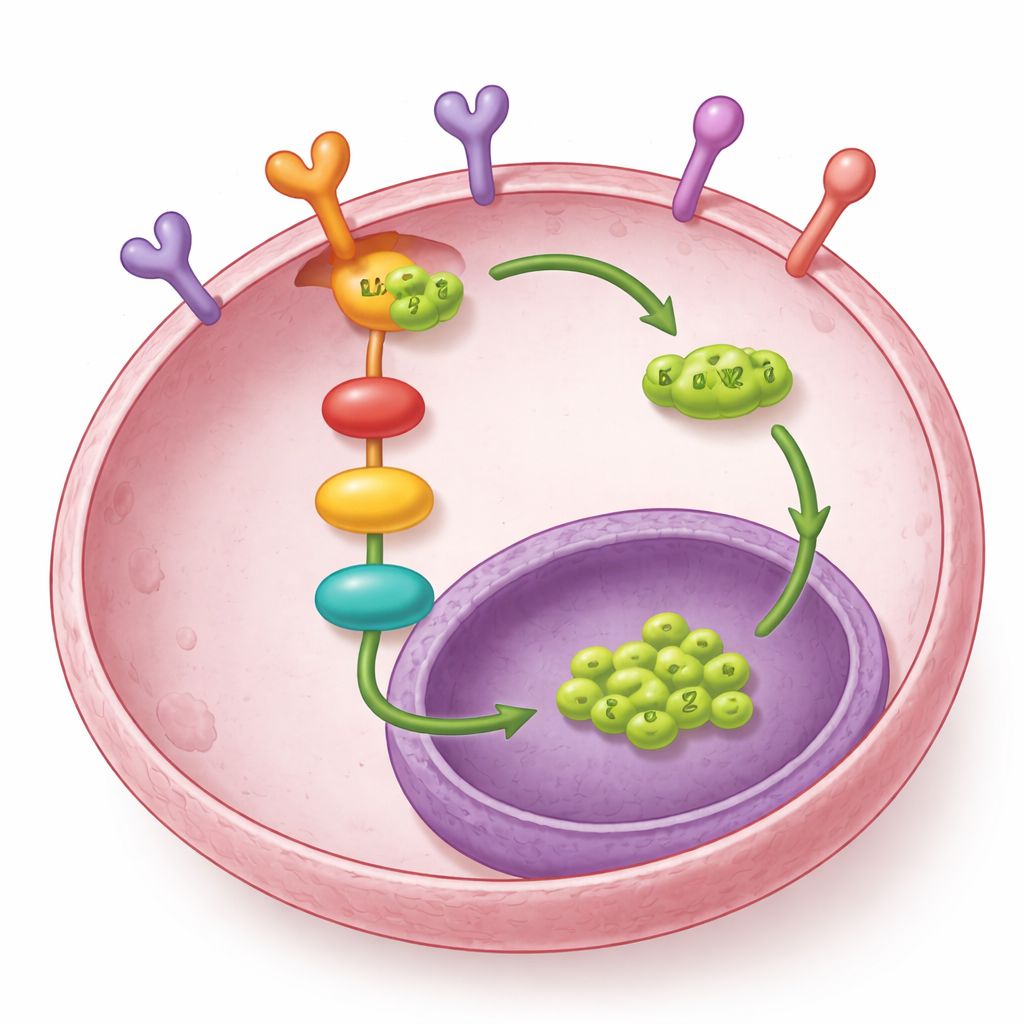
Qué implica esto para tratamientos futuros
En conjunto, los hallazgos revelan un círculo vicioso: COL1A1 en el entorno tumoral activa EGFR en las células de cáncer de ovario, lo que enciende MEK–ERK, moviliza SP1 al núcleo y aumenta la producción de LOXL2. LOXL2, a su vez, estabiliza EGFR protegiéndolo de la degradación, retroalimentando para mantener la misma vía en funcionamiento. Este bucle ayuda a las células cancerosas a desplazarse y sembrar nuevos tumores por toda la cavidad abdominal. Para las pacientes, esta investigación sugiere que dirigirse a LOXL2 —especialmente a sus acciones internas, no solo a la porción extracelular— podría debilitar la señalización de EGFR y frenar la metástasis. Combinadas con fármacos existentes que bloquean EGFR, dichas estrategias podrían algún día ofrecer maneras más efectivas de ralentizar o detener la propagación del cáncer de ovario.
Cita: Shen, Z., Gu, L., Zheng, M. et al. COL1A1-induced LOXL2 promotes ovarian cancer metastasis via a feedback loop upon inhibiting EGFR lysosomal degradation. Exp Mol Med 58, 864–878 (2026). https://doi.org/10.1038/s12276-026-01675-6
Palabras clave: metástasis del cáncer de ovario, microambiente tumoral, LOXL2, señalización de EGFR, colágeno COL1A1