Clear Sky Science · zh
富含脯氨酸/丝氨酸的卷曲螺旋蛋白1通过重塑由粘膜阿克曼氏菌介导的色氨酸代谢缓解动脉粥样硬化
肠道微生物与一个隐秘基因如何共同影响心脏健康
动脉粥样硬化——动脉逐渐被堵塞和瘢痕化的过程——通常被归咎于高胆固醇和炎症。本研究揭示了一个令人意外的新角色:一个鲜少被研究的人类基因PSRC1,它通过与一种喜爱黏液的肠道微生物及由膳食蛋白产生的分子协同作用来保护动脉。三者形成一条从结肠到动脉壁免疫细胞的连锁反应,或为高危心血管患者提供精准治疗的新思路。
守护动脉的基因
研究者聚焦于PSRC1,这一基因在大型基因组研究中曾被提示与冠状动脉疾病相关。早期小鼠研究表明,缺失PSRC1会加重动脉粥样硬化,部分原因是扰乱了肠道微生物组。在这项研究中,团队证实缺失PSRC1的小鼠在摄入与对照组相同高脂饮食的情况下,仍然形成更大且更脆弱的斑块。它们的动脉壁显示出更大范围的脂质堆积、斑块内更大的坏死区和更少的支撑性胶原——这些都是易破裂、可诱发心肌梗死和中风的危险病变特征。
当黏液屏障与关键微生物消失时
为探明宿主基因如何影响肠道微生物,科学家们检查了缺失PSRC1小鼠的肠道。他们发现覆盖结肠的保护性黏液层变薄,分泌黏液的杯状细胞减少,肠细胞间的连接也被削弱。受损的屏障更容易导致有益细菌的丧失。尤其是一种通常靠分解黏液为生并有助于维护黏液层的微生物——粘膜阿克曼氏菌(Akkermansia muciniphila)显著减少。鉴于阿克曼氏菌与对抗肥胖、炎症和动脉粥样硬化有关,它的消失为PSRC1缺失与动脉病情恶化之间提供了合理的联系。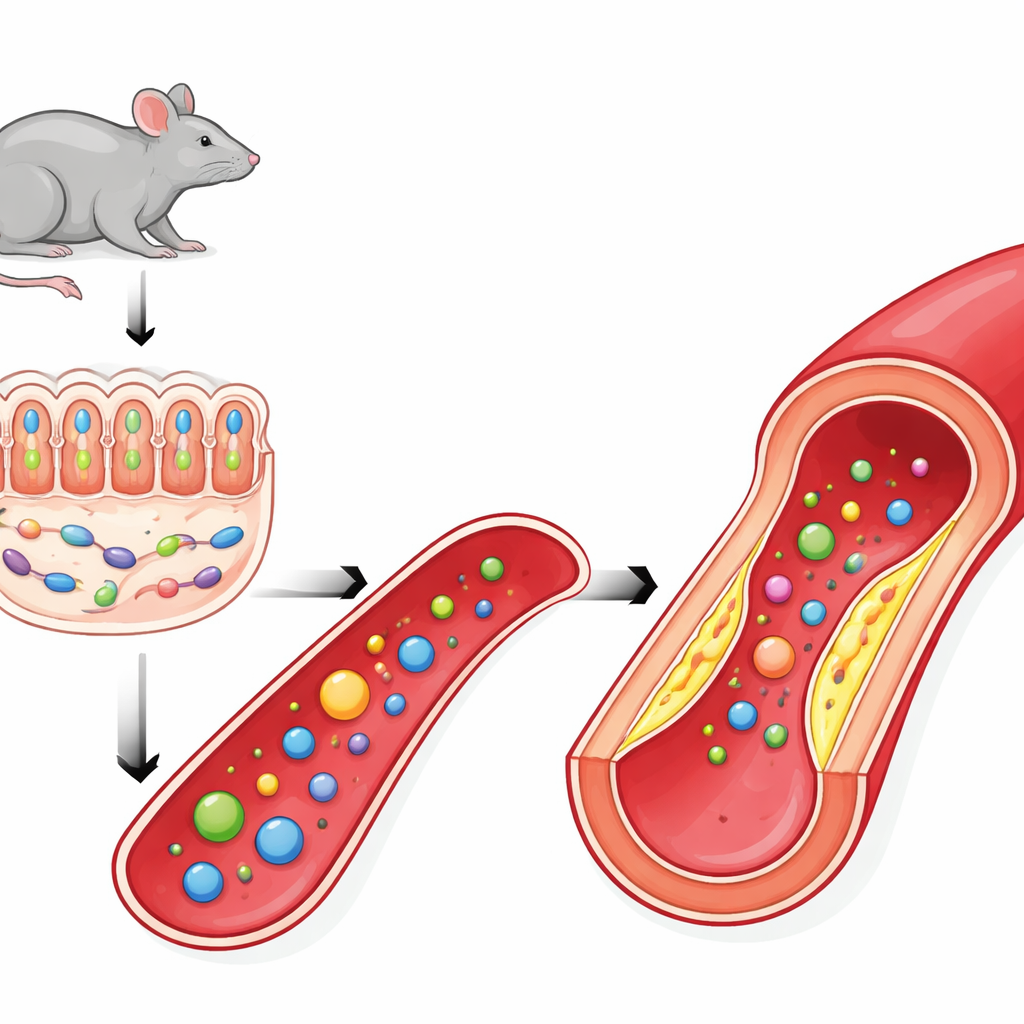
从膳食蛋白到保护性信号
团队随后关注色氨酸,这种来自食物的必需氨基酸可被肠道细菌转化为多种化学信使。在缺失PSRC1的小鼠血液中,若干色氨酸衍生物下降,尤其是吲哚-3-乙酸(IAA),这是一种在实验模型中已知可抑制炎症和氧化应激的产物。IAA可激活免疫细胞内的一种感受器——芳香烃受体(AHR),进而调控有助于限制炎症和细胞死亡的基因。在突变小鼠中,肝脏、结肠以及关键的斑块内巨噬细胞中的AHR活性及其下游标志物均下降——巨噬细胞是吞噬脂质的免疫细胞,其行为可使斑块稳定或不稳定。
为免疫细胞搭建的微生物—分子生命线
为检验恢复阿克曼氏菌或IAA是否能挽救受损系统,研究者在用抗生素清除本土菌群后,给予缺失PSRC1的小鼠活菌或热灭活的阿克曼氏菌。只有活菌显著缩小了斑块体积、改善了斑块结构并提高了血液中IAA水平,同时恢复了巨噬细胞中的AHR活性。直接给予IAA同样降低了斑块负担并使斑块更稳定,伴随更少的巨噬细胞死亡及更多的平滑肌和胶原。在细胞培养实验中,提高巨噬细胞内PSRC1水平可以通过减缓一种去泛素化酶UCHL3介导的降解来增加AHR蛋白,而敲低PSRC1则使细胞在应激下更易死亡。补充IAA可以逆转这一促死信号,但仅在AHR活性存在的情况下有效,表明IAA的保护作用依赖于该受体。
来自人类患者的线索
研究者还检查了接受心脏评估的人的血样。与没有显著冠状动脉阻塞的个体相比,冠状动脉疾病患者的循环IAA水平以及血液免疫细胞中PSRC1和AHR响应基因的表达均较低。统计分析表明,PSRC1表达较高与IAA水平较高和更强的AHR信号相关联,这与小鼠结果相呼应,支持在人类中也存在PSRC1–阿克曼氏菌–IAA–AHR轴的概念。
面向个体化心脏治疗的新路径
总体而言,该研究勾画出一条由肠到动脉的回路:PSRC1有助于维持健康的黏液屏障并支持阿克曼氏菌,阿克曼氏菌则从膳食色氨酸中产生IAA。IAA在巨噬细胞中激活AHR,限制其死亡并帮助保持斑块更小更稳定。当PSRC1丧失时,这一链条被削弱——阿克曼氏菌减少、IAA下降、AHR信号减弱,巨噬细胞更易死亡,斑块危险核心扩大。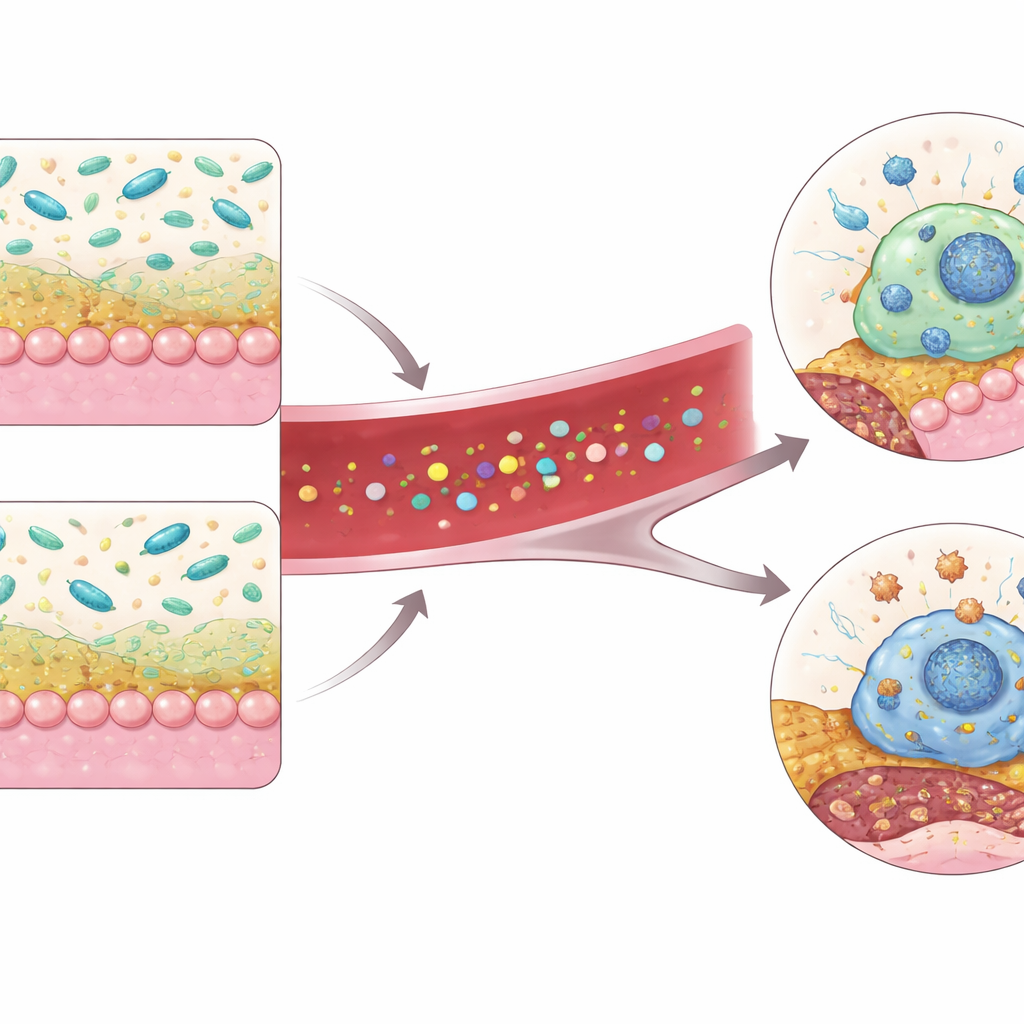
引用: Wu, Q., Hu, K., Wang, Q. et al. Proline/serine-rich coiled-coil 1 alleviates atherosclerosis via remodeling tryptophan metabolism mediated by Akkermansia muciniphila. Exp Mol Med 58, 848–863 (2026). https://doi.org/10.1038/s12276-026-01668-5
关键词: 动脉粥样硬化, 肠道微生物组, 色氨酸代谢, 粘膜阿克曼氏菌, 吲哚-3-乙酸